solo para uso en investigación
GW9662 Antagonista de PPARγ
Cat. No.S2915
Estructura química
Peso molecular: 276.68
Control de calidad
| Dianas relacionadas | HDAC PARP ATM/ATR DNA-PK WRN DNA/RNA Synthesis Topoisomerase Sirtuin Casein Kinase eIF |
|---|---|
| Otros PPAR Inhibidores | T0070907 GW6471 WY-14643 (Pirinixic Acid) GSK3787 GW0742 AZ6102 Harmine Astaxanthin Eupatilin GSK0660 |
Cultivo celular, tratamiento y concentración de trabajo
| Líneas celulares | Tipo de ensayo | Concentración | Tiempo de incubación | Formulación | Descripción de la actividad | PMID |
|---|---|---|---|---|---|---|
| 293H | Function assay | 30 mins | Antagonist activity at human PPARgamma expressed in 293H cells assessed as reduction in transcriptional response preincubated for 30 mins followed by addition and measured after 16 hrs by reporter gene-based FRET assay, EC50=0.002μM | 31294974 | ||
| Haga clic para ver más datos experimentales de líneas celulares | ||||||
Información química, almacenamiento y estabilidad
| Peso molecular | 276.68 | Fórmula | C13H9ClN2O3 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 22978-25-2 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | N/A | Smiles | C1=CC=C(C=C1)NC(=O)C2=C(C=CC(=C2)[N+](=O)[O-])Cl | ||
Solubilidad
|
In vitro |
DMSO
: 55 mg/mL
(198.78 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
PPARγ
(Cell-free assay) 3.3 nM
PPARα
(Cell-free assay) 32 nM
|
|---|---|
| In vitro |
GW9662 se une a Cys(285) en PPARgamma, que está conservado entre los tres PPAR. Este compuesto actúa como un antagonista de PPARgamma, lo que se confirma en un ensayo de inhibición de la diferenciación de adipocitos. Previene la activación de PPARγ e inhibe el crecimiento de líneas celulares de tumores mamarios humanos (MCF7, MDA-MB-468, MDA-MB-231) con una IC50 de 20 μM-30 μM, lo que sugiere la existencia de propiedades agonistas de PPARγ de esta sustancia química o mecanismos inhibidores del crecimiento independientes de PPARγ. El cotratamiento con este compuesto (10 μM) resulta en un número de células viables estadísticamente menor después de 7 días en células MDA-MB-231. Los ligandos de PPARγ1 podrían suprimir la formación de osteoclastos inducida por RANKL en células mieloides murinas primarias (BMs) y RAW264.7. Es importante destacar que la supresión por estos ligandos se revierte de forma dependiente de la concentración con esta sustancia química (2 μM). Este (2 μM) bloquea la supresión de la formación de osteoclastos por IL-4 en BMs. Este compuesto (1 μM) bloquea la activación de NF-κB por RANKL en células RAW264.7. GW9662 (10 μM) inhibe la adipogénesis inducida por hormonas y agonistas de preadipocitos primarios de pacientes con enfermedad ocular tiroidea. |
| Ensayo de quinasa |
Ensayo de unión
|
|
Los dominios de unión a ligando (LBDs) de PPARα, PPARγ y PPARδ humanos se expresan en E. coli como proteínas de fusión con etiqueta de polihistidina. Los receptores se inmovilizan en perlas SPA mediante la adición del receptor deseado (15 nM) a una suspensión de perlas SPA modificadas con estreptavidina (0,5 mg/mL) en tampón de ensayo. La mezcla se deja equilibrar durante al menos 1 hora a temperatura ambiente, y las perlas se precipitan por centrifugación a 1×103 g. El sobrenadante se desecha, y las perlas se resuspenden en el volumen original de tampón de ensayo fresco con agitación suave. El procedimiento de centrifugación/resuspensión se repite, y la suspensión resultante de perlas recubiertas de receptor se utiliza inmediatamente o se almacena a 4 ℃ durante un máximo de 1 semana antes de su uso. Se utilizan [3H]GW2443 como radioligandos para la determinación de la unión competitiva a PPARα, PPARγ y PPARδ, respectivamente. A menos que se indique lo contrario, el tampón utilizado para todos los ensayos es 50 mM HEPES (pH 7), 50 mM NaCl, 5 mM CHAPS, 0,1 mg/mL BSA y 10 mM DTT. Para algunos experimentos, el HEPES (pH 7) se reemplaza por 50 mM Tris (pH 8).
|
|
| In vivo |
El pretratamiento con LPS (1 mg/kg i.p.) atenúa significativamente todos los marcadores de lesión y disfunción renal causados por la lesión de isquemia/reperfusión (I/R) en ratas. En particular, este compuesto (1 mg/kg i.p.) anula los efectos protectores del LPS. |
Referencias |
|
Aplicaciones
| Métodos | Biomarcadores | Imágenes | PMID |
|---|---|---|---|
| Western blot | Vimentin / Slug / MMP9 / MMP2 |
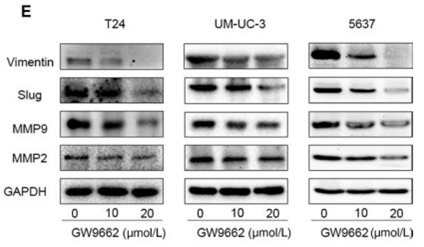
|
30912275 |
| Growth inhibition assay | Cell proliferation |
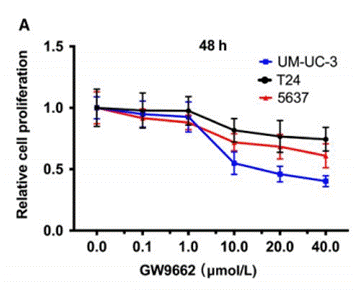
|
30912275 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
