solo para uso en investigación
Eupatilin PPAR agonista
Cat. No.S3846
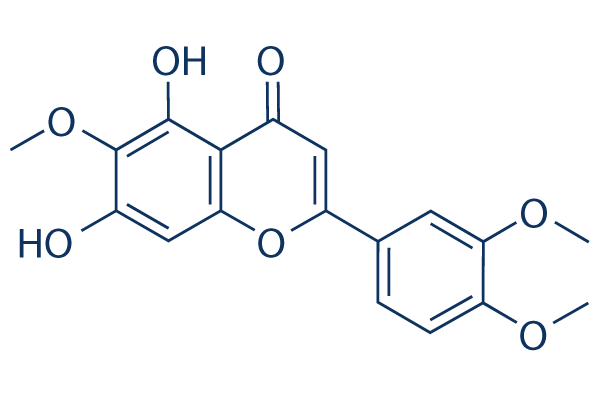
Estructura química
Peso molecular: 344.32
Control de calidad
| Dianas relacionadas | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase Vitamin Carbohydrate Metabolism Mitochondrial Metabolism Drug Metabolite |
|---|---|
| Otros PPAR Inhibidores | T0070907 GW9662 GW6471 WY-14643 (Pirinixic Acid) GSK3787 GW0742 AZ6102 Harmine Astaxanthin GSK0660 |
Información química, almacenamiento y estabilidad
| Peso molecular | 344.32 | Fórmula | C18H16O7 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 22368-21-4 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | NSC 122413 | Smiles | COC1=C(C=C(C=C1)C2=CC(=O)C3=C(O2)C=C(C(=C3O)OC)O)OC | ||
Solubilidad
|
In vitro |
DMSO
: 68 mg/mL
(197.49 mM)
|
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| In vitro |
Se ha informado que Eupatilin induce apoptosis en células AGS de cáncer gástrico humano y también desencadena la diferenciación de estas células. El tratamiento de células AGS con este compuesto induce la detención del ciclo celular en la fase G1 con la inducción concomitante de p21cip1, un inhibidor del ciclo celular. También induce marcadamente el factor trefoil 1 (TFF1). Este compuesto induce drásticamente la redistribución de proteínas de unión estrecha como la ocludina y ZO-1, y la F-actina en la región de unión entre las células. También induce la fosforilación de la quinasa 2 regulada por señales extracelulares y la quinasa p38. Se sabe que este químico inhibe el crecimiento de las células MCF-10A-ras al inhibir la expresión de reguladores del ciclo celular como la ciclina D1, la ciclina B1, Cdk2 y Cdc2.
|
|---|---|
| In vivo |
El tratamiento con eupatilin disminuye significativamente la alanina aminotransferasa sérica y la aspartato aminotransferasa sérica, así como los cambios histológicos hepáticos. Este compuesto también previene el agotamiento del glutatión hepático y aumenta los niveles de malondialdehído inducidos por la lesión por isquemia-reperfusión (IRI). Mejora la IRI hepática aguda al reducir la inflamación y la apoptosis. La administración oral de este químico (10 mg/kg) en un paradigma terapéutico reduce significativamente el infarto cerebral y mejora las funciones neurológicas en ratones desafiados con tMCAO. Su administración reduce el número de células inmunopositivas Iba1 en el cerebro isquémico e induce sus cambios morfológicos de ameboides a ramificadas en el núcleo isquémico, lo que se acompaña de una proliferación microglial reducida en el cerebro isquémico. Este agente suprime las actividades de señalización de NF-κB en el cerebro isquémico al reducir la fosforilación de IKKα/β, la fosforilación de IκBα y la degradación de IκBα.
|
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
