solo para uso en investigación
Echinocystic acid Immunology & Inflammation related químico
Cat. No.S3837
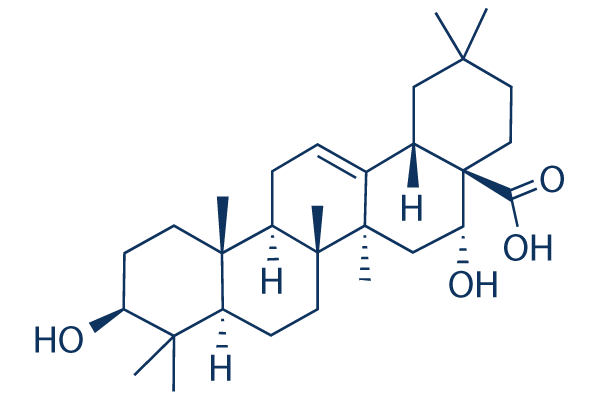
Estructura química
Peso molecular: 472.70
Control de calidad
- Citado en Nature Medicine por su máxima calidad
- COA
- NMR
- SDS
- Hoja de datos
| Dianas relacionadas | PD-1/PD-L1 CXCR STING AhR CD markers Interleukins Anti-infection Antioxidant COX Histamine Receptor |
|---|---|
| Otros Immunology & Inflammation related Inhibidores | Cl-amidine Bestatin (Ubenimex) Bindarit (AF 2838) Tranilast Tempol Sinomenine GI254023X (GI4023) ATP Geniposidic acid CORM-3 |
Información química, almacenamiento y estabilidad
| Peso molecular | 472.70 | Fórmula | C30H48O4 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 510-30-5 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | N/A | Smiles | CC1(CCC2(C(C1)C3=CCC4C5(CCC(C(C5CCC4(C3(CC2O)C)C)(C)C)O)C)C(=O)O)C | ||
Solubilidad
|
In vitro |
DMSO
: 94 mg/mL
(198.85 mM)
|
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| In vitro |
El Echinocystic acid (EA) podría inducir apoptosis en células HepG2 humanas, caracterizada por la fragmentación del ADN, la activación de caspasa-3, -8 y -9, y la escisión de PARP. El EA induce la truncación de la proteína Bid y la reducción de la proteína Bcl-2. El EA también causa la pérdida del potencial de membrana mitocondrial (ΔΨm) y la liberación de citocromo c de las mitocondrias al citosol. Además, el EA podría activar la cinasa c-Jun NH2-terminal (JNK) y la cinasa p38, y el inhibidor específico de JNK SP600125 y el inhibidor específico de la cinasa p38 SB200235 podrían bloquear los eventos moleculares en serie de la apoptosis inducida por EA, como la truncación de Bid, la reducción de Bcl-2, la liberación de citocromo c, la activación de caspasas y la fragmentación del ADN en células HepG2. El EA inhibe la proliferación de células HepG2 de manera dosis-dependiente con un valor de IC50 de 45,4 μM en un tratamiento de 24h.
|
|---|---|
| In vivo |
Se ha descubierto que la administración de Echinocystic acid (EA) mejora el estrés máximo y el módulo de Young del fémur en ratas OVX. El análisis de microtomografía computarizada revela que el EA podría mejorar la arquitectura trabecular, como se muestra por el aumento de BV/TV, Tb.N y Tb.Th en ratas OVX. Sin embargo, el EA no afecta el peso corporal ni el peso uterino. Se ha demostrado que el EA ejerce un efecto antiinflamatorio en diferentes modelos de inflamación crónica en ratones mediante la regulación a la baja de citoquinas proinflamatorias como IL-1β, IL-18, TNF-α. El EA atenúa la díada dolor/depresión inducida por reserpina parcialmente a través de la regulación de los niveles de aminas biogénicas y los receptores GluN2B en el hipocampo.
|
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
