solo para uso en investigación
Eleutheroside B Immunology & Inflammation related químico
Cat. No.S3841
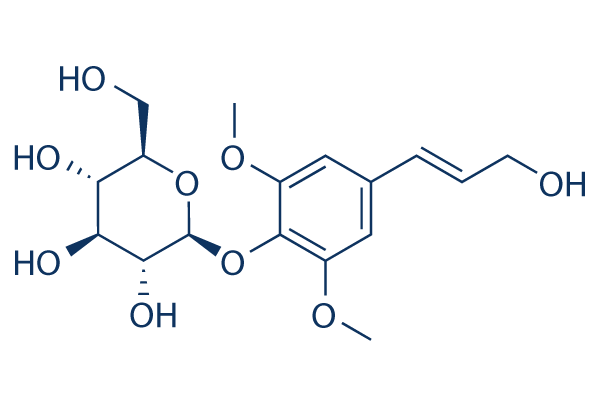
Estructura química
Peso molecular: 372.37
Control de calidad
- Citado en Nature Medicine por su máxima calidad
- COA
- HPLC
- SDS
- Hoja de datos
| Dianas relacionadas | PD-1/PD-L1 CXCR STING AhR CD markers Interleukins Anti-infection Antioxidant COX Histamine Receptor |
|---|---|
| Otros Immunology & Inflammation related Inhibidores | Cl-amidine Bestatin (Ubenimex) Bindarit (AF 2838) Tranilast Tempol Sinomenine GI254023X (GI4023) ATP Geniposidic acid CORM-3 |
Información química, almacenamiento y estabilidad
| Peso molecular | 372.37 | Fórmula | C17H24O9 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 118-34-3 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | syringin, Syringoside, Lilacin | Smiles | COC1=CC(=CC(=C1OC2C(C(C(C(O2)CO)O)O)O)OC)C=CCO | ||
Solubilidad
|
In vitro |
DMSO
: 74 mg/mL
(198.72 mM)
|
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| In vitro |
La siringina muestra baja citotoxicidad en las células U937 y PBMC con un IC50 de >100 y 91.14 mg/mL, respectivamente.
|
|---|---|
| In vivo |
La siringina tiene una potente protección contra la insuficiencia hepática fulminante (FHF) inducida por LPS/D-GalN, como lo indica la disminución de la alta letalidad, alivia la lesión patológica hepática, inhibe la apoptosis de los hepatocitos y reduce las respuestas inflamatorias hepáticas. Dichos efectos protectores probablemente se llevan a cabo a través de la supresión de la producción de TNF-α, mediada por NF-kB. La siringina también protege contra la lesión pulmonar aguda (ALI) inducida por LPS al activar Nrf2 e inhibir la vía de señalización NF-κB. La siringina mejora la tolerancia a la glucosa sin un aumento de peso en ratones obesos inducidos por una dieta alta en grasas. Aumenta la fosforilación de Akt estimulada por insulina en el músculo esquelético, el tejido adiposo epididimal (EAT) y el hígado, mostrando una actividad sensibilizadora a la insulina. Los ratones tratados con siringina también muestran una producción marcadamente elevada de adiponectina en EAT y suprimen la expresión de citocinas proinflamatorias en los tejidos periféricos, lo que indica una reducción significativa de la inflamación crónica de bajo grado. Además, la siringina mejora la actividad de la proteína quinasa activada por AMP y disminuye la expresión de genes lipogénicos en el músculo esquelético, lo que se asocia con una reducción del estrés del retículo endoplasmático (ER).
|
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
