solo para uso en investigación
TAK-632 Raf inhibidor
Cat. No.S7291
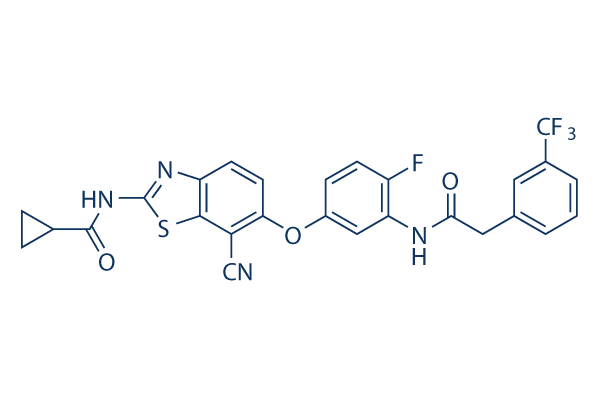
Estructura química
Peso molecular: 554.52
Control de calidad
| Dianas relacionadas | ERK p38 MAPK JNK MEK Ras KRas S6 Kinase MAP4K TAK1 Mixed Lineage Kinase |
|---|---|
| Otros Raf Inhibidores | LY3009120 Exarafenib (KIN-2787) GDC-0879 Avutometinib (Ro5126766, CH5126766) PLX-4720 AZ 628 SB590885 GW5074 RAF265 (CHIR-265) PLX8394 (Plixorafenib, FORE8394) |
Cultivo celular, tratamiento y concentración de trabajo
| Líneas celulares | Tipo de ensayo | Concentración | Tiempo de incubación | Formulación | Descripción de la actividad | PMID |
|---|---|---|---|---|---|---|
| human A375 cells | Function assay | 2 h | Inhibition of BRAF V600E mutant in human A375 cells assessed as phosphorylation of MEK after 2 hrs by Western blotting analysis, IC50=12 nM | |||
| human HMVII cells | Function assay | 2 h | Inhibition of NRASQ61k/BRAFG469V-mutant in human HMVII cells assessed as phosphorylation of MEK after 2 hrs by Western blotting analysis, IC50=49 nM | |||
| human HT-29 cells | Function assay | Inhibition of BRAF V600E mutant in human HT-29 cells assessed as phosphorylation of MEK, IC50=75 nM | ||||
| human HMVII cells | Proliferation assay | 72 h | Antiproliferative activity against human HMVII cells assessed as growth inhibition after 72 hrs by chemi-luminescence cell viability assay, GI50=0.2 μM | |||
| 293 cells | Function assay | 20 mins | Inhibition of N-terminal GST-tagged MEK1 (unknown origin) expressed in 293 cells using GST-ERK1(K71A) as substrate after 20 mins, IC50=3.7 μM | |||
| Haga clic para ver más datos experimentales de líneas celulares | ||||||
Información química, almacenamiento y estabilidad
| Peso molecular | 554.52 | Fórmula | C27H18F4N4O3S |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 1228591-30-7 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | N/A | Smiles | C1CC1C(=O)NC2=NC3=C(S2)C(=C(C=C3)OC4=CC(=C(C=C4)F)NC(=O)CC5=CC(=CC=C5)C(F)(F)F)C#N | ||
Solubilidad
|
In vitro |
DMSO
: 100 mg/mL
(180.33 mM)
Ethanol : 2 mg/mL Water : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Características |
Orally bioavailable, pan-raf inhibitor that targets both wild-type and mutant forms.
|
|---|---|
| Targets/IC50/Ki |
C-Raf
(Cell-free assay) 1.4 nM
B-Raf
(Cell-free assay) 8.3 nM
Aurora B
(Cell-free assay) 66 nM
PDGFRβ
(Cell-free assay) 120 nM
FGFR3
(Cell-free assay) 280 nM
GSK-3β
(Cell-free assay) 500 nM
CDK2
(Cell-free assay) 580 nM
p38α
(Cell-free assay) 600 nM
PDGFRα
(Cell-free assay) 610 nM
|
| In vitro |
TAK-632 inhibe la fosforilación de MEK y ERK en células de melanoma A375 (BRAFV600E) con una IC50 de 12 nM y 16 nM, respectivamente. En células de melanoma humano HMVII (NRASQ61K/BRAFG469V), este compuesto también muestra una fuerte inhibición de pMEK y pERK con una IC50 de 49 nM y 50 nM, respectivamente. Además, también exhibe actividad antiproliferativa en ambas células A375 y HMVII con una GI50 de 66 nM y 200 nM, respectivamente. Este químico induce la dimerización de RAF pero inhibe la actividad quinasa del dímero RAF debido a su lenta disociación de RAF. La combinación de este compuesto y TAK-733 exhibe efectos antiproliferativos sinérgicos en células de melanoma con mutaciones en BRAF y NRAS.
|
| Ensayo de quinasa |
Ensayo de perfil de quinasa
|
|
Los ensayos para quinasas de serina/treonina que utilizan ATP radiomarcado [γ-33P] se realizan en placas de 96 pocillos. BRAF y c-RAF se expresan como proteína con etiqueta FLAG N-terminal utilizando un sistema de expresión de baculovirus. Las condiciones de reacción se optimizan para cada quinasa: BRAF (25 ng/pocillo de enzima, 1 μg/pocillo de GST-MEK1(K96R), 0,1 μCi/pocillo de ATP [γ-32P], temperatura ambiente, 20 min de reacción); c-RAF (25 ng/pocillo de enzima, 1 μg/pocillo de GST-MEK1 (K96R), 0,1 μCi/pocillo de ATP [γ-32P], temperatura ambiente, 20 min de reacción). Las reacciones enzimáticas se realizan en 25 mM HEPES, pH 7,5, 10 mM de acetato de magnesio, 1 mM de ditiotreitol y 0,5 μM de ATP que contienen una concentración optimizada de enzima, sustrato y ATP radiomarcado como se describió anteriormente en un volumen total de 50 μL. Antes de la reacción de la quinasa, este compuesto y la enzima se incuban durante 5 min a la temperatura de reacción descrita anteriormente. Las reacciones de la quinasa se inician añadiendo ATP. Después del período de reacción descrito anteriormente, las reacciones se terminan con la adición de ácido tricloroacético al 10% (concentración final). Las proteínas fosforiladas con [γ-33P] o [γ-32P] se filtran en placas de filtro GFC con un Cell Harvester y luego las placas se lavan con ácido fosfórico al 3%. Las placas se secan, seguido de la adición de 40 μL de MicroScint0. La radioactividad se cuenta con un contador de centelleo TopCount.
|
|
| In vivo |
TAK-632 muestra una biodisponibilidad oral superior tanto en ratas como en perros. Este compuesto (3,9–24,1 mg/kg, p.o.) exhibe una eficacia antitumoral dosis-dependiente sin una reducción grave del peso corporal en un modelo de xenoinjerto de melanoma A375 (BRAFV600E) y un xenoinjerto de melanoma humano HMVII (NRASQ61K/BRAFG469V) en ratas. En el modelo de xenoinjerto de melanoma SK-MEL-2 mutante en NRAS, este químico (60 o 120 mg/kg, p.o.) también exhibe una potente eficacia antitumoral sin toxicidad grave.
|
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
