solo para uso en investigación
BGP-15 2HCl PARP inhibidor
Cat. No.S8370
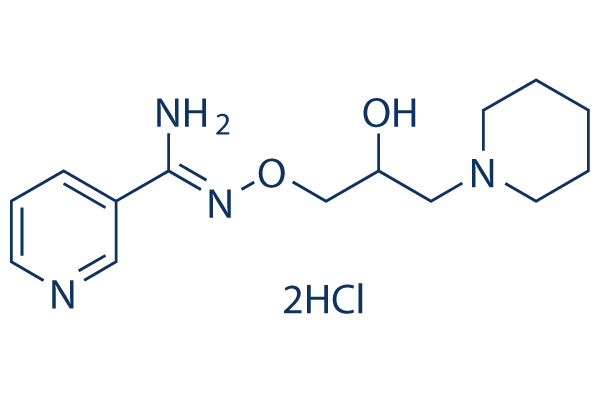
Estructura química
Peso molecular: 351.27
Control de calidad
- Citado en Nature Medicine por su máxima calidad
- COA
- NMR
- HPLC
- SDS
- Hoja de datos
| Dianas relacionadas | HDAC ATM/ATR DNA-PK WRN DNA/RNA Synthesis Topoisomerase PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Otros PARP Inhibidores | XAV-939 AZD5305 (Saruparib) Veliparib (ABT-888) PJ34 HCl AG-14361 Iniparib (BSI-201) G007-LK Pamiparib UPF 1069 A-966492 |
Información química, almacenamiento y estabilidad
| Peso molecular | 351.27 | Fórmula | C14H22N4O2.2HCl |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 66611-37-8 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | N/A | Smiles | C1CCN(CC1)CC(CON=C(C2=CN=CC=C2)N)O.Cl.Cl | ||
Solubilidad
|
In vitro |
DMSO
: 70 mg/mL
(199.27 mM)
Water : 70 mg/mL Ethanol : 70 mg/mL |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
PARP
|
|---|---|
| In vitro |
El derivado de hidroxilamina BGP-15 es un coinductor de HSP72 in vitro, pero solo en presencia de cotratamiento con calor y no tuvo efecto sobre los niveles de HSP90. BGP-15 (200 μM) previno los daños oxidativos inducidos por el mesilato de imatinib, atenuó el agotamiento de los fosfatos de alta energía, alteró el efecto de señalización del mesilato de imatinib al prevenir la activación de la MAP quinasa p38 y JNK, e indujo la fosforilación de Akt y GSK-3beta. El efecto supresor de BGP-15 sobre la activación de p38 y JNK podría ser significativo porque estas quinasas contribuyen a la muerte celular y la inflamación en el corazón perfundido aislado.
|
| In vivo |
BGP-15 mejora la función cardíaca y reduce los episodios arrítmicos en dos modelos de ratón independientes, que desarrollan progresivamente IC y FA. BGP-15 administrado en dosis orales de 100-200 mg/kg poco antes del tratamiento con cisplatino previno o inhibió significativamente el desarrollo de insuficiencia renal aguda inducida por cisplatino. BGP-15 tuvo un efecto significativo sobre el estado antioxidante del riñón durante la nefrotoxicidad inducida por cisplatino. Elevó los niveles disminuidos de glutatión y catalasa, pero no afectó la actividad de SOD. El tratamiento con BGP-15 disminuyó la producción de ROS causada por cisplatino y restauró el nivel de intermediarios de fosfato de alta energía. Si bien BGP-15 protegió contra la nefrotoxicidad inducida por cisplatino, no redujo la eficacia antitumoral de este agente citostático. BGP-15 aumentó la supervivencia de ratones con leucemia P-388 tratados con cisplatino. BGP-15 inhibe la poli-ADP-ribosilación inducida por cisplatino en el riñón. Al mismo tiempo, BGP-15 restauró la alteración del metabolismo energético inducida por cisplatino y preservó el nivel de ATP en el tejido protegido.
|
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
