solo para uso en investigación
AG-14361 PARP inhibidor
Cat. No.S2178
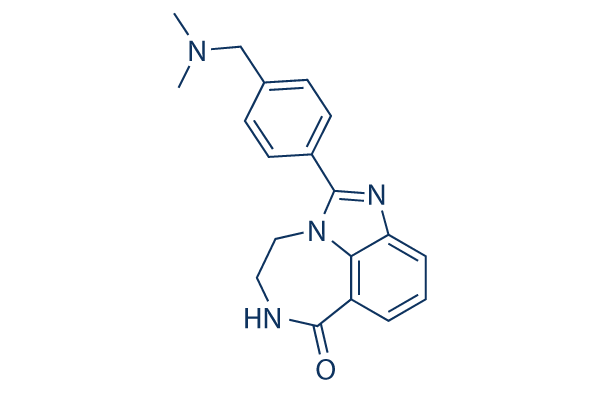
Estructura química
Peso molecular: 320.39
Control de calidad
| Dianas relacionadas | HDAC ATM/ATR DNA-PK WRN DNA/RNA Synthesis Topoisomerase PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Otros PARP Inhibidores | XAV-939 AZD5305 (Saruparib) Veliparib (ABT-888) PJ34 HCl Iniparib (BSI-201) G007-LK Pamiparib UPF 1069 A-966492 Stenoparib (E7449) |
Cultivo celular, tratamiento y concentración de trabajo
| Líneas celulares | Tipo de ensayo | Concentración | Tiempo de incubación | Formulación | Descripción de la actividad | PMID |
|---|---|---|---|---|---|---|
| LoVo cells | Function assay | Concentration that gives 50% growth inhibition in LoVo cells, activity expressed as GI50, GI50=11.2 μM | ||||
| Haga clic para ver más datos experimentales de líneas celulares | ||||||
Información química, almacenamiento y estabilidad
| Peso molecular | 320.39 | Fórmula | C19H20N4O |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 328543-09-5 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | N/A | Smiles | CN(C)CC1=CC=C(C=C1)C2=NC3=CC=CC4=C3N2CCNC4=O | ||
Solubilidad
|
In vitro |
DMSO
: 51 mg/mL
(159.18 mM)
Ethanol : 21 mg/mL Water : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Características |
The 1st high-potency PARP-1 inhibitor with the specificity & in vivo activity to enhance chemotherapy and radiation therapy of human cancers.
|
|---|---|
| Targets/IC50/Ki |
PARP1
(Cell-free assay) <5 nM(Ki)
|
| In vitro |
AG14361 es al menos 1000 veces más potente que las benzamidas. El IC50 para AG14361 es de 29 nM en células SW620 permeabilizadas y de 14 nM en células SW620 intactas. El análisis cristalográfico de AG14361 unido al dominio catalítico de PARP-1 de pollo muestra que el sistema de anillo tricíclico de AG14361 se encuentra en un bolsillo compuesto por los residuos de aminoácidos Trp861, His862, Gly863, Tyr896, Phe897, Ala898, Lys903, Ser904, Tyr907 y Glu988. AG14361 forma importantes enlaces de hidrógeno con Ser904 y Gly863 y un enlace de hidrógeno mediado por agua con Glu988. La inhibición del crecimiento inducida por AG14361 no se atribuye a efectos relacionados con PARP-1 porque la inhibición máxima de PARP-1 se observa a concentraciones mucho más bajas (≤1 μM) que la GI50. AG14361 a 0,4 μM no afecta la expresión génica ni el crecimiento de las células cancerosas, pero aumenta la actividad antiproliferativa e inhibe la recuperación del daño por radiación γ potencialmente letal en células LoVo en un 73%. Además, 0,4 μM AG14361 no altera sustancialmente la expresión génica, como lo demuestra el análisis de microarrays. Una exposición de 17 horas de células A549 a 0,4 μM AG14361 no cambia la expresión de los 6800 genes. Por lo tanto, aunque 0,4 μM AG14361 inhibe la actividad de PARP-1 celular en más del 85%, esencialmente no cambia la expresión génica y la proliferación celular, lo que indica que los efectos celulares de esta baja concentración de AG14361 son específicos para la inhibición de PARP-1. Concentraciones más altas e inhibitorias del crecimiento de AG14361 afectan la expresión génica, pero es poco probable que estos efectos estén relacionados con la inhibición de PARP-1 porque la proliferación celular se ve afectada por igual en células PARP-/- y PARP-1+/+. AG14361 se absorbe rápidamente en el torrente sanguíneo y se distribuye al tumor y al hígado con concentraciones más bajas detectadas en el cerebro. La relación de concentración tejido-plasma indica que AG14361 se retiene en el tejido tumoral con el tiempo en ambos modelos de xenoinjertos, con concentraciones tumorales (≥15 μM durante 2 horas) que exceden las requeridas para inhibir la actividad de PARP-1 in vitro. AG14361 mejora la actividad en todas las células competentes en MMR (1,5–3,3 veces) pero es más eficaz en células deficientes en MMR (potenciación de 3,7–5,2 veces), superando la resistencia. En contraste, la bencilguanina solo aumenta la eficacia en células competentes en MMR pero es ineficaz en células deficientes en MMR. AG14361 mejora los efectos inhibidores del crecimiento y citotóxicos de los venenos de topoisomerasa I. AG14361 aumenta la persistencia de las roturas de ADN de una sola hebra inducidas por camptotecina. |
| Ensayo de quinasa |
Ensayos de actividad PARP-1
|
|
La actividad de la PARP-1 humana recombinante de longitud completa se mide en una mezcla de reacción que contiene 20 nM PARP-1, 500 μM NAD+ más [32P]NAD+ (0,1–0,3 μCi por mezcla de reacción) y ADN de timo de ternera activado (10 μg/mL) a 25oC; la reacción se termina después de 4 minutos añadiendo ácido tricloroacético helado al 10% (p/v). El producto de la reacción [32P]ADP-ribosa incorporado en material insoluble en ácido se deposita en filtros de fibra de vidrio Whatman GF/C con un aparato de microfiltración Bio-Dot y se cuantifica con un PhosphorImager. Se mide la inhibición de la actividad de PARP-1 por AG14361 a 0–600 nM, y el Ki para AG14361 se calcula mediante análisis de regresión no lineal.
|
|
| In vivo |
El tratamiento con AG14361 antes de la irradiación aumenta de forma estadísticamente significativa la sensibilidad a la radioterapia de ratones portadores de xenoinjertos LoVo. AG14361 aumenta de forma estadísticamente significativa el flujo sanguíneo en los xenoinjertos y, por lo tanto, aumenta potencialmente la administración de fármacos a los xenoinjertos tumorales. In vivo, dosis no tóxicas de AG14361 aumentan el retraso del crecimiento de los xenoinjertos LoVo inducido por la irradiación de rayos X en 2 a 3 veces. La coadministración de AG14361 aumenta de forma estadísticamente significativa la actividad contra los xenoinjertos LoVo, con un retraso del crecimiento tumoral que aumenta de 3 días a 9 días con AG14361 a 5 mg/kg y a 10 días con AG14361 a 15 mg/kg. La combinación de AG14361 provoca una regresión completa de los tumores de xenoinjerto SW620. La actividad de PARP-1, detectada mediante un ensayo farmacodinámico, en los xenoinjertos SW620 se inhibe en más del 75% durante al menos 4 horas después de la administración intraperitoneal de AG14361 (10 mg/kg), lo que concuerda con la concentración de AG14361 que persiste en el tumor. |
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
