solo para uso en investigación
Neratinib (HKI-272) Inhibidor de HER2/EGFR
Cat. No.S2150
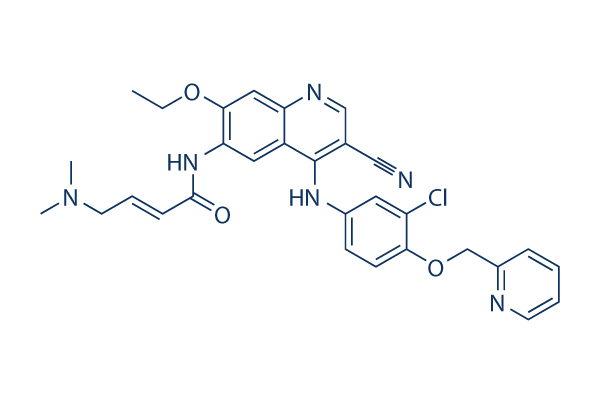
Estructura química
Peso molecular: 557.04
Control de calidad
| Dianas relacionadas | EGFR VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 c-Kit |
|---|---|
| Otros HER2 Inhibidores | CP-724714 Sapitinib (AZD8931) Mubritinib (TAK 165) AC480 (BMS-599626) Tyrphostin AG 879 HER2-Inhibitor-1 TAS0728 Zongertinib |
Cultivo celular, tratamiento y concentración de trabajo
| Líneas celulares | Tipo de ensayo | Concentración | Tiempo de incubación | Formulación | Descripción de la actividad | PMID |
|---|---|---|---|---|---|---|
| BT-474 | Growth Inhibition Assay | IC50<0.005 μM | 24009064 | |||
| EFM-192A | Growth Inhibition Assay | IC50<0.005 μM | 24009064 | |||
| HCC1569 | Growth Inhibition Assay | IC50<0.005 μM | 24009064 | |||
| HCC1954 | Growth Inhibition Assay | IC50<0.005 μM | 24009064 | |||
| MDA-MB-175 | Growth Inhibition Assay | IC50<0.005 μM | 24009064 | |||
| MDA-MB-361 | Growth Inhibition Assay | IC50<0.005 μM | 24009064 | |||
| SK-BR-3 | Growth Inhibition Assay | IC50<0.005 μM | 24009064 | |||
| UACC-812 | Growth Inhibition Assay | IC50<0.005 μM | 24009064 | |||
| UACC-893 | Growth Inhibition Assay | IC50<0.005 μM | 24009064 | |||
| SUM-225 | Growth Inhibition Assay | IC50=0.01 μM | 24009064 | |||
| SUM-190 | Growth Inhibition Assay | IC50=0.01 μM | 24009064 | |||
| ZR-75-1 | Growth Inhibition Assay | IC50=0.03 μM | 24009064 | |||
| HCC70 | Growth Inhibition Assay | IC50=0.03 μM | 24009064 | |||
| BT-20 | Growth Inhibition Assay | IC50=0.07 μM | 24009064 | |||
| MDA-MB-453 | Growth Inhibition Assay | IC50=0.09 μM | 24009064 | |||
| HCC1187 | Growth Inhibition Assay | IC50=0.10 μM | 24009064 | |||
| EFM-19 | Growth Inhibition Assay | IC50=0.11 μM | 24009064 | |||
| T-47D | Growth Inhibition Assay | IC50=0.16 μM | 24009064 | |||
| MDA-MB-134 | Growth Inhibition Assay | IC50=0.17 μM | 24009064 | |||
| HCC38 | Growth Inhibition Assay | IC50=0.25 μM | 24009064 | |||
| MDA-MB-435 | Growth Inhibition Assay | IC50=0.33 μM | 24009064 | |||
| MDA-MB-468 | Growth Inhibition Assay | IC50=0.33 μM | 24009064 | |||
| CAMA-1 | Growth Inhibition Assay | IC50=0.37 μM | 24009064 | |||
| MDA-MB-436 | Growth Inhibition Assay | IC50=0.41 μM | 24009064 | |||
| MCF-7 | Growth Inhibition Assay | IC50=0.41 μM | 24009064 | |||
| MDA-MB-415 | Growth Inhibition Assay | IC50=0.42 μM | 24009064 | |||
| HCC1806 | Growth Inhibition Assay | IC50=0.44 μM | 24009064 | |||
| HCC1395 | Growth Inhibition Assay | IC50=0.49 μM | 24009064 | |||
| HCC1937 | Growth Inhibition Assay | IC50=0.50 μM | 24009064 | |||
| HCC1143 | Growth Inhibition Assay | IC50=0.54 μM | 24009064 | |||
| UACC-732 | Growth Inhibition Assay | IC50=0.65 μM | 24009064 | |||
| MDA-MB-231 | Growth Inhibition Assay | IC50=1.00 μM | 24009064 | |||
| MDA-MB-157 | Growth Inhibition Assay | IC50=1.12 μM | 24009064 | |||
| BT-549 | Growth Inhibition Assay | IC50=1.14 μM | 24009064 | |||
| KPL-1 | Growth Inhibition Assay | IC50=1.89 μM | 24009064 | |||
| CAL-51 | Growth Inhibition Assay | IC50=1.89 μM | 24009064 | |||
| BT474 | Growth Inhibition Assay | IC50=0.00323 ± 0.00075 μM | 23816254 | |||
| SKBR3 | Growth Inhibition Assay | IC50=0.0075 ± 0.005 μM | 23816254 | |||
| MDAMB453 | Growth Inhibition Assay | IC50=1.59 ± 0.179 μM | 23816254 | |||
| KB | Growth Inhibition Assay | IC50=4.13 ± 0.47 μM | 22491935 | |||
| KBv200 | Growth Inhibition Assay | IC50=6.03 ± 0.64 μM | 22491935 | |||
| MCF-7 | Growth Inhibition Assay | IC50=3.30 ± 0.41 μM | 22491935 | |||
| MCF-7/Adr | Growth Inhibition Assay | IC50= 2.88 ± 0.30 μM | 22491935 | |||
| MCF-7 | Growth Inhibition Assay | IC50=3.02 ± 0.34 μM | 22491935 | |||
| MCF-7/FLV1000 | Growth Inhibition Assay | IC50=7.09 ± 0.71 μM | 22491935 | |||
| HL60 | Growth Inhibition Assay | IC50=2.26 ± 0.23 μM | 22491935 | |||
| HL60/Adr | Growth Inhibition Assay | IC50=1.42 ± 0.15 μM | 22491935 | |||
| HEK293/pcDNA3.1 | Growth Inhibition Assay | IC50=5.29 ± 0.53 μM | 22491935 | |||
| HEK293/ABCB1 | Growth Inhibition Assay | IC50=6.91 ± 0.70 μM | 22491935 | |||
| SKBR | Growth Inhibition Assay | 0.01-100 nM | 3-7 d | inhibits cell growth in time and dose dependent manner | 21487605 | |
| L858R(EGFR) | Cell Viability Assay | decreases cell viability in time and dose dependent manner | 17311002 | |||
| L858R/T790M(EGFR) | Cell Viability Assay | decreases cell viability in time and dose dependent manner | 17311002 | |||
| G776insV_G/C | Cell Viability Assay | decreases cell viability in time and dose dependent manner | 17311002 | |||
| wild-type | Cell Viability Assay | decreases cell viability in time and dose dependent manner | 17311002 | |||
| A775insYVMA | Cell Viability Assay | decreases cell viability in time and dose dependent manner | 17311002 | |||
| G776insV_G/L | Cell Viability Assay | decreases cell viability in time and dose dependent manner | 17311002 | |||
| P780insGSP | Cell Viability Assay | decreases cell viability in time and dose dependent manner | 17311002 | |||
| NCI-H1781 | Growth Inhibition Assay | inhibits cell growth in time and dose dependent manner | 16818618 | |||
| HCC827 | Growth Inhibition Assay | inhibits cell growth in time and dose dependent manner | 16818618 | |||
| H3255 | Growth Inhibition Assay | inhibits cell growth in time and dose dependent manner | 16818618 | |||
| NCI-H1975 | Growth Inhibition Assay | inhibits cell growth in time and dose dependent manner | 16818618 | |||
| A549 | Growth Inhibition Assay | inhibits cell growth in time and dose dependent manner | 16818618 | |||
| 3T3 | Growth Inhibition Assay | IC50=700 ± 78 nM | 15173008 | |||
| 3T3/neu | Growth Inhibition Assay | IC50=3 ± 0.14 nM | 15173008 | |||
| SK-Br-3 | Growth Inhibition Assay | IC50=2 ± 0.18 nM | 15173008 | |||
| BT 474 | Growth Inhibition Assay | IC50=2 ± 0.06 nM | 15173008 | |||
| A431 | Growth Inhibition Assay | IC50=81 ± 9 nM | 15173008 | |||
| MDA-MB-435 | Growth Inhibition Assay | IC50=960 ± 165 nM | 15173008 | |||
| SW620 | Growth Inhibition Assay | IC50=690 ± 84 nM | 15173008 | |||
| SKBR3 | Function assay | Inhibition of human Her2 in SKBR3 cells, EC50 = 0.002 μM. | 18077425 | |||
| BT474 | Function assay | Inhibition of human Her2 in BT474 cells, EC50 = 0.002 μM. | 18077425 | |||
| A431 | Function assay | Inhibition of human Her2 in A431 cells, EC50 = 0.081 μM. | 18077425 | |||
| SW620 | Function assay | Inhibition of human Her2 in SW620 cells, EC50 = 0.69 μM. | 18077425 | |||
| BA/F3 | Cytotoxicity assay | Cytotoxicity against mouse BA/F3 cells expressing EGFR L858R mutant, IC50 = 0.0035 μM. | 19239229 | |||
| BA/F3 | Cytotoxicity assay | Cytotoxicity against mouse BA/F3 cells expressing EGFR L858R/T790M mutant, IC50 = 0.18 μM. | 19239229 | |||
| Sf9 | Function assay | 10 mins | Inhibition of human wild type EGFR expressed in Sf9 cells using [gamma32P]-ATP after 10 mins by scintillation counting, IC50 = 0.0025 μM. | 24900643 | ||
| Sf9 | Function assay | 10 mins | Inhibition of human EGFR T790M/L858R mutant expressed in Sf9 cells using [gamma32P]-ATP after 10 mins by scintillation counting, IC50 = 0.066 μM. | 24900643 | ||
| BAF3 | Function assay | 72 hrs | Inhibition of Tel-fused IGF1R (unknown origin) expressed in mouse BAF3 cells assessed as growth inhibition after 72 hrs by CellTiter-Glo assay, GI50 = 0.19 μM. | 28282122 | ||
| BAF3 | Function assay | 72 hrs | Inhibition of Tel-fused INSR (unknown origin) expressed in mouse BAF3 cells assessed as growth inhibition after 72 hrs by CellTiter-Glo assay, GI50 = 0.29 μM. | 28282122 | ||
| BAF3 | Growth inhibition assay | 72 hrs | Growth inhibition of mouse BAF3 cells after 72 hrs by CellTiter-Glo assay, GI50 = 1.9 μM. | 28282122 | ||
| Haga clic para ver más datos experimentales de líneas celulares | ||||||
Información química, almacenamiento y estabilidad
| Peso molecular | 557.04 | Fórmula | C30H29ClN6O3 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 698387-09-6 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | HKI-272 | Smiles | CCOC1=C(C=C2C(=C1)N=CC(=C2NC3=CC(=C(C=C3)OCC4=CC=CC=N4)Cl)C#N)NC(=O)C=CCN(C)C | ||
Solubilidad
|
In vitro |
DMSO
: 6 mg/mL
(10.77 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
HER2
(Cell-free assay) 59 nM
EGFR
(Cell-free assay) 92 nM
KDR
(Cell-free assay) 800 nM
Src
(Cell-free assay) 1.4 μM
|
|---|---|
| In vitro |
Neratinib inhibe débilmente las tirosina quinasas KDR y Src con IC50 de 0,8 μM y 1,4 μM, respectivamente, siendo 14 y 24 veces menos activo en comparación con HER2. Este compuesto no muestra actividad contra otras serina-treonina quinasas como Akt, ciclina D1/cdk4, ciclina E/cdk2, ciclina B1/cdk1, IKK-2, MK-2, PDK1, c-Raf y Tpl-2, así como la tirosina quinasa c-Met. Inhibe selectivamente la proliferación de células 3T3 transfectadas con HER2 (3T3/neu), así como otras dos células SK-Br-3 y BT474 que sobreexpresan HER-2 con valores de IC50 de 2-3 nM, mostrando una potencia >230 veces mayor en comparación con células 3T3 no transfectadas, así como MDA-MB-435 y SW620 que son negativas para EGFR y HER2. Este químico también inhibe la proliferación de células A431 dependientes de EGFR con una IC50 de 81 nM. Reduce la autofosforilación del receptor HER2 en células BT474 con una IC50 de 5 nM, y la fosforilación de EGFR dependiente de EGF en células A431 con una IC50 de 3 nM. El bloqueo de HER-2 por este compuesto resulta en la inhibición de las vías MAPK y Akt corriente abajo con una IC50 de 2 nM, más potentemente que Trastuzumab. Inhibe la expresión de ciclina D1 y la fosforilación de la producción del gen de susceptibilidad a Rb en células BT474 con una IC50 de 9 nM, lo que lleva a la detención en G1-S y, en última instancia, a una disminución de la proliferación celular.
|
| Ensayo de quinasa |
Ensayo de autofosforilación sin células mediante fluorometría resuelta en el tiempo
|
|
Neratinib se prepara como reservas de 10 mg/mL en DMSO y se diluye en 25 mM HEPES (pH 7,5; 0,002 ng/mL-20 μg/mL). Fragmentos COOH-terminales recombinantes purificados de HER2 (aminoácidos 676-1255) o del receptor del factor de crecimiento epidérmico (EGFR) (aminoácidos 645-1186) [diluidos en 100 mM HEPES (pH 7,5) y 50% de glicerol] se incuban con concentraciones crecientes de este compuesto en 4 mM HEPES (pH 7,5), 0,4 mM MnCl2, 20 μM de vanadato de sodio y 0,2 mM de DTT durante 15 minutos a temperatura ambiente en placas ELISA de 96 pocillos. La reacción de la quinasa se inicia mediante la adición de 40 μM de ATP y 20 mM de MgCl2 y se deja proceder durante 1 hora a temperatura ambiente. Las placas se lavan y la fosforilación se detecta utilizando anticuerpos antifosfotirosina marcados con europio (15 ng/pocillo). Después de los pasos de lavado y mejora, la señal se detecta utilizando un lector de fluorescencia Victor2 (longitud de onda de excitación 340 nm, longitud de onda de emisión 615 nm). La concentración de este químico que inhibe la fosforilación del receptor en un 50% (IC50) se calcula a partir de las curvas de inhibición.
|
|
| In vivo |
La administración oral de Neratinib inhibe significativamente el crecimiento de los xenoinjertos 3T3/neu, con una inhibición del 34%, 53%, 98% y 98% a dosis de 10, 20, 40 y 80 mg/kg/día, respectivamente. De acuerdo con la inhibición de la fosforilación de HER-2 en un 84% dentro de 1 hora de administración a 40 mg/kg/día, este compuesto inhibe el crecimiento de los xenoinjertos BT474 en un 70-82%, 67% y 93% a dosis de 5, 10 y 40 mg/kg/día, respectivamente. También es eficaz contra los xenoinjertos SK-OV-3 con una inhibición del 31% y 85% a 5 y 60 mg/kg/día, respectivamente. Este químico es menos potente contra los xenoinjertos A431 dependientes de EGFR que contra los tumores dependientes de HER-2, con una inhibición del 32% y 44% a 5 y 20 mg/kg/día, respectivamente. Muestra poca actividad contra los xenoinjertos MCF-7 y MX-1 que expresan bajos niveles de HER-2 y EGFR, con solo un 28% de inhibición a 80 mg/kg/día, lo que sugiere que tiene una actividad selectiva para las células que expresan HER-2 o EGFR.
|
Referencias |
Aplicaciones
| Métodos | Biomarcadores | Imágenes | PMID |
|---|---|---|---|
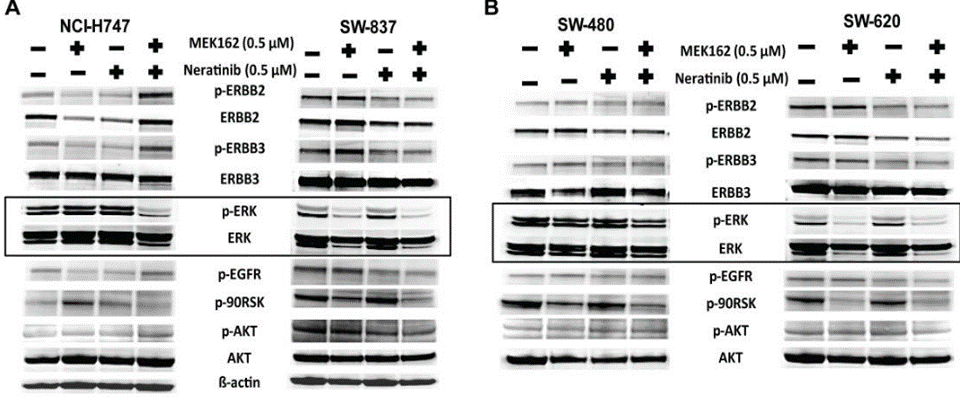
| Western blot | p-ERBB2 / ERBB2 / p-ERBB3 / ERBB3 / p-EGFR / p-90RSK pHER2 / HER2 / pAKT / AKT / pERK / ERK |
|
30118499 |
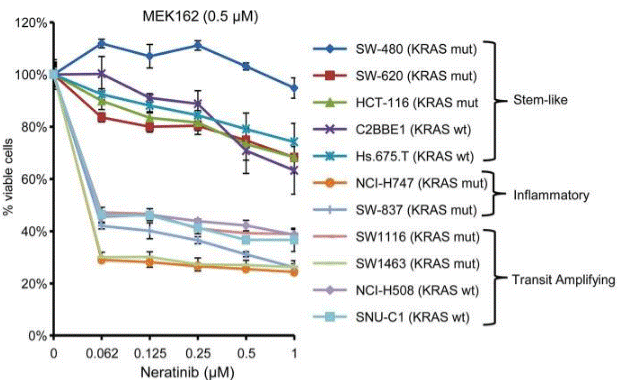
| Growth inhibition assay | Cell viability |
|
30118499 |
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT05388149 | Recruiting | Breast Cancer|HER2-positive Breast Cancer |
University Health Network Toronto |
December 6 2022 | Phase 2 |
| NCT05252988 | Recruiting | Early-stage Breast Cancer|HER2 Positive Breast Cancer|Hormone Receptor Positive |
Spanish Breast Cancer Research Group|Puma Biotechnology Inc.|Pierre Fabre Laboratories |
August 31 2022 | Phase 2 |
| NCT04856475 | Withdrawn | Breast Cancer|Brain Metastases |
Jules Bordet Institute |
November 24 2021 | Phase 2 |
| NCT04781374 | Withdrawn | Metastatic Prostate Adenocarcinoma|Castration-resistant Prostate Cancer|Prostate Cancer|Prostate Cancer Metastatic |
Beth Israel Deaconess Medical Center|Puma Biotechnology Inc.|Dana-Farber Cancer Institute |
May 21 2021 | Phase 2 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
