Datos técnicos
| Fórmula | C30H29ClN6O3 |
||||||||||
| Peso molecular | 557.04 | Número CAS | 698387-09-6 | ||||||||
| Solubilidad (25°C)* | In vitro | DMSO | 5 mg/mL (8.97 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Neratinib es un inhibidor altamente selectivo de HER2 y EGFR con IC50 de 59 nM y 92 nM en ensayos sin células; inhibe débilmente KDR y Src, sin inhibición significativa de Akt, CDK1/2/4, IKK-2, MK-2, PDK1, c-Raf y c-Met. Fase 3. | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
||||||||
| In vitro | Neratinib inhibe débilmente las tirosina quinasas KDR y Src con IC50 de 0,8 μM y 1,4 μM, respectivamente, siendo 14 y 24 veces menos activo en comparación con HER2. Este compuesto no muestra actividad contra otras serina-treonina quinasas como Akt, ciclina D1/cdk4, ciclina E/cdk2, ciclina B1/cdk1, IKK-2, MK-2, PDK1, c-Raf y Tpl-2, así como la tirosina quinasa c-Met. Inhibe selectivamente la proliferación de células 3T3 transfectadas con HER2 (3T3/neu), así como otras dos células SK-Br-3 y BT474 que sobreexpresan HER-2 con valores de IC50 de 2-3 nM, mostrando una potencia >230 veces mayor en comparación con células 3T3 no transfectadas, así como MDA-MB-435 y SW620 que son negativas para EGFR y HER2. Este químico también inhibe la proliferación de células A431 dependientes de EGFR con una IC50 de 81 nM. Reduce la autofosforilación del receptor HER2 en células BT474 con una IC50 de 5 nM, y la fosforilación de EGFR dependiente de EGF en células A431 con una IC50 de 3 nM. El bloqueo de HER-2 por este compuesto resulta en la inhibición de las vías MAPK y Akt corriente abajo con una IC50 de 2 nM, más potentemente que Trastuzumab. Inhibe la expresión de ciclina D1 y la fosforilación de la producción del gen de susceptibilidad a Rb en células BT474 con una IC50 de 9 nM, lo que lleva a la detención en G1-S y, en última instancia, a una disminución de la proliferación celular. | ||||||||
| In vivo | La administración oral de Neratinib inhibe significativamente el crecimiento de los xenoinjertos 3T3/neu, con una inhibición del 34%, 53%, 98% y 98% a dosis de 10, 20, 40 y 80 mg/kg/día, respectivamente. De acuerdo con la inhibición de la fosforilación de HER-2 en un 84% dentro de 1 hora de administración a 40 mg/kg/día, este compuesto inhibe el crecimiento de los xenoinjertos BT474 en un 70-82%, 67% y 93% a dosis de 5, 10 y 40 mg/kg/día, respectivamente. También es eficaz contra los xenoinjertos SK-OV-3 con una inhibición del 31% y 85% a 5 y 60 mg/kg/día, respectivamente. Este químico es menos potente contra los xenoinjertos A431 dependientes de EGFR que contra los tumores dependientes de HER-2, con una inhibición del 32% y 44% a 5 y 20 mg/kg/día, respectivamente. Muestra poca actividad contra los xenoinjertos MCF-7 y MX-1 que expresan bajos niveles de HER-2 y EGFR, con solo un 28% de inhibición a 80 mg/kg/día, lo que sugiere que tiene una actividad selectiva para las células que expresan HER-2 o EGFR. |
Protocolo (de referencia)
| Ensayo de quinasa:[1] |
|
|---|---|
| Ensayo celular:[1] |
|
| Estudio en animales:[1] |
|
Referencias
|
Validación de productos por parte del cliente

-
Datos de [ Cancer Discov , 2013 , 3, 224-37 ]

-
Datos de [ Cancer Discov , 2012 , 2, 458-471 ]

-
Datos de [ Cancer Discov , 2012 , 2, 458-471 ]
-
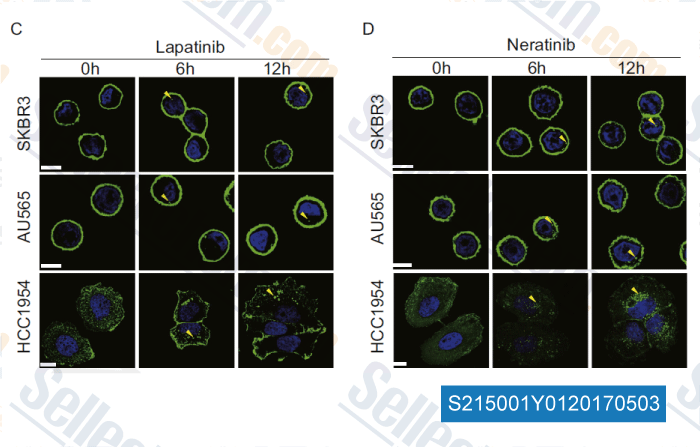
Datos de [ , , Cancer Lett, 2016, 382(2):176-185 ]
Sellecks Neratinib (HKI-272) Ha sido citado por 116 Publicaciones
| APOBEC3 mutagenesis drives therapy resistance in breast cancer [ Nat Genet, 2025, 57(6):1452-1462] | PubMed: 40379787 |
| Sevabertinib, a Reversible HER2 Inhibitor with Activity in Lung Cancer [ Cancer Discov, 2025, 10.1158/2159-8290.CD-25-0605] | PubMed: 41090369 |
| Small molecule kinase inhibitor altiratinib inhibits brain cyst forming bradyzoites of Toxoplasma gondii [ J Microbiol, 2025, 63(2):e2409001] | PubMed: 40044130 |
| KinoViz: A User-Friendly Web Application for High-Throughput Kinome Profiling Analysis and Visualization in Cancer Research [ Res Sq, 2025, rs.3.rs-6431257] | PubMed: 40630533 |
| Hotspot mutations in HER2 interfaces destabilize structure, causing breast cancer treatment failure [ Res Sq, 2025, rs.3.rs-5931887] | PubMed: 40166021 |
| Proteogenomic analysis dissects early-onset breast cancer patients with prognostic relevance [ Exp Mol Med, 2024, 56(11):2382-2394] | PubMed: 39482530 |
| Peptidylarginine deiminase 3 modulates response to neratinib in HER2 positive breast cancer [ Oncogenesis, 2024, 13(1):30] | PubMed: 39097594 |
| Patient-derived rhabdomyosarcoma cells recapitulate the genetic and transcriptomic landscapes of primary tumors [ iScience, 2024, 27(10):110862] | PubMed: 39319271 |
| Synergistic Effects of Neratinib in Combination With Palbociclib or Miransertib in Brain Cancer Cells [ World J Oncol, 2024, 15(3):492-505] | PubMed: 38751701 |
| The Combination of Afatinib With Dasatinib or Miransertib Results in Synergistic Growth Inhibition of Stomach Cancer Cells [ World J Oncol, 2024, 15(2):192-208] | PubMed: 38545471 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
