solo para uso en investigación
LXR-623 (WAY-252623) Agonista LXR
Cat. No.S8390
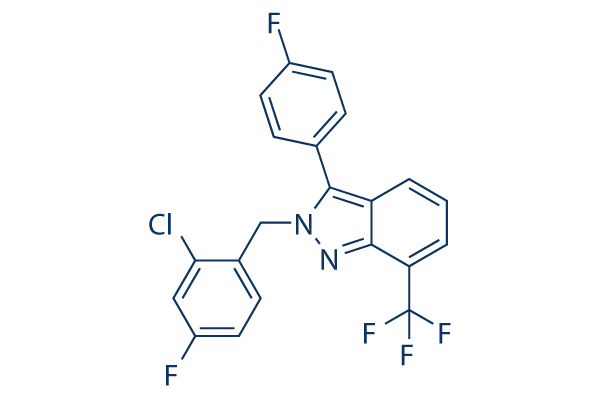
Estructura química
Peso molecular: 422.78
Control de calidad
| Dianas relacionadas | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Otros Liver X Receptor Inhibidores | GW3965 Hydrochloride T0901317 GSK2033 SR9243 Abequolixron (RGX-104) AZ876 GSK3987 Desmosterol |
Cultivo celular, tratamiento y concentración de trabajo
| Líneas celulares | Tipo de ensayo | Concentración | Tiempo de incubación | Formulación | Descripción de la actividad | PMID |
|---|---|---|---|---|---|---|
| THP1 cells | Function assay | Effect on ABCA1 gene expression in human differentiated THP1 cells, EC50=0.54 μM | ||||
| HepG2 cells | Function assay | Effect on triglyceride accumulation in human HepG2 cells, EC50=1 μM | ||||
| HuH7 cells | Function assay | Agonist activity at human LXRbeta ligand binding domain expressed in human HuH7 cells co-transfected with Gal4-DBD by transactivation assay, EC50=3.67 μM | ||||
| Haga clic para ver más datos experimentales de líneas celulares | ||||||
Información química, almacenamiento y estabilidad
| Peso molecular | 422.78 | Fórmula | C21H12ClF5N2 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 875787-07-8 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | WAY-252623 | Smiles | C1=CC2=C(N(N=C2C(=C1)C(F)(F)F)CC3=C(C=C(C=C3)F)Cl)C4=CC=C(C=C4)F | ||
Solubilidad
|
In vitro |
DMSO
: 84 mg/mL
(198.68 mM)
Ethanol : 84 mg/mL Water : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
LXR-β
24 nM
LXR-α
179 nM
|
|---|---|
| In vitro |
LXR-623 suprime la expresión de LDLR, aumenta la expresión del transportador de eflujo ABCA1 e induce una muerte celular sustancial en todas las muestras de GBM analizadas. La línea celular de cáncer de mama metastásico cerebral MDA-MB-361, que alberga la amplificación de ERBB2, también es altamente sensible a esta muerte celular dependiente del compuesto de forma concentración-dependiente. Inhibe la captación de LDL e induce el eflujo de colesterol en las células de GBM, lo que resulta en una reducción significativa del contenido de colesterol celular. La insensibilidad de las células cerebrales normales a este químico puede deberse a la dependencia de la síntesis endógena de colesterol y a una retroalimentación negativa intacta a través de la síntesis de oxisteroles endógenos.
|
| In vivo |
LXR-623 se absorbe rápidamente, alcanzando concentraciones máximas (Cmax) aproximadamente a las 2 horas. La Cmax y el área bajo la curva de concentración-tiempo aumentan de manera dosis-proporcional. La vida media de disposición terminal media es de entre 41 y 43 horas, independientemente de la dosis. En un modelo de ratón knockout para el receptor de lipoproteínas de baja densidad (LDLr) de aterosclerosis, este compuesto administrado oralmente regula al alza el ABCG5 y ABCG8 intestinales y reduce la carga del ateroma sin alterar el colesterol sérico o hepático y los triglicéridos. Muestra penetración cerebral y causa regresión tumoral en un modelo de ratón de GBM (glioblastomas), reduciendo el colesterol e induciendo la muerte celular.
|
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
