solo para uso en investigación
Flumequine Topoisomerase inhibidor
Cat. No.S3181
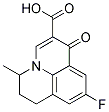
Estructura química
Peso molecular: 261.25
Control de calidad
- Citado en Nature Medicine por su máxima calidad
- COA
- NMR
- SDS
- Hoja de datos
| Dianas relacionadas | HDAC PARP ATM/ATR DNA-PK WRN DNA/RNA Synthesis PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Otros Topoisomerase Inhibidores | Camptothecin (CPT) Betulinic acid Beta-Lapachone (S)-10-Hydroxycamptothecin Amonafide Voreloxin (SNS-595) hydrochloride Ellagic acid Cu(II)-Elesclomol Hydroxy Camptothecine Rubitecan |
Información química, almacenamiento y estabilidad
| Peso molecular | 261.25 | Fórmula | C14H12FNO3 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 42835-25-6 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | R-802 | Smiles | CC1CCC2=C3N1C=C(C(=O)C3=CC(=C2)F)C(=O)O | ||
Solubilidad
|
In vitro |
DMSO
: 3 mg/mL
(11.48 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
Topo II
15 μM
|
|---|---|
| In vitro |
Flumequine inhibe la topoisomerase II eucariota, que es responsable de la reacción de ruptura del ADN de doble cadena, así como la girasa bacteriana; los efectos inhibitorios de este compuesto sobre la topoisomerasa II son altos en relación con la influencia sobre la girasa bacteriana. Tiene una concentración mínima inhibitoria (CMI) que oscila entre 0,06 μg/mL y 32 μg/mL en 12 aislados clínicos de A. salmonicida. Este producto químico exhibe altos valores de E(max) de 16 para los aislados más resistentes, lo que indica una contribución importante del eflujo al fenotipo de resistencia. Sus experimentos de acumulación confirman que los altos valores de E(max) están asociados con un nivel de acumulación mucho menor. |
| In vivo |
Flumequine (4000 ppm, dieta oral) induce daño en el ADN dependiente de la dosis en el estómago, colon y vejiga urinaria de ratones adultos a las 3 horas, pero no a las 24 horas después de su administración. Este compuesto muestra una biodisponibilidad del 44,7% después de la administración oral de alimento medicado en salmón del Atlántico. Esto resulta en volúmenes de distribución en estado estacionario de 3,5 L/kg, una vida media de eliminación (t1/2) de 22,8 horas y un área bajo la curva de concentración plasmática-tiempo (AUC) de 140 μg×horas/mL después de la administración intravenosa en salmón del Atlántico. Este químico (100 mg/L) reduce la longitud media de la raíz, hipocotilo, cotiledón y el número medio de raíces secundarias en la maleza acuática Lythrum salicaria L. El compuesto (10 mg/kg, oral) resulta en volúmenes de distribución en estado estacionario (Vss) de 2,41 L/kg (bacalao) y 2,15 L/kg (lábrido) después de la administración intravenosa. Las aclaraciones corporales totales (Cl) son 0,024 L/h.kg (bacalao) y 0,14 L/h.kg (lábrido) y las vidas medias de eliminación (t1/2 λ z) se calculan en 75 horas (bacalao) y 31 horas (lábrido) después de la administración de este compuesto (10 mg/kg, oral). Las biodisponibilidades orales (F) se calculan en 65% (bacalao) y 41% (lábrido) después de la administración oral de este químico. |
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
