solo para uso en investigación
Crizotinib hydrochloride c-Met inhibidor
Cat. No.S5190
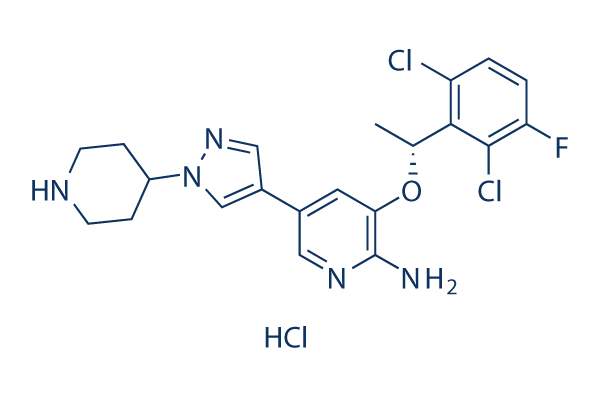
Estructura química
Peso molecular: 486.8
Control de calidad
| Dianas relacionadas | EGFR VEGFR PDGFR FGFR Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Otros c-Met Inhibidores | Tepotinib Dihexa SGX-523 PHA-665752 Foretinib SU11274 BMS-777607 JNJ-38877605 Tivantinib PF-04217903 |
Información química, almacenamiento y estabilidad
| Peso molecular | 486.8 | Fórmula | C21H23Cl3FN5O |
Almacenamiento (Desde la fecha de recepción) | 3 years -20°C powder |
|---|---|---|---|---|---|
| Nº CAS | 1415560-69-8 | -- | Almacenamiento de soluciones madre |
|
|
| Sinónimos | Xalkori, PF-02341066 hydrochloride | Smiles | Cl.CC(OC1=C(N)N=CC(=C1)C2=C[N](N=C2)C3CCNCC3)C4=C(Cl)C=CC(=C4Cl)F | ||
Solubilidad
|
In vitro |
DMSO
: 97 mg/mL
(199.26 mM)
Water : 97 mg/mL Ethanol : 97 mg/mL |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
ROS1
(Cell-free assay) <0.025 nM(Ki)
c-Met
(Cell-based assay) 11 nM
NPM-ALK
(Cell-based assay) 24 nM
|
|---|---|
| In vitro |
El PF-2341066 muestra una potencia similar contra la fosforilación de c-Met en células epiteliales de ratón mIMCD3 o caninas MDCK con un IC50 de 5 nM y 20 nM, respectivamente. El PF-2341066 muestra una actividad mejorada o similar contra las células NIH3T3 diseñadas para expresar los mutantes del sitio de unión al ATP de c-Met V1092I o H1094R o el mutante del bucle P M1250T con un IC50 de 19 nM, 2 nM y 15 nM, respectivamente, en comparación con las células NIH3T3 que expresan el receptor de tipo salvaje con un IC50 de 13 nM. En contraste, se observa un cambio marcado en la potencia de PF-2341066 contra las células diseñadas para expresar los mutantes del bucle de activación de c-Met Y1230C e Y1235D con un IC50 de 127 nM y 92 nM, respectivamente, en comparación con el receptor de tipo salvaje. El PF-2341066 también previene potentemente la fosforilación de c-Met en las células NCI-H69 y HOP92, con un IC50 de 13 nM y 16 nM, respectivamente, que expresan las variantes endógenas de c-Met R988C y T1010I, respectivamente. El PF-2341066 es >1.000 veces selectivo para las RTK VEGFR2 y PDGFRβ, >250 veces selectivo para IRK y Lck, y ~40 a 60 veces selectivo para Tie2, TrkA y TrkB, todo en comparación con c-Met. El PF-2341066 es 20 a 30 veces selectivo para las RTK RON y Axl. En contraste, el PF-2341066 muestra un IC50 casi equivalente de 24 nM contra la variante de fusión oncogénica de la ALK RTK, nucleofosmina (NPM)-anaplastic lymphoma kinase (ALK), expresada por la línea celular de linfoma anaplásico de células grandes humano (ALCL) KARPAS299. El PF-2341066 inhibe los fenotipos neoplásicos dependientes de c-Met de las células cancerosas y los fenotipos angiogénicos de las células endoteliales. El PF-2341066 suprime el crecimiento de las células de carcinoma gástrico humano GTL-16 con un IC50 de 9,7 nM. El PF-2341066 induce la apoptosis en las células GTL-16 con un IC50 de 8,4 nM. El PF-2341066 inhibe la migración e invasión de las células de carcinoma pulmonar humano NCI-H441 estimuladas por HGF con un IC50 de 11 nM y 6,1 nM, respectivamente. El PF-2341066 inhibe la dispersión de células MDCK con un IC50 de 16 nM. El PF-2341066 previene la fosforilación de c-Met estimulada por HGF, la supervivencia celular y la invasión de Matrigel con un IC50 de 11 nM, 14 nM y 35 nM, respectivamente. Además, el PF-2341066 previene la tubulogénesis de ramificación de HMVEC estimulada por suero (formación de tubos vasculares) en geles de fibrina. |
| Ensayo de quinasa |
Ensayos ELISA de fosforilación de quinasas celulares
|
|
Las células se siembran en placas de 96 pocillos en medios suplementados con 10 % de suero bovino fetal (FBS) y se transfieren a medios sin suero [con 0,04 % de albúmina de suero bovino (BSA)] después de 24 h. En experimentos que investigan la fosforilación de RTK dependiente de ligando, se añaden los factores de crecimiento correspondientes durante un máximo de 20 min. Después de la incubación de las células con PF-2341066 durante 1 h y/o ligandos apropiados durante los tiempos designados, las células se lavan una vez con HBSS suplementado con 1 mM de Na3VO4, y se generan lisados de proteínas a partir de las células. Posteriormente, la fosforilación de Protein Tyrosine Kinase seleccionadas se evalúa mediante un método ELISA tipo sándwich utilizando anticuerpos de captura específicos utilizados para recubrir placas de 96 pocillos y un anticuerpo de detección específico para residuos de tirosina fosforilados. Las placas recubiertas con anticuerpos se (a) incuban en presencia de lisados de proteínas a 4 °C durante la noche; (b) se lavan siete veces en 1 % de Tween 20 en PBS; (c) se incuban en un anticuerpo anti-fosfotirosina total (PY-20) conjugado con peroxidasa de rábano picante (1:500) durante 30 min; (d) se lavan siete veces de nuevo; (e) se incuban en sustrato de peroxidasa de 3,3′,5,5′-tetrametilbencidina para iniciar una reacción colorimétrica que se detiene añadiendo 0,09 N H2SO4; y (f) se mide la absorbancia a 450 nm utilizando un espectrofotómetro.
|
|
| In vivo |
En el modelo GTL-16, el PF-2341066 revela la capacidad de causar una marcada regresión de grandes tumores establecidos (>600 mm3) tanto en las cohortes de tratamiento de 50 mg/kg/día como de 75 mg/kg/día, con una disminución del 60 % en el volumen tumoral medio durante el programa de administración de 43 días. En otro estudio, el PF-2341066 muestra la capacidad de inhibir completamente el crecimiento tumoral de GTL-16 durante >3 meses, con solo 1 de 12 ratones mostrando un aumento significativo en el crecimiento tumoral durante el programa de tratamiento de 3 meses a 50 mg/kg/día. En el modelo de CPNM NCI-H441, se observa una disminución del 43 % en el volumen tumoral medio a 50 mg/kg/día durante el ciclo de administración de PF-2341066 de 38 días. En el modelo de CCR Caki-1, se observa una disminución del 53 % en el volumen tumoral medio asociada a una disminución del volumen de cada tumor en al menos un 30 % a 50 mg/kg/día durante el ciclo de administración de PF-2341066 de 33 días. El PF-2341066 también revela una prevención casi completa del crecimiento de tumores establecidos a 50 mg/kg/día en los modelos de xenoinjertos de glioblastoma U87MG o carcinoma prostático PC-3, con un 97 % o 84 % de inhibición en el último día del estudio, respectivamente. En contraste, el PF-2341066 administrado por vía oral a 50 mg/kg/día no inhibe significativamente el crecimiento tumoral en el modelo de carcinoma de mama MDA-MB-231, o el modelo de carcinoma de colon DLD-1. Se observa una reducción significativa dosis-dependiente de las células endoteliales CD31-positivas a 12,5 mg/kg/día, 25 mg/kg/día y 50 mg/kg/día en tumores GTL-16, lo que indica que la inhibición de la MVD muestra una correlación dosis-dependiente con la eficacia antitumoral. El PF-2341066 muestra una reducción significativa dosis-dependiente de los niveles plasmáticos humanos de VEGFA e IL-8 en los modelos GTL-16 y U87MG. Se observa una marcada inhibición de los niveles fosforilados de c-Met, Akt, Erk, PLCλ1 y STAT5 en tumores GTL-16 después de la administración oral de PF-2341066.
|
Referencias |
|
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT06062810 | Not yet recruiting | Non-Small Cell Lung Cancer |
Han Xu M.D. Ph.D. FAPCR Sponsor-Investigator IRB Chair|Medicine Invention Design Inc |
March 28 2024 | Phase 2|Phase 3 |
| NCT04148066 | Completed | Carcinoma Non-Small-Cell Lung |
The Netherlands Cancer Institute|Roche Pharma AG |
July 17 2019 | Not Applicable |
| NCT03947385 | Recruiting | Metastatic Uveal Melanoma|Cutaneous Melanoma|Colorectal Cancer|Other Solid Tumors |
IDEAYA Biosciences |
June 28 2019 | Phase 1|Phase 2 |
| NCT03672643 | Terminated | ALK or ROS1-positive NSCLC |
Pfizer |
January 28 2019 | Phase 4 |
| NCT03439215 | Unknown status | Carcinoma Non-Small-Cell Lung |
Fondazione Ricerca Traslazionale|Clinical research technology Srl |
June 13 2017 | Phase 2 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
