solo para uso en investigación
SGX-523 c-Met inhibidor
Cat. No.S1112
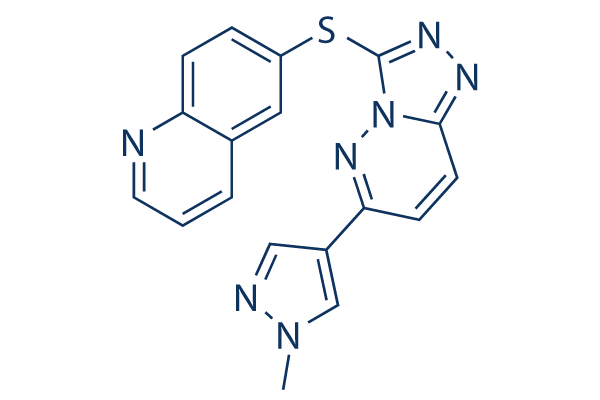
Estructura química
Peso molecular: 359.41
Control de calidad
| Dianas relacionadas | EGFR VEGFR PDGFR FGFR Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Otros c-Met Inhibidores | Tepotinib Dihexa PHA-665752 Foretinib SU11274 BMS-777607 JNJ-38877605 Tivantinib PF-04217903 Savolitinib (AZD6094) |
Información química, almacenamiento y estabilidad
| Peso molecular | 359.41 | Fórmula | C18H13N7S |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 1022150-57-7 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | N/A | Smiles | CN1C=C(C=N1)C2=NN3C(=NN=C3SC4=CC5=C(C=C4)N=CC=C5)C=C2 | ||
Solubilidad
|
In vitro |
DMSO
: 2 mg/mL
(5.56 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
c-Met
(Cell-free assay) 4 nM
|
|---|---|
| In vitro |
SGX-523 pertenece a la clase de inhibidores de Protein Tyrosine Kinase c-Met/receptor del factor de crecimiento de hepatocitos (HGFR). Este compuesto estabiliza MET en una conformación inactiva única que es inaccesible a otras proteínas quinasas, lo que sugiere una explicación para su selectividad. Inhibe potentemente el dominio catalítico de MET purificado, pero no la Protein Tyrosine Kinase RON, estrechamente relacionada. Este químico indica una inhibición competitiva de ATP con una mayor afinidad aparente por la forma menos activa y no fosforilada de MET [MET-KD(0P), con una Ki de 2,7 nM] frente a la fosfoenzima más activa [MET-KD(3P), con una Ki de 23 nM], un fenómeno consistente con la unión preferencial a una conformación enzimática inactiva. Inhibe la señalización mediada por MET, la proliferación celular y la migración celular a concentraciones nanomolares, pero no tuvo efecto sobre la señalización dependiente de otras proteínas quinasas, incluida la RON estrechamente relacionada, incluso a concentraciones micromolares.
|
| Ensayo de quinasa |
Ensayos de quinasa
|
|
Las constantes de velocidad iniciales se miden a 21 °C en presencia de 100 mM HEPES (pH 7,5), 0,3 mg/mL de sustrato peptídico poli(Glu-Tyr), 10 mM MgCl2, 1 mg/mL de albúmina sérica bovina, 5 % de DMSO, 20 nM MET-KD y varias concentraciones de ATP y SGX523. Los volúmenes de reacción totales (20 μL) se inactivan con 20 μL de tampón de detección Kinase-Glo. La luminiscencia se detecta en un luminómetro de lectura de placas y los resultados se analizan mediante regresión no lineal.
|
|
| In vivo |
El SGX523 retrasa significativamente el crecimiento de tumores GTL16 preestablecidos cuando se administra por vía oral en dosis de ≥10 mg/kg dos veces al día. Este compuesto inhibe potentemente el crecimiento tumoral de U87MG; a 30 mg/kg administrados dos veces al día, provoca una clara regresión de los tumores U87MG. Este producto químico, administrado dos veces al día a 30 mg/kg, también retrasa el crecimiento de los tumores H441 con una reducción concomitante en los niveles de autofosforilación de MET tumoral. Su inhibición de MET in vivo se asocia con la inhibición dependiente de la dosis del crecimiento de xenoinjertos tumorales derivados de glioblastoma humano, cánceres de pulmón y gástricos, lo que confirma la dependencia de estos tumores de la actividad catalítica de MET.
|
Referencias |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
