solo para uso en investigación
AG-490 EGFR inhibidor
Cat. No.S1143
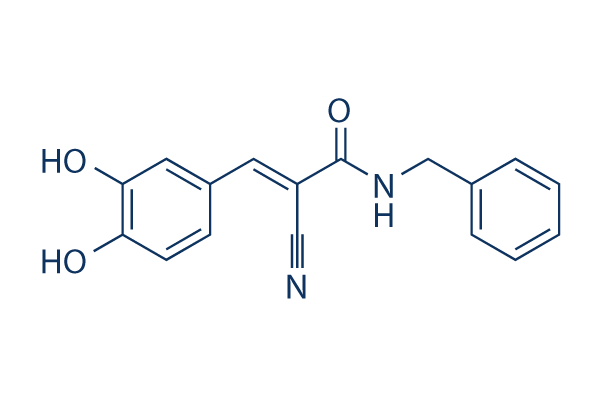
Estructura química
Peso molecular: 294.30
Control de calidad
| Dianas relacionadas | VEGFR PDGFR FGFR c-Met Src MEK CSF-1R FLT3 HER2 c-Kit |
|---|---|
| Otros EGFR Inhibidores | Lazertinib (YH25448) Icotinib Hydrochloride Sunvozertinib AG-1478 Canertinib (CI-1033) WZ4002 Rociletinib (CO-1686) Poziotinib (NOV120101, HM781-36B) Genistein Allitinib tosylate |
Cultivo celular, tratamiento y concentración de trabajo
| Líneas celulares | Tipo de ensayo | Concentración | Tiempo de incubación | Formulación | Descripción de la actividad | PMID |
|---|---|---|---|---|---|---|
| BC3 | Function Assay | 100 µM | 24 h | mediates PEL cell apoptosis | ||
| BCBL1 | Function Assay | 100 µM | 24 h | mediates PEL cell apoptosis | ||
| BC3 | Function Assay | 100 µM | 24 h | mediates de-phosphorylation of STAT3 correlated with HSP70 and HSF1 reduction | ||
| BCBL1 | Function Assay | 100 µM | 24 h | mediates de-phosphorylation of STAT3 correlated with HSP70 and HSF2 reduction | ||
| BC3 | Function Assay | 100 µM | 24 h | induces a complete autophagic flux | ||
| BCBL1 | Function Assay | 100 µM | 24 h | induces a complete autophagic flux | ||
| SK-MEL-28 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| MeWo | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| SK-MEL-5 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| SK-MEL-2 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| B16-F0 | Function Assay | 50/100 µM | 48 h | DMSO | reduces anoikis resistance | |
| TRPM2/HEK | Function Assay | 0.1–25 µM | 15 min | DMSO | reduces H2O2-induced Ca2+increase in a concentration-dependent manner, and the IC50 value was 1.7 µM | |
| U937 | Function Assay | 0.1–25 µM | 15 min | DMSO | reduces H2O2-induced Ca2+increase in a concentration-dependent manner, and the IC50 value was 0.4 µM | |
| TRPM2/HEK | Function Assay | 10 µM | 40 min | DMSO | reduces TRPM2 activation even at high concentrations of H2O2 | |
| GL37 | Cell Viability Assay | 0-10 µM | 48 h | suppresses La expression | ||
| NRK-52E | Function Assay | 1 µM | 10 min | blocks the stimulatory effect of Ang II on Pax-2 expression | ||
| NRK-52E | Function Assay | 1 µM | 10 min | blocks Ang II induced CD24 expression | ||
| HSC | Function Assay | 20 μM | 1 h | abrogates the differential effects of leptin or AGEs | ||
| EJ | Growth Inhibition Assay | 50/80 μM | 24/48/72 h | inhibits cell growth in both time and dose dependent manner | ||
| EJ | Growth Inhibition Assay | 50/80 μM | 48 h | causes S-phase arrest | ||
| EJ | Function Assay | 50/80 μM | 48 h | downregulates c-Myc, cyclinD1, survivin and VEGF expressions | ||
| HepG2 | Function Assay | 50-500 μM | 60 min | inhibits the IL-6-induced phosphorylation of STAT1 (Tyr705) and STAT3 (Tyr705) in a dose-dependent manner | ||
| SGC7901 | Cell Viability Assay | 0-100 μM | 24/48/72 h | causes a significant reduction in cell viability dose-dependently but not time-dependently | ||
| AGS | Cell Viability Assay | 0-100 μM | 24/48/72 h | causes a significant reduction in cell viability dose-dependently but not time-dependently | ||
| SGC7901 | Function Assay | 50 μM | 24/48/72 h | the levels of pJAK2 began to decline at 24 hr, and rebounded at 72 hr | ||
| AGS | Function Assay | 50 μM | 24/48/72 h | the levels of pJAK2 began to decline at 24 hr, and rebounded at 72 hr | ||
| SGC7901 | Function Assay | 50 μM | 24/48/72 h | the cytoplasmic localization of pJAK2 (JAK2 phosphorylated at residues Tyr1007 and Tyr1008) decreased after AG490 treatment for 24 and 48 hr, but started to rebound at 72 hr | ||
| AGS | Function Assay | 50 μM | 24/48/72 h | the cytoplasmic localization of pJAK2 (JAK2 phosphorylated at residues Tyr1007 and Tyr1008) decreased after AG490 treatment for 24 and 48 hr, but started to rebound at 72 hr | ||
| MC3T3-E1 | Function Assay | 50 μM | 4 h | inhibits HSE-induced BMP7 and GHR protein expression | ||
| 7TD1-DXM | Growth Inhibition Assay | 10 μM | 72 h | DMSO | inhibits cell growth | |
| 7TD1-WD-90 | Growth Inhibition Assay | 10 μM | 72 h | DMSO | inhibits cell growth | |
| 7TD1-DXM | Apoptosis Assay | 50 μM | 48 h | DMSO | induces apoptosis | |
| 7TD1-WD-90 | Apoptosis Assay | 50 μM | 48 h | DMSO | induces apoptosis | |
| 7TD1-WD-90 | Function Assay | 50 μM | 6 h | DMSO | significantly inhibits the phosphorylation of JAK2 and phosphorylation of STAT3 | |
| HepG2 | Function Assay | 100 μM | 12/24 h | inhibits STAT3 tyrosine phosphorylation | ||
| RAW264.7 | Function Assay | 50 μM | 24/48 h | suppresses RANKL-induced osteoclastogenesis | ||
| RAW264.7 | Growth Inhibition Assay | 0-50 μM | 48 h | inhibits cell growth dose-dependently | ||
| RAW264.7 | Growth Inhibition Assay | 0-50 μM | 48 h | causes an arrest of RAW264.7 cells at the G0/G1 phase of the cell cycle | ||
| RAW264.7 | Function Assay | 50 μM | 24/48 h | inhibits RANKL-induced NFATc1 expression and phosphorylation of Ser727STAT3 | ||
| A549 | Function Assay | 20/40 μM | 20 h | 20 μM AG490 suppresses the radiation-induced invasion of A549 cells | ||
| A549 | Function Assay | 10/20/40 μM | 24 h | suppresses the radiation-induced elevation of VEGF | ||
| HUVECs | Cell Viability Assay | 20 µM | 4 h | attenuates H2O2-induced cell shrinkage and improved the attachment rate of the cells | ||
| HUVECs | Apoptosis Assay | 20 µM | 4 h | significantly decreases the cell apoptotic index | ||
| BV-2 | Function Assay | 20 µM | 16 h | inhibits LPS-induced STAT1 phosphorylation with almost completely diminished iNOS expression | ||
| NRK-52E | Function Assay | 5 μM | 30 min | attenuates Ang-(1–7)-inhibited TGF-β1 mRNA at 16 h | ||
| SW620 | Function Assay | 20 µM | 1/6 h | inhibits p-STAT3 activation | ||
| RPE | Function Assay | 30 µM | 3 h | inhibits the induction of p-STAT3 expression | ||
| SW1116 | Function Assay | 100 µM | 24/48/72 h | decreases the expression of JAK2 and pJAK2 time-dependently | ||
| HT29 | Function Assay | 100 µM | 24/48/72 h | decreases the expression of JAK2 and pJAK2 time-dependently | ||
| SW1116 | Function Assay | 100 µM | 24/48/72 h | decreases the pSTAT3 levels in a time-dependent manner | ||
| HT29 | Function Assay | 100 µM | 24/48/72 h | decreases the pSTAT3 levels in a time-dependent manner | ||
| ARPE-19 | Function Assay | 5 μM | 30 min | inhibits JAK2 phosphorilation | ||
| HSC-T6 | Apoptosis Assay | 10 μM | 2 h | inhibits the apoptosis of HSC-T6 cells induced by CDE | ||
| HSC-T6 | Function Assay | 10 μM | 2 h | inhibits the expressions of pY-STAT1 and Bad induced by CDE | ||
| Hep-2 | Growth Inhibition Assay | 25-100 μM | 24/48/72 h | inhibits cell growth in both time and dose dependent manner | ||
| Hep-2 | Apoptosis Assay | 50 μM | 24/48/72 h | induces cell apoptosis time dependently | ||
| Hep-2 | Function Assay | 50 μM | 24/48/72 h | inhibits G1 to S cell cycle transition and induces G1 cell cycle arrest | ||
| Hep-2 | Function Assay | 50 μM | 24/48/72 h | downregulates the STAT3, p-STAT3 and survivin protein levels | ||
| KF8 | Function Assay | 10 μM | 1 h | DMSO | inhibits IL-33-induced NF-κB activation | |
| KF8 | Function Assay | 10 μM | 1 h | DMSO | inhibits IL-33-induced IκBα degradation and NF-κB activation | |
| HEL | Function Assay | 100 μM | 12-72 h | inhibits the level of p-JAK2, JAK2 | ||
| HEL | Growth Inhibition Assay | 100 μM | 0-5 d | reduces growth of JAK2V617F-expressing HEL cells | ||
| A-172 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-18 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-54 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-256 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| MZ-304 | Function Assay | 50/100 μM | 48 h | reduces the levels of constitutively activated STAT3 in a time-dependent and dose-dependent fashion | ||
| A-172 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-18 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-54 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-256 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| MZ-304 | Growth Inhibition Assay | 50/100 μM | 48 h | leads to a statistically significant reduction of cell proliferation over a time period of 48 h | ||
| A-172 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-18 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-54 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-256 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| MZ-304 | Function Assay | 50/100 μM | 48 h | inhibits migration | ||
| A-172 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-18 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-54 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-256 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| MZ-304 | Function Assay | 100 μM | 48 h | inhibits invasion | ||
| A-172 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-18 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-54 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-256 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| MZ-304 | Function Assay | 50/100 μM | 48 h | reduces transcription of MMP genes and reduces enzymatic activity of MMPs | ||
| SW1990 | Growth Inhibition Assay | 20 μM | 24/48/72 h | inhibits cell growth time dependently | ||
| SW1990 | Function Assay | 20 μM | 24 h | decreases the expression of MMP-2 and VEGF mRNAs | ||
| SW1990 | Function Assay | 20 μM | 24 h | decreases the intensity of p-Stat3 expression | ||
| SW1990 | Invasion Assay | 20 μM | 24 h | reduces invasion of SW1990 cells | ||
| THP1 | Function Assay | 10 uM | 30 min | inhibits STAT3 tyrosine phosphorylation by over 60% | ||
| BMMC | Function Assay | 0-10 μM | 15 min | inhibits LTC4 release in a dose-dependent fashion with near complete inhibition at concentrations ⩾10 μM | ||
| A549 | Function Assay | 15 μm | 1 h | inhibits the phosphorylation of STAT1 on tyrosine 701 was detected 15 min after SPE B treatment | ||
| OVCAR-3 | Function Assay | 10 uM | 1 h | inhibits LPA-induced STAT3 phosphorylation | ||
| PA-1 | Function Assay | 10 uM | 1 h | inhibits LPA-induced STAT3 phosphorylation | ||
| OVCAR-3 | Function Assay | 10 uM | 1 h | inhibits LPA-induced ovarian cancer cell motility | ||
| PA-1 | Function Assay | 10 uM | 1 h | inhibits LPA-induced ovarian cancer cell motility | ||
| Jurkat | Growth Inhibition Assay | 50 μM | 24/48/72 h | enhances TRAIL-induces cell growth inhibition | ||
| SUPT1 | Growth Inhibition Assay | 50 μM | 24/48/72 h | enhances TRAIL-induces cell growth inhibition | ||
| Jurkat | Apoptosis Assay | 50 μM | 24/48 h | enhances TRAIL-induces cell apoptosis | ||
| SUPT1 | Apoptosis Assay | 50 μM | 24/48 h | enhances TRAIL-induces cell apoptosis | ||
| Haga clic para ver más datos experimentales de líneas celulares | ||||||
Información química, almacenamiento y estabilidad
| Peso molecular | 294.30 | Fórmula | C17H14N2O3 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 133550-30-8 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | Tyrphostin B42, Zinc02557947 | Smiles | C1=CC=C(C=C1)CNC(=O)C(=CC2=CC(=C(C=C2)O)O)C#N | ||
Solubilidad
|
In vitro |
DMSO
: 58 mg/mL
(197.07 mM)
Ethanol : 9 mg/mL Water : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
JAK2 (V617F)
EGFR
(Cell-free assay) 0.1 μM
|
|---|---|
| In vitro |
AG-490 inhibe la proliferación celular impulsada por HER-2 con una IC50 de 3,5 μM. Correspondiendo a la inhibición específica dependiente de la dosis de JAK2 activado constitutivamente en células de leucemia linfoblástica aguda (LLA) pre-B, este compuesto (5 μM) bloquea casi completamente el crecimiento de todas las células LLA al inducir la muerte celular programada, sin efectos deletéreos sobre la hematopoyesis normal. Este químico no inhibe las actividades de Lck, Lyn, Btk, Syk y Src. Él (60-100 μM) bloquea la activación constitutiva de Stat3sm e inhibe el crecimiento espontáneo, así como el inducido por interleucina 2, de las células tumorales de micosis fungoide (MF) con valores de IC50 de 75 μM y 20 μM, respectivamente. Este compuesto inhibe potentemente el crecimiento de células T humanas mediado por IL-2 con una IC50 de 25 μM al bloquear las actividades de JAK3 y STAT5a/b. Inhibe significativamente la activación constitutiva de Stat3 en células MOPC, MPC11 y S194, lo que lleva a una apoptosis dramática dependiente de la dosis. Este químico (100 μM) inhibe la fosforilación de Akt, inhibe la activación del factor nuclear-κB y causa la activación de GSK-3β, lo que lleva a la reducción de c-Myc. Él (50 μM) puede inducir la apoptosis de células BaF3 que expresan los mutantes T315I y E255K de Bcr-Abl. Este compuesto a 30 μM inhibe no solo la fosforilación de JAK2 de tipo salvaje inducida por Epo, sino también la fosforilación constitutiva del mutante JAK2 V617F. También inhibe potentemente el crecimiento celular independiente de citocinas inducido por el mutante JAK2 V617F en células BaF3. |
| Ensayo de quinasa |
Autofosforilación de la quinasa in vitro
|
|
AG-490 se disuelve en DMSO 10%-H2O-etanol 45%. Los extractos de membrana crudos (0,125 μg/mL) se preactivan con EGF (20 nM) en tampón HEPES 50 mM, pH 7,6, y NaCl 125 mM, durante 15 minutos a 4 °C. La actividad de autofosforilación de la quinasa EGFR o ErbB2 se ensaya a 4 °C durante 30 segundos en placas de 96 pocillos en forma de V. Se añaden extractos de membrana (8 μL) a cada pocillo que contiene la mezcla de reacción (12 μL, HEPES 50 mM, pH 7,4, NaCl 125 mM, M8Ac2 12 mM, MnCl2 2 mM, NaVO3 1 mM, ATP 1 μM y [γ-32P]ATP 1 μCi, concentraciones finales) y concentraciones crecientes de este compuesto (4 μL). Después de la terminación por adición de tampón de muestra caliente, las muestras se corren en un minigel de electroforesis en gel de poliacrilamida SDS al 6 %, los geles se secan y se realiza una autorradiografía durante el período de tiempo de exposición lineal. Las bandas del receptor se escanean densitrométricamente y los resultados se analizan mediante el programa Ez-Fit. Para el análisis de la autofosforilación de JAK2, JAK2 se inmunoprecipita utilizando un anticuerpo anti-JAK2 a partir de lisados de células G2 pretratadas durante 16 horas con concentraciones crecientes de este químico (0-50 μM). Luego, los inmunocomplejos se inmunotransfieren con un anticuerpo anti-fosfotirosina. Se demuestra una inhibición dependiente de la dosis de la actividad quinasa in vitro mediante la evaluación de la autofosforilación de JAK2.
|
|
| In vivo |
La administración de AG-490 reduce drásticamente el número de células CD45+ y HLA-DR+ del 48 % y 46 % en la médula ósea de ratones no tratados, así como del 38 % y 22 % en el bazo de ratones no tratados a niveles indetectables. La administración in vivo de este compuesto causa apoptosis de las células tumorales de mieloma murino, pero no inhibe la activación de macrófagos mediada por IL-12 ni la producción de IFN-γ por los linfocitos. De acuerdo con el bloqueo in vitro de la actividad del mutante JAK2 V617F, el tratamiento con este químico a 0,5 mg/día durante 10 días inhibe eficazmente la tumorigénesis y la invasión de células tumorales inducidas por el mutante JAK2 V617F en ratones nude. La terapia combinada con este agente e IL-12 induce mayores efectos antitumorales que cualquiera de los agentes solos en un modelo de tumor de mieloma murino. |
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
Preguntas frecuentes
Pregunta 1:
I would like to know whether it (S1143) goes to CNS through BBB, or not?
Respuesta:
It can go through the BBB, as shown in this reference: http://bloodjournal.hematologylibrary.org/content/111/4/2062.full.html.
