solo para uso en investigación
Pitavastatin (NK-104) Calcium HMG-CoA Reductase inhibidor
Cat. No.S1759
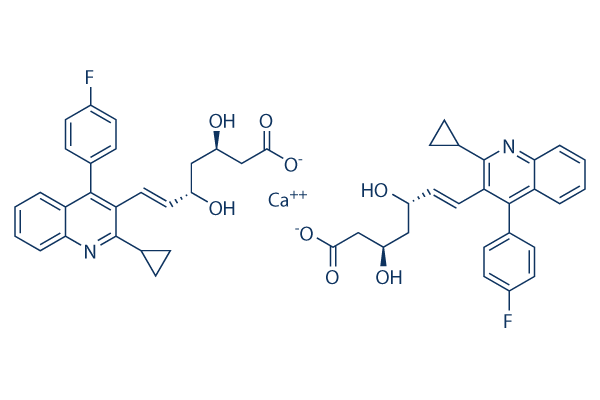
Estructura química
Peso molecular: 880.98
Control de calidad
| Dianas relacionadas | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Otros HMG-CoA Reductase Inhibidores | Mevastatin SR-12813 Clinofibrate Dihydrolanosterol 7-ketocholesterol Cerivastatin sodium |
Cultivo celular, tratamiento y concentración de trabajo
| Líneas celulares | Tipo de ensayo | Concentración | Tiempo de incubación | Formulación | Descripción de la actividad | PMID |
|---|---|---|---|---|---|---|
| HEK293 | Function assay | Drug uptake in HEK293 cells expressing OATP1B1 (unknown origin) assessed as OATP1B1-mediated drug transport, Km = 4.8 μM. | 22587986 | |||
| hepatocytes | Function assay | 0.1 to 10 uM | up to 90 mins | Drug metabolism in Sprague-Dawley rat hepatocytes assessed per 10'6 cells at 0.1 to 10 uM up to 90 mins by media-loss method, Km = 13 μM. | 22593038 | |
| Neuro2a | Function assay | 1 uM | Inhibition of delta 8-7 isomerase in mouse Neuro2a cells assessed as decrease in 7-DHC levels at 1 uM by LC-MS/GC-MS analysis | 26789657 | ||
| Neuro2a | Function assay | 1 uM | Inhibition of DR24 in mouse Neuro2a cells assessed as decrease in 7-DHC levels at 1 uM by LC-MS/GC-MS analysis | 26789657 | ||
| Neuro2a | Function assay | 1 uM | Inhibition of HMGCoA reductase in Dhcr7-deficient mouse Neuro2a cells assessed as decrease in 7-DHC levels at 1 uM by LC-MS/GC-MS analysis | 26789657 | ||
| MCF-7 | Function assay | 10 uM | 24 hrs | Antagonist activity at Myc-tagged RXRalpha (unknown origin) expressed in human MCF-7 cells assessed as inhibition of 9-cis-RA induced receptor transactivation at 10 uM after 24 hrs by luciferase reporter gene assay | 28089347 | |
| MCF-7 | Function assay | 1 uM | 24 hrs | Antagonist activity at Myc-tagged RXRalpha (unknown origin) expressed in human MCF-7 cells assessed as inhibition of 9-cis-RA induced receptor transactivation at 1 uM after 24 hrs by luciferase reporter gene assay | 28089347 | |
| Haga clic para ver más datos experimentales de líneas celulares | ||||||
Información química, almacenamiento y estabilidad
| Peso molecular | 880.98 | Fórmula | C50H46CaF2N2O8 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 147526-32-7 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | NK-104 calcium | Smiles | C1CC1C2=NC3=CC=CC=C3C(=C2C=CC(CC(CC(=O)[O-])O)O)C4=CC=C(C=C4)F.C1CC1C2=NC3=CC=CC=C3C(=C2C=CC(CC(CC(=O)[O-])O)O)C4=CC=C(C=C4)F.[Ca+2] | ||
Solubilidad
|
In vitro |
DMSO
: 100 mg/mL
(113.5 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
cholesterol esters
HMG-CoA reductase
|
|---|---|
| In vitro |
La pitavastatina reduce significativamente los niveles intracelulares y la síntesis de ésteres de colesterol. Se ha demostrado que la pitavastatina mejora la expresión del receptor de LDL in vitro, así como la cantidad de unión de LDL al receptor de LDL. La pitavastatina también exhibe una inducción más potente de la expresión de ARNm del receptor de LDL en comparación con la simvastatina y la atorvastatina. La pitavastatina tiene muchos efectos pleiotrópicos in vitro e in vivo, incluyendo la prevención de la progresión de la aterosclerosis a través de la inhibición de la síntesis de tromboxano, la inhibición de la migración/proliferación de células de músculo liso vascular inducida por la angiotensina II y la estabilización de la placa aterosclerótica.
La pitavastatina es capaz de activar el PPARα e inducir el apoA-I del HDL a través de la inhibición de la vía de señalización Rho.
El tratamiento con pitavastatina (1 μM) durante 48 h es capaz de aumentar la expresión de la proteína morfogenética ósea-2 BMP-2 (2,5 veces) y la osteocalcina (10 veces) mediante la inhibición de la Rho-quinasa asociada en osteoblastos humanos. La pitavastatina inhibe el crecimiento y la formación de colonias de células de cáncer de hígado Huh-7 y células SMMC7721. Induce la detención de las células de cáncer de hígado en la fase G1. Se observa una mayor proporción de células sub-G1 después del tratamiento con pitavastatina. La pitavastatina promueve la escisión de la caspasa-9 y la caspasa-3 en células de cáncer de hígado. La pitavastatina podría regular el NF-κB y la antiinflamación en células de carcinoma hepatocelular. La pitavastatina podría inducir la muerte celular autofágica en células de glioma y promover la sensibilidad de las células a la radioterapia. También podría inhibir la proliferación celular e inducir la apoptosis celular en células de colangiocarcinoma.
|
| In vivo |
La pitavastatina disminuye el crecimiento tumoral y mejora la supervivencia de los ratones portadores de tumores. La pitavastatina ejerce un efecto protector sobre la miocardiopatía dilatada, posiblemente mediante la regulación a la baja del RAS circulante y local, seguida de la inhibición de la fosforilación de PKCb2, y consecuentemente promoviendo la fosforilación de PLB, así como la actividad y las expresiones de SERCA2a y RyR2, con lo que se preserva la función cardíaca en el desarrollo de la DCM.
|
Referencias |
|
Aplicaciones
| Métodos | Biomarcadores | Imágenes | PMID |
|---|---|---|---|
| Western blot | Nrf2 / NQO1 / HO-1 Flt1 / Flk1 VEGF / p-Akt / AKT / Jagged-1 / c-Notch1 / Notch-1 / Hes-1 |
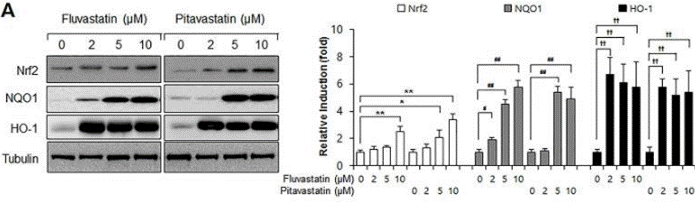
|
28542559 |
| Growth inhibition assay | Cell number |
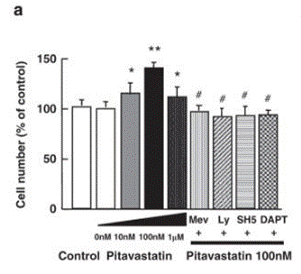
|
21301413 |
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT05977738 | Recruiting | Glioblastoma Multiforme Adult|Recurrent Glioblastoma |
C.Dirven|Erasmus Medical Center |
January 18 2024 | Early Phase 1 |
| NCT04643093 | Completed | Primary Hypercholesterolemia|Mixed Dyslipidemias |
Orient Pharma Co. Ltd. |
August 1 2020 | Phase 3 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
Preguntas frecuentes
Pregunta 1:
How to prepare the solution of it for in vivo use?
Respuesta:
You could use the formulation: 5% DMSO +40%PEG 300+5%Tween80+ddH2O for i.p., at a working concentration of 12.5mg/ml, stable for no longer than 40min.
