solo para uso en investigación
Cilengitide trifluoroacetate Integrin inhibidor
Cat. No.S7077

Estructura química
Peso molecular: 702.68
Control de calidad
| Dianas relacionadas | Akt Wnt/beta-catenin PKC HSP ROCK Microtubule Associated Bcr-Abl Actin FAK Kinesin |
|---|---|
| Otros Integrin Inhibidores | SB273005 Cilengitide (EMD 121974) RGD peptide (Arg-Gly-Asp) ATN-161 Cyclo(-RGDfK) TFA Cyclo(RGDyK) TFA Leukadherin-1 A-205804 Pyrintegrin RGD peptide (GRGDNP) |
Cultivo celular, tratamiento y concentración de trabajo
| Líneas celulares | Tipo de ensayo | Concentración | Tiempo de incubación | Formulación | Descripción de la actividad | PMID |
|---|---|---|---|---|---|---|
| G28 | Function Assay | 50 μg/ml | 30/60/120 min | inhibits phosphorylation of FAK, Src and Akt | 19114005 | |
| HMEC-1 | Function Assay | 20/40/60 μg/ml | inhibits FAK and Src | 19114005 | ||
| G44 | Apoptosis Assay | 1/5/50 μg/ml | 24 h | induces apoptosis | 19114005 | |
| G28 | Apoptosis Assay | 1/5/50 μg/ml | 24 h | induces apoptosis | 19114005 | |
| G44 | Proliferation Assay | 1/5/50 μg/ml | 24/48/72 h | inhibits proliferation in a dose dependent manner | 19114005 | |
| G28 | Proliferation Assay | 1/5/50 μg/ml | 24/48/72 h | inhibits proliferation in a dose dependent manner | 19114005 | |
| HMEC-1 | Apoptosis Assay | 1/5/50 μg/ml | 24 h | induces apoptosis | 19114005 | |
| HMEC-1 | Proliferation Assay | 1/5/50 μg/ml | 24/48/72 h | inhibits proliferation in a dose dependent manner | 19114005 | |
| HMEC-1 | Function Assay | 1/5/50 μg/ml | 24 h | induces a dose dependent detachment | 19114005 | |
| LNT-229 | Function Assay | 0.1/1/10 μM | 24 h | impairs the adhesion of cells to vitronectin in a dose dependent manner | 19221171 | |
| T98G | Function Assay | 0.1/1/10 μM | 24 h | impairs the adhesion of cells to vitronectin in a dose dependent manner | 19221171 | |
| LN-18 | Function Assay | 0.1/1/10 μM | 24 h | impairs the adhesion of cells to vitronectin in a dose dependent manner | 19221171 | |
| LN-308 | Function Assay | 0.1/1/10 μM | 24 h | impairs the adhesion of cells to vitronectin in a dose dependent manner | 19221171 | |
| U87MG | Function Assay | 0.1/1/10 μM | 24 h | impairs the adhesion of cells to vitronectin in a dose dependent manner | 19221171 | |
| U87 | Function Assay | 0-25 μg/mL | 12 h | induces autophagy dose dependently | 21788343 | |
| U251 | Function Assay | 0-25 μg/mL | 12 h | induces autophagy dose dependently | 21788343 | |
| U87 | Apoptosis Assay | 25 μg/mL | 24/48 h | induces apoptosis at 48 h significantly | 21788343 | |
| U251 | Apoptosis Assay | 25 μg/mL | 24/48 h | induces apoptosis at 48 h significantly | 21788343 | |
| U87 | Growth Inhibition Assay | 0-25 μg/mL | 0-48 h | inhibits cell growth in dose and time dependent manner | 21788343 | |
| U251 | Growth Inhibition Assay | 0-25 μg/mL | 0-48 h | inhibits cell growth in dose and time dependent manner | 21788343 | |
| U251MG | Apoptosis Assay | 1 µM | 48 h | induces apoptosis | 23354807 | |
| U87MG | Apoptosis Assay | 1 µM | 48 h | induces apoptosis | 23354807 | |
| U251MG | Growth Inhibition Assay | 0-25 μM | 24/48 h | inhibits cell growth in dose and time dependent manner | 23354807 | |
| U87MG | Growth Inhibition Assay | 0-25 μM | 24/48 h | inhibits cell growth in dose and time dependent manner | 23354807 | |
| MCF-7 | Apoptosis Assay | 0-20 μM | 48 h | induces apoptosis | 24153102 | |
| T-47D | Apoptosis Assay | 0-20 μM | 48 h | induces apoptosis | 24153102 | |
| MCF-7 | Growth Inhibition Assay | 0-20 μM | 96 h | inhibits cell growth in a dose dependent manner | 24153102 | |
| T-47D | Growth Inhibition Assay | 0-20 μM | 96 h | inhibits cell growth in a dose dependent manner | 24153102 | |
| FaDu | Apoptosis Assay | 25 µM | 48 h | induces apoptosis | 24557056 | |
| CAL27 | Apoptosis Assay | 25 µM | 48 h | induces apoptosis | 24557056 | |
| SCC25 | Apoptosis Assay | 25 µM | 48 h | induces apoptosis | 24557056 | |
| FaDu | Growth Inhibition Assay | 6.25–200 µM | 72 h | results moderate, dose-dependent growth inhibition | 24557056 | |
| CAL27 | Growth Inhibition Assay | 6.25–200 µM | 72 h | results moderate, dose-dependent growth inhibition | 24557056 | |
| SCC25 | Growth Inhibition Assay | 6.25–200 µM | 72 h | results moderate, dose-dependent growth inhibition | 24557056 | |
| H28 | Cell Viability Assay | 1 nM-200 μM | 72 h | decreases cell viability in a dose dependent manner | 24595274 | |
| MM05 | Cell Viability Assay | 1 nM-200 μM | 72 h | decreases cell viability in a dose dependent manner | 24595274 | |
| MSTO-211H | Cell Viability Assay | 1 nM-200 μM | 72 h | decreases cell viability in a dose dependent manner | 24595274 | |
| REN | Cell Viability Assay | 1 nM-200 μM | 72 h | decreases cell viability in a dose dependent manner | 24595274 | |
| LN-308 | Function Assay | 10 μm | 24 h | DMSO | reduces AhR protein levels and DRE reporter activity | 26500056 |
| HaCaT | Function Assay | 10 μm | 48 h | DMSO | reduces TGF-β2 mRNA expression | 26500056 |
| S-24 | Function Assay | 1/10 μm | 24 h | DMSO | reduces DRE reporter activity | 26500056 |
| ZH-161 | Function Assay | 1/10 μm | 24 h | DMSO | reduces DRE reporter activity | 26500056 |
| LN-308 | Function Assay | 1/10/100 μm | 24 h | DMSO | reduces DRE reporter activity in a concentration-dependent manner | 26500056 |
| M21 | Function assay | 1 hr | Binding affinity to integrin alphav/beta3 heterodimer in human M21 cells assessed as inhibition of integrin-mediated human M21 cell adhesion to vitronectin after 1 hr in presence of MnCl2, IC50 = 0.0004 μM. | 26753814 | ||
| HEK293T | Function assay | 2 hrs | Binding affinity to soluble truncated human recombinant Fc-tagged alphaVbeta3 and integrins were expressed in HEK293T cells after 2 hrs by competition ELISA-like assay, IC50 = 0.00051 μM. | 24095096 | ||
| HT-29 | Function assay | 2 hrs | Antagonist activity at integrin alphaVbeta5 (unknown origin) expressed in HT-29 cells assessed as reduction in cell adhesion to vitronectin after 2 hrs by MTT assay, IC50 = 0.12 μM. | 28351594 | ||
| HEK293 | Function assay | 2 hrs | Antagonist activity at integrin alphaVbeta3 (unknown origin) expressed in HEK293 cells assessed as reduction in cell adhesion to fibrinogen after 2 hrs by MTT assay, IC50 = 0.22 μM. | 28351594 | ||
| SKOV3 | Function assay | 2 hrs | Antagonist activity at integrin alphaVbeta3alphaVbeta5 (unknown origin) expressed in SKOV3 cells assessed as reduction in cell adhesion to fibrinogen after 2 hrs by MTT assay, IC50 = 0.37 μM. | 28351594 | ||
| U87MG | Function assay | 100 nM | 24 hrs | Inhibition of alphaVbeta3 integrin in human U87MG cells assessed as increase in p53 accumulation at 100 nM after 24 hrs by Western blot method | 29775303 | |
| U87MG | Function assay | 100 nM | 24 hrs | Inhibition of alphaVbeta3 integrin in human U87MG cells assessed as increase in p53 accumulation at 100 nM after 24 hrs in presence of MDM2 inhibitor nutlin-3 by Western blot method | 29775303 | |
| U87MG | Function assay | 100 nM | 24 hrs | Inhibition of alphaVbeta3 integrin in human U87MG cells assessed as increase in p53 accumulation at 100 nM after 24 hrs in presence of MDM2 inhibitor nutlin-3 and MDM4 inhibitor SJ-1722550 by Western blot method | 29775303 | |
| U87MG | Function assay | 100 nM | 8 hrs | Inhibition of alphaVbeta3 integrin in human U87MG cells assessed as increase in MDM2 mRNA expression at 100 nM after 8 hrs in presence of MDM2 inhibitor nutlin-3 and MDM4 inhibitor SJ-1722550 by RT-PCR method | 29775303 | |
| U87MG | Function assay | 100 nM | 24 hrs | Inhibition of alphaVbeta3 integrin in human U87MG cells assessed as increase in PUMA mRNA expression at 100 nM after 24 hrs by RT-PCR method | 29775303 | |
| U87MG | Function assay | 100 nM | 24 hrs | Inhibition of alphaVbeta3 integrin in human U87MG cells assessed as increase in PUMA mRNA expression at 100 nM after 24 hrs in presence of MDM2 inhibitor nutlin-3 by RT-PCR method | 29775303 | |
| U87MG | Function assay | 100 nM | 24 hrs | Inhibition of alphaVbeta3 integrin in human U87MG cells assessed as increase in PUMA mRNA expression at 100 nM after 24 hrs in presence of MDM4 inhibitor SJ-1722550 by RT-PCR method | 29775303 | |
| U87MG | Function assay | 100 nM | 24 hrs | Inhibition of alphaVbeta3 integrin in human U87MG cells assessed as increase in PUMA mRNA expression at 100 nM after 24 hrs in presence of MDM2 inhibitor nutlin-3 and MDM4 inhibitor SJ-1722550 by RT-PCR method | 29775303 | |
| U87MG | Function assay | 100 nM | 24 hrs | Inhibition of alphaVbeta3 integrin in human U87MG cells assessed as increase in p21 mRNA expression at 100 nM after 24 hrs by RT-PCR method | 29775303 | |
| U87MG | Antiproliferative assay | 100 nM | 72 hrs | Antiproliferative activity against human U87MG cells at 100 nM after 72 hrs in presence of MDM2 inhibitor nutlin-3 by MTS assay | 29775303 | |
| U87MG | Antiproliferative assay | 100 nM | 72 hrs | Antiproliferative activity against human U87MG cells at 100 nM after 72 hrs in presence of MDM2 inhibitor nutlin-3 and MDM4 inhibitor SJ-1722550 by MTS assay | 29775303 | |
| U87MG | Cell cycle assay | 100 nM | 24 hrs | Cell cycle arrest in human U87MG cells assessed as accumulation at G0/G1 phase at 100 nM after 24 hrs | 29775303 | |
| U87MG | Anti-invasive assay | 10 uM | 24 hrs | Anti-invasive activity in human U87MG cells at 10 uM after 24 hrs by transwell assay | 29775303 | |
| U87MG | Anti-invasive assay | 10 uM | 24 hrs | Anti-invasive activity in human U87MG cells at 10 uM after 24 hrs in presence of MDM2 inhibitor nutlin-3 and MDM4 inhibitor SJ-1722550 by transwell assay | 29775303 | |
| Haga clic para ver más datos experimentales de líneas celulares | ||||||
Información química, almacenamiento y estabilidad
| Peso molecular | 702.68 | Fórmula | C29H41F3N8O9 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 199807-35-7 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | EMD 121974, NSC 707544 | Smiles | CC(C)C1C(=O)NC(C(=O)NCC(=O)NC(C(=O)NC(C(=O)N1C)CC2=CC=CC=C2)CC(=O)O)CCCN=C(N)N.C(=O)(C(F)(F)F)O | ||
Solubilidad
|
In vitro |
DMSO
: 100 mg/mL
(142.31 mM)
Water : 6.25 mg/mL Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
αvβ3 receptor
(Cell-free assay) 4.1 nM
αvβ5 receptor
(Cell-free assay) 79 nM
|
|---|---|
| In vitro |
Cilengitide es un peptidomimético pentapeptídico ciclado diseñado para competir por la secuencia peptídica de arginina-glicina-ácido aspártico (RGD) que regula la unión ligando-integrina. Cilengitide bloquea de forma selectiva y potente la ligación de las integrinas αvβ3 y αvβ5 a proteínas de la matriz provisional como la vitronectina, fibronectina, fibrinógeno, factor de von Willebrand, osteopontina y otras.
Cilegitide inhibe la angiogénesis in vitro. 10 μM de Cilengitide inhibe completamente la adhesión de células BAE, BME y HUVE a vitronectina y fibronectina. Cilengitide inhibe la angiogénesis in vitro de células BAE en geles tridimensionales de colágeno y fibrina pretratados con FGF-2 (o VEGF-A) con una IC50 de 15 μM y 8 μM, 4 μM y 3 μM, respectivamente.
Cilengitide bloquea la proliferación e induce la apoptosis de células endoteliales, así como la diferenciación de células precursoras endoteliales humanas (EPCs). 50 μg/mL de Cilengitide inhibe completamente la proliferación de la línea celular endotelial microvascular humana HMEC-1 y conduce a la apoptosis en ~30% de las células. 1,0 μM de Cilengitide, tratando durante 9 días, inhibe la proliferación de EPCs en casi un 40%. 1 μM de Cilengitide inhibe la diferenciación de EPCs en más de un 80% a los 14 días.
Cilengitide inhibe la adhesión e induce la apoptosis de células tumorales. 25 μg/mL de Cilengitide causa el desprendimiento de células DAOY (meduloblastoma) y células U87MG (glioblastoma) de vitronectina y tenascina en más de un 60%. 25 μg/mL de Cilengitide induce una tasa de apoptosis de casi el 50% de estas células.
|
| Ensayo de quinasa |
Ensayo de competición por la unión a integrinas
|
|
Las integrinas solubles recombinantes se inmovilizan, y los péptidos, que se diluyen en serie en solución salina tamponada con Tris (TBS++) (0,1% (p/v) de BSA, 150 mM de NaCl, 1 mM de CaCl2, 1 mM de MgCl2, 10 μM de MnCl2, 20 mM de Tris-HCl; pH 7,4), se añaden en paralelo con vitronectina biotinilada (hasta 1 μg/mL). Después de una incubación de 3 horas a 37 °C y un lavado con solución salina tamponada con Tris, el ligando unido se detecta mediante incubación con un anticuerpo conjugado con fosfatasa alcalina anti-biotina (BioRad) seguido de un desarrollo con sustrato de p-nitrofenil fosfatasa. La reacción se detiene mediante la adición de NaOH y la intensidad del color se lee a 405 nm.
|
|
| In vivo |
Cilengitide es activo contra el crecimiento tumoral y la angiogénesis como agente único. 100 μg de Cilengitide inducen una disminución significativa en el número de vasos CD31+ observados en tumores (2/campo de alta potencia) en comparación con tumores de control (56/campo de alta potencia). 100 μg de Cilengitide aumentan la apoptosis celular en los tumores cerebrales de animales (2,2% de células apoptóticas/campo de alta potencia) en comparación con aquellos que recibieron el péptido inactivo (1,7% de células/campo de alta potencia). El tratamiento con Cilengitide resulta en una supervivencia prolongada de los ratones portadores de xenoinjertos de melanoma M21 en comparación con el grupo de tratamiento de control (36,5 vs 17,3 días).
Cilengitide puede aumentar el beneficio terapéutico asociado con agentes citotóxicos, incluida la quimioterapia y la radioterapia, en modelos tumorales. Cilengitide (250 mg/dosis) solo no altera el crecimiento tumoral de xenoinjertos de cáncer de mama en comparación con ratones no tratados, pero la modalidad combinada RIT (CMRIT) utilizando RIT y seis dosis de Cilengitide (250 mg/dosis) aumenta la eficacia del tratamiento, con una tasa de curación para los ratones que solo reciben RIT que aumenta del 15 al 53%. CMRIT aumenta significativamente la apoptosis de células tumorales y endoteliales a los 5 días y disminuye la proliferación tumoral.
|
Referencias |
|
Aplicaciones
| Métodos | Biomarcadores | Imágenes | PMID |
|---|---|---|---|
| Western blot | GLI1 pFAK / p-AKT |
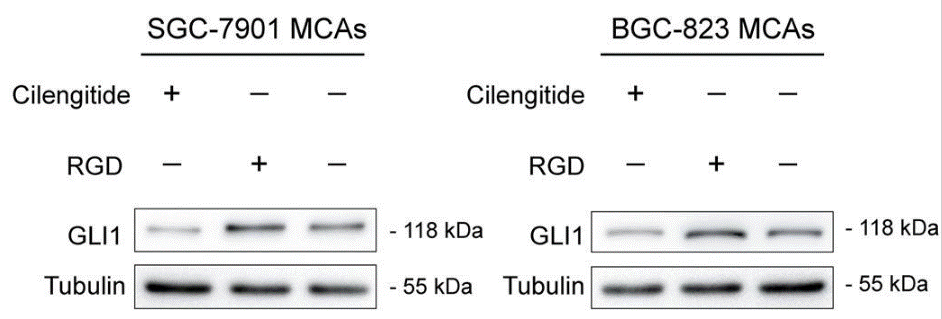
|
31366904 |
| Immunofluorescence | VE-cadherin / β3 integrin |
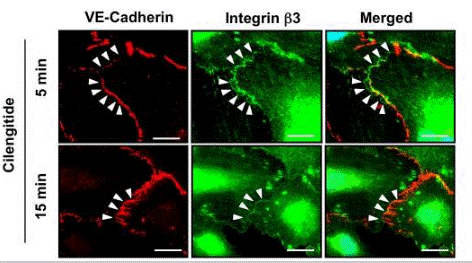
|
19212436 |
| Growth inhibition assay | Cell number |
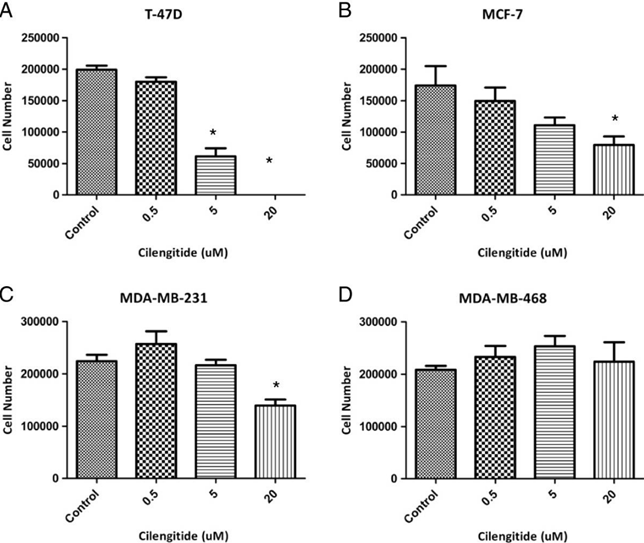
|
24153102 |
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT01517776 | Terminated | Gliomas |
Martin-Luther-Universität Halle-Wittenberg|Merck KGaA Darmstadt Germany |
January 2012 | Phase 2 |
| NCT01118676 | Completed | Locally Advanced Non Small Cell Lung Cancer (NSCLC) |
Institut Claudius Regaud|Merck KGaA Darmstadt Germany |
March 2010 | Phase 1 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
Preguntas frecuentes
Pregunta 1:
The recommended vehicle for it is 30% propylene glycol, 5% Tween 80, 65% D5W at 30mg/ml. Can you let me know if this is a suspension or clear solution?
Respuesta:
S7077 can be dissolved in 30% propylene glycol/5% Tween 80/65% D5W at 10 mg/ml as a clear solution.
Pregunta 2:
Is it a TFA salt?
Respuesta:
S7077 is actually a TFA salt, and the ratio between it and TFA is 1:1.
