solo para uso en investigación
Apremilast PDE inhibidor
Cat. No.S8034
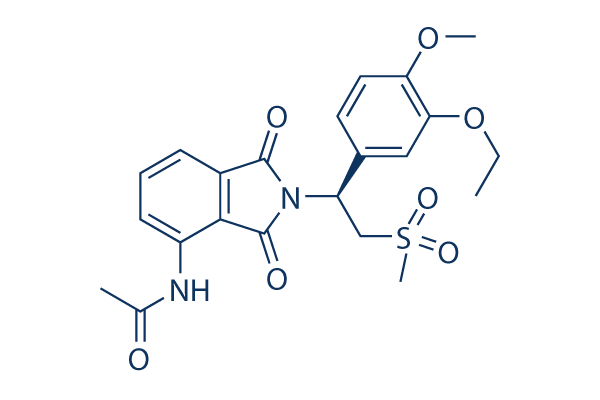
Estructura química
Peso molecular: 460.5
Control de calidad
Información química, almacenamiento y estabilidad
| Peso molecular | 460.5 | Fórmula | C22H24N2O7S |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 608141-41-9 | -- | Almacenamiento de soluciones madre |
|
|
| Sinónimos | CC-10004 | Smiles | CCOC1=C(C=CC(=C1)C(CS(=O)(=O)C)N2C(=O)C3=C(C2=O)C(=CC=C3)NC(=O)C)OC | ||
Solubilidad
|
In vitro |
DMSO
: 92 mg/mL
(199.78 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
PDE4
74 nM
TNF-α
77 nM
|
|---|---|
| In vitro |
Apremilast es más potente para la inhibición de PDE4 en comparación con las enzimas hidrolizantes de cAMP o cGMP de otras familias de PDE. Este compuesto muestra un amplio patrón de actividad antiinflamatoria en una variedad de tipos celulares, inhibe la producción de TNF-α, IL-12 e IL-23, así como las respuestas de las células NK y los queratinocitos. Se ha encontrado que inhibe la producción de IL-8 inducida por zimosán en PMN con una IC50 de 94 nM. Este químico inhibe la expresión de CD18 y CD11b en PMN inducida por fMLF con una IC50 de 390 nM y 74 nM, respectivamente, e inhibe la adhesión de PMN a HUVECs inducida por fMLF con una IC50 de 150 nM. Inhibe la producción de TNF-α por queratinocitos, sin efecto sobre la viabilidad de las células queratinocíticas medida por los niveles de ATP intracelular. .
|
| Ensayo de quinasa |
Actividad inhibidora de PDE4
|
|
Las células (1×109) se lavan en PBS y se lisan en tampón de homogeneización frío (20 mM Tris-HCl, pH 7,1, 3 mM 2-mercaptoetanol, 1 mM MgCl2, 0,1 mM EGTA, 1 μM PMSF, 1 μg/mL leupeptina). Tras la homogeneización en un homogeneizador Dounce, el sobrenadante se recoge por centrifugación y se carga en una columna Sephacryl S-200 equilibrada en tampón de homogeneización. La PDE se eluye en tampón de homogeneización y las fracciones sensibles a rolipram se agrupan y almacenan en alícuotas. La actividad enzimática se ensaya en 50 mM Tris-HCl, pH 7,5, 5 mM MgCl2 y 1 μM cAMP (de los cuales el 1% es 3H cAMP) en presencia de concentraciones variables de inhibidores. La cantidad de extracto utilizada se predetermina para asegurar que las reacciones estén dentro del rango lineal y consuman menos del 15% del sustrato total. Las reacciones se realizan a 30 °C durante 30 min y se terminan hirviendo durante 2 min. Las muestras se enfrían y se tratan con veneno de serpiente (1 mg/mL) a 30 °C durante 15 min. El sustrato no utilizado se elimina mediante incubación con 200 μL de resina AG1-X8 durante 15 min. Luego, las muestras se centrifugan a 3000 rpm durante 5 min y se toman 50 μL de la fase acuosa para el recuento. Cada punto de datos se realiza por duplicado, expresando la actividad como porcentaje del control. La IC50 se determina a partir de curvas de respuesta a la dosis derivadas de tres experimentos independientes.
|
|
| In vivo |
Apremilast es estable en presencia de microsomas humanos (t1/2 > 60 min). Se une en un 90% a proteínas en plasma humano. La administración oral e intravenosa de este compuesto en ratas hembra mostró que tiene una buena farmacocinética con baja depuración, un volumen de distribución moderado y una biodisponibilidad oral del 64%. En un modelo de inhibición de TNF-α inducida por LPS en ratas, se examinó la capacidad de inhibición de TNF-α de este compuesto in vivo, y la ED50 se determinó en 0,03 mg/kg. En otro modelo de neutrofilia inducida por LPS en ratas, este compuesto exhibió un rango de ED50 de 0,3 mg/kg a 0,9 mg/kg.
|
Referencias |
|
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT06382987 | Recruiting | Plaque Psoriasis |
Bristol-Myers Squibb |
January 22 2024 | -- |
| NCT06122649 | Recruiting | Plaque Psoriasis |
Amgen |
November 27 2023 | Phase 3 |
| NCT06108544 | Recruiting | Plaque Psoriasis |
Takeda |
November 6 2023 | Phase 3 |
| NCT06088043 | Recruiting | Plaque Psoriasis |
Takeda |
November 6 2023 | Phase 3 |
| NCT05926882 | Completed | Alopecia Areata |
Jinnah Postgraduate Medical Centre |
August 1 2022 | Phase 4 |
| NCT04804553 | Recruiting | Active Juvenile Psoriatic Arthritis |
Amgen |
March 17 2022 | Phase 3 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
