solo para uso en investigación
TTNPB (Arotinoid acid) Agonista RAR
Cat. No.S4627
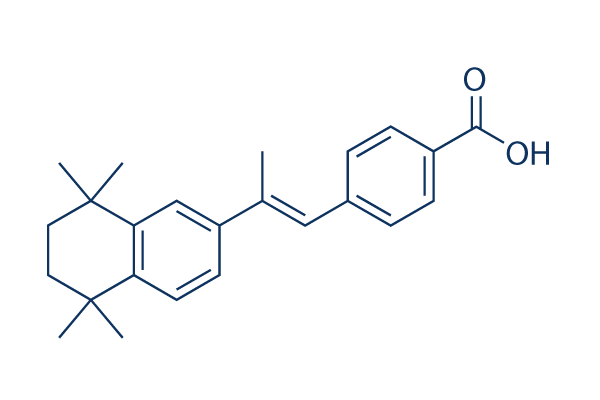
Estructura química
Peso molecular: 348.48
Control de calidad
| Dianas relacionadas | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Otros Retinoid Receptor Inhibidores | Tamibarotene AM580 Fenretinide UVI 3003 SR 11237 AR7 BMS493 All trans-Retinal MSU-42011 Palovarotene |
Cultivo celular, tratamiento y concentración de trabajo
| Líneas celulares | Tipo de ensayo | Concentración | Tiempo de incubación | Formulación | Descripción de la actividad | PMID |
|---|---|---|---|---|---|---|
| HEK293 cells | Function assay | Agonist activity at human RARalpha expressed in HEK293 cells by luciferase reporter gene assay, EC50=0.18 nM | ||||
| CV-1 cells | Function assay | Binding affinity against retinoic Acid gamma receptors co-transfected into CV-1 cells, EC50=0.002 Μm | ||||
| HL60 cells | Cytotoxicity assay | In vitro cytotoxicity against HL60 cells, IC50=46 μM | ||||
| HeLa cells | Function assay | Agonist activity at human RARalpha expressed in human HeLa cells assessed as relative luminescence units at >=10 uM by luciferase assay relative to control | ||||
| Haga clic para ver más datos experimentales de líneas celulares | ||||||
Información química, almacenamiento y estabilidad
| Peso molecular | 348.48 | Fórmula | C24H28O2 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 71441-28-6 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | Arotinoid Acid, Ro 13-7410, AGN-191183 | Smiles | CC(=CC1=CC=C(C=C1)C(=O)O)C2=CC3=C(C=C2)C(CCC3(C)C)(C)C | ||
Solubilidad
|
In vitro |
DMSO
: 15 mg/mL
(43.04 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
RARβ
(cell-free assay) 4.5 nM
RARα
(cell-free assay) 5.1 nM
RARγ
(cell-free assay) 9.3 nM
|
|---|---|
| In vitro |
TTNPB se une a los Retinoid Receptor nucleares con alta afinidad, e inhibe la unión de [3H]tRA con una IC50 de 3,8 nM, 4,0 nM y 4,5 nM para mRARα, β y γ, respectivamente. Este compuesto aumenta la activación transcripcional de los RAR de ratón en células JEG-3 después de 72 h utilizando medios condicionados con una EC50 de 2,0 nM, 1,1 nM y 0,8 nM para mRARα, β y γ, respectivamente. Inhibe el crecimiento de células epiteliales mamarias humanas normales (HMEC) y células de cáncer de mama positivas para el receptor de estrógenos (ER-positivas) al inducir un bloqueo del ciclo celular G1. Este químico provoca una disminución dependiente de la concentración en la diferenciación de células ES-D3.
|
| Ensayo de quinasa |
Ensayos de unión
|
|
Los ensayos de unión se realizan como se describió anteriormente (Allenby et al., 1993, 1994). Brevemente, los retinoides marcados y no marcados se añaden a fracciones nucleosólicas o citosólicas en etanol, de modo que la cantidad total de etanol añadida sea constante en todos los tubos y no exceda el 2% del volumen de incubación. Las preparaciones de receptores se incuban con retinoides a 4°C durante 4-6 horas. Se utilizan columnas de desalación Sephadex PD-10 para separar el radioligando unido del radioligando libre una vez que se alcanza el equilibrio. Para los ensayos de unión competitiva, se incuban concentraciones variables de ligando competidor no marcado con el nucleosol o citosol apropiado en presencia de una concentración fija de [3H]tRA (act. esp. 49,3 Ci/mmol) o [3H]9-cis RA (act. esp. 24,0 Ci/mmol). Las concentraciones finales de [3H]tRA y [3H]9-cis RA para los ensayos de unión a Retinoid Receptor nucleares son de 5 nM. Las concentraciones finales de [3H]tRA para los ensayos de unión a CRABP son de 30 nM. Las IC50 se calculan como se describió anteriormente (DeLean et al., 1978). Para la cinética de saturación, se añaden concentraciones crecientes de ligando radiomarcado ([3H]tRA act. esp. 49,3 Ci/mmol, [3H]this compound act. esp. 5,5 Ci/mmol) al nucleosol del subtipo de receptor apropiado en presencia (unión no específica) o ausencia (unión total) de un exceso molar de 100 veces del retinoide no marcado correspondiente. La unión específica se define como la unión total menos la unión no específica. Las cinéticas de saturación se calculan como se describió anteriormente (Scatchard, 1949; Grippo y Gudas, 1987; Levin et al., 1992).
|
|
| In vivo |
TTNPB (0,25 mg/kg) provoca la inhibición del crecimiento en los modelos MXT-HS y MXT-HI al inducir la apoptosis celular.
|
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
