solo para uso en investigación
Tiplaxtinin (PAI-039) PAI-1 inhibidor
Cat. No.S7922
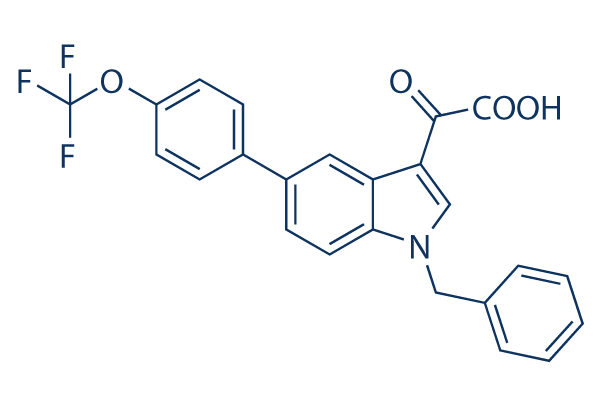
Estructura química
Peso molecular: 439.38
Control de calidad
| Dianas relacionadas | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Otros PAI-1 Inhibidores | Notoginsenoside R1 Loureirin B Toddalolactone TM5275 Sodium TM5441 |
Información química, almacenamiento y estabilidad
| Peso molecular | 439.38 | Fórmula | C24H16F3NO4 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 393105-53-8 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | N/A | Smiles | C1=CC=C(C=C1)CN2C=C(C3=C2C=CC(=C3)C4=CC=C(C=C4)OC(F)(F)F)C(=O)C(=O)O | ||
Solubilidad
|
In vitro |
DMSO
: 88 mg/mL
(200.28 mM)
Ethanol : 7 mg/mL Water : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
PAI-1
2.7 μM
|
|---|---|
| In vitro |
Tiplaxtinin (PAI-039) reduce la proliferación celular, la adhesión celular y la formación de colonias, e induce la apoptosis y la anoikis en un panel de líneas celulares de vejiga humana.
|
| Ensayo de quinasa |
Ensayos de actividad in vitro directa de PAI-I
|
|
El ensayo cromogénico se inicia con la adición de Tiplaxtinin (PAI-039) (concentración final de 10 a 100 µM, concentración máxima de DMSO del 0,2%) a PAI-1 humano recombinante (140 nM en tampón pH 6,6). Después de una incubación de 15 minutos a 25°C, se añaden 70 nM de t-PA humano recombinante, y la combinación de este compuesto, PAI-1 y tPA se incuba durante 30 minutos adicionales. Después de la segunda incubación, se añade Spectrozyme tPA y la absorbancia se lee a 405 nm a 0 y 60 minutos. La actividad inhibidora relativa de PAI-1 es igual a la actividad residual de tPA en el tratamiento con Tiplaxtinin/PAI-1. Los tratamientos de control incluyen la inhibición completa de tPA por PAI-1 en la relación molar empleada (2:1), y la ausencia de cualquier efecto sobre t-PA solo. El ensayo inmunofuncional se basa en la interacción no disociable por SDS entre tPA y PAI-1 activo. Las placas de ensayo se recubren con 100 µl de una solución de t-PA (10 µg/ml en TBS) y se mantienen a 4 °C durante la noche. Este compuesto se disuelve en DMSO y se diluye a una concentración final de 1-100 µM como se describió anteriormente. Luego se incuba con PAI-1 humano (50 ng/ml) durante 15 minutos, y una alícuota de esta solución se añade a la placa recubierta con t-PA durante 1 h. La solución se aspira de la placa, que luego se lava con un tampón que consiste en 0,05% de Tween 20 y 0,1% de BSA en TBS. Este ensayo detecta solo el PAI-1 inhibidor activo (no latente o sustrato) unido a la placa, y se cuantifica utilizando un anticuerpo monoclonal contra PAI-1 humano (MA33B8). Una dilución 1000X de MA33B8 se añade a la placa y se incuba durante una hora, se aspira y se lava. Se añade un anticuerpo secundario consistente en un conjugado de fosfatasa alcalina IgG (H+L)-AP de cabra anti-ratón, se incuba durante una hora, se aspira y se lava. Se añade una alícuota de 100 µl de solución de fosfatasa alcalina, seguida de la determinación de la absorbancia a 405 nm 60 minutos después. La cuantificación del PAI-1 activo residual unido a t-PA a diferentes concentraciones se utiliza para determinar la IC50 ajustando los resultados a un programa logístico de dosis-respuesta, con la IC50 definida como la concentración del compuesto requerida para lograr el 50% de inhibición de la actividad de PAI-1. La sensibilidad del ensayo es de 5 ng/ml de PAI-1 humano, según lo determinado a partir de una curva estándar que va de 0 a 100 ng/ml de PAI-1 humano.
|
|
| In vivo |
Tiplaxtinin (PAI-039) ha demostrado en múltiples estudios exhibir diversos efectos biológicos. En un modelo de trombosis carotídea en ratas, este (1 mg/kg, p.o.) aumenta el tiempo hasta la oclusión y previene la reducción del flujo sanguíneo carotídeo. En ratones C57BL/6J, (1 mg/g de alimento) atenúa el remodelado aórtico inducido por Ang II. En ratones diabéticos tipo 1 no tratados, este compuesto (p.o.) restaura la regeneración del músculo esquelético. En ratones atímicos portadores de xenoinjertos de líneas celulares de cáncer humano T24 y HeLa, este (1 mg/kg, p.o.) reduce el crecimiento del xenoinjerto tumoral, asociado con una reducción de la angiogénesis tumoral, una reducción de la proliferación celular y un aumento de la apoptosis.
|
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
