solo para uso en investigación
Ramatroban Prostaglandin Receptor antagonista
Cat. No.S5286
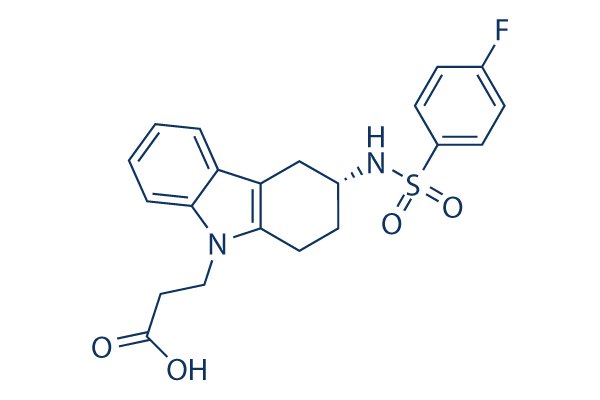
Estructura química
Peso molecular: 416.47
Control de calidad
| Dianas relacionadas | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Otros Prostaglandin Receptor Inhibidores | PF-04418948 TG4-155 Ethamsylate E7046 (ER-886406) Grapiprant (CJ-023,423) Timapiprant Sodium Seratrodast(AA-2414) Ozagrel Rebamipide mofetil (-)-(S)-α-terpineol |
Información química, almacenamiento y estabilidad
| Peso molecular | 416.47 | Fórmula | C21H21FN2O4S |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 116649-85-5 | -- | Almacenamiento de soluciones madre |
|
|
| Sinónimos | BAY u 3405 | Smiles | C1CC2=C(CC1NS(=O)(=O)C3=CC=C(C=C3)F)C4=CC=CC=C4N2CCC(=O)O | ||
Solubilidad
|
In vitro |
DMSO
: 83 mg/mL
(199.29 mM)
Ethanol : 83 mg/mL Water : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
TxA2 receptor
|
|---|---|
| In vitro |
Ramatroban puede bloquear el receptor de PGD2, molécula homóloga al receptor quimioatrayente expresada en las células Th2 (CRTh2). Este compuesto puede suprimir la expresión de la proteína quimioatrayente de monocitos-1 (MCP-1) y las moléculas de adhesión en las células endoteliales y prevenir la exacerbación de la inflamación al bloquear estas respuestas. Tiene efectos inhibidores sobre la agregación plaquetaria y la contracción del músculo liso vascular. Este producto químico inhibió significativamente la unión de [3H]PGD2 a CRTh2 con un valor de IC50 de 100 nM. También inhibió, de manera dependiente de la concentración, la movilización de Ca2+ inducida por PGD2 en transfectantes de CRTh2 con un IC50 = 30 nM y suprimió la migración de eosinófilos humanos inducida por PGD2 con un IC50 = 170 nM.
|
| In vivo |
En conejos hipercolesterolémicos, ramatroban previene la infiltración de macrófagos mediante la regulación a la baja de MCP-1 y la formación de neointima después de una lesión con balón y atenúa la respuesta vascular a la acetilcolina. Los parámetros farmacocinéticos después de una única administración oral de 75 mg de este compuesto se estudiaron en voluntarios adultos sanos en ayunas: la biodisponibilidad relativa de sus comprimidos (en comparación con la solución acuosa) fue del 80,3%. La farmacocinética de este producto químico en dosis que oscilaron entre 25 y 150 mg resultó ser lineal. Cuando se administró una dosis única de 50 mg de este agente por vía oral a voluntarios sanos después de las comidas, el AUC fue del 88,8% del obtenido en estado de ayuno. Se observa un aclaramiento corporal total bajo de esta sustancia en sujetos de edad avanzada; después de la administración oral de material marcado con [14C] a ratas macho, las concentraciones máximas de radioactividad fueron más altas en el hígado, los riñones y los tejidos adiposos que en el plasma. Otros tejidos orgánicos tuvieron niveles de radioactividad más bajos que el plasma. Los niveles de radioactividad en la mayoría de los tejidos orgánicos disminuyeron paralelamente a la disminución de la radioactividad plasmática. En contraste, la eliminación de la radioactividad de las células sanguíneas fue relativamente prolongada. Se encontraron niveles extremadamente bajos de radioactividad solo en el cerebro. La relación de los niveles cerebro-plasma fue tan baja como el 8% en el máximo.
|
Referencias |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
