solo para uso en investigación
Meldonium Hydroxylase inhibidor
Cat. No.S4130
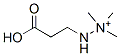
Estructura química
Peso molecular: 147.19
Control de calidad
| Dianas relacionadas | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Otros Hydroxylase Inhibidores | Ro 61-8048 4-Chloro-DL-phenylalanine Nepicastat (SYN-117) HCl 2-Thiouracil (R)-Nepicastat HCl H-Tyr(3-I)-OH |
Información química, almacenamiento y estabilidad
| Peso molecular | 147.19 | Fórmula | C6H14N2O2 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 76144-81-5 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | MET-88, Quaterin | Smiles | C[N+](C)(C)NCCC(=O)[O-].O.O | ||
Solubilidad
|
In vitro |
Water : 29 mg/mL Ethanol : 29 mg/mL
DMSO
: Insoluble
|
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
GBB hydroxylase
|
|---|---|
| In vitro |
Meldonium (40 μM) inhibe la reacción de la γ-butyrobetaine hydroxylase con la γ-butirobetaína con Km y Vmax de 36,8 μM y 0,08 nmol/min/mg de proteína, respectivamente. |
| In vivo |
Meldonium administrado oralmente a ratas durante 10 días (150 mg/kg) provoca una reducción del contenido miocárdico de carnitina libre y acilcarnitina de cadena larga en un 63,7 y 74,3 %, respectivamente. El tratamiento con este compuesto (100 mg/kg, oral) y la posterior administración de isoproterenol resultan en una reducción de la concentración de carnitina libre en un 48,7 % en comparación con las ratas que recibieron isoproterenol. Una administración previa de esta sustancia química protege eficazmente el miocardio de las variaciones inducidas por el isoproterenol en el contenido de ATP y la carga energética miocárdica, así como previene un aumento en la actividad de la creatina fosfocinasa y la lactato deshidrogenasa. El tratamiento a largo plazo con este compuesto (200 mg/kg) aumenta significativamente la tasa de captación de glucosa estimulada por insulina en un 35 % y la expresión del transportador de glucosa 4 (aumento de 1,7 veces), la hexocinasa II (aumento de 2,1 veces), las proteínas del receptor de insulina (aumento de 2,5 veces) y las carnitina palmitoiltransferasas IA (aumento de 2,2 veces) en corazones de ratón. Este tratamiento químico a largo plazo disminuye estadísticamente significativamente la glucosa en sangre en estado de alimentación de 6 a 5 mM. Reduce las alteraciones inducidas por azidotimidina en el tejido cerebral de ratones. Este compuesto (50 mg/kg) normaliza el aumento de la caspasa-3, la proteína de susceptibilidad a la apoptosis celular (CAS) y la expresión de iNOS. También normaliza los cambios en la expresión de la citocromo c oxidasa (COX), reduce la expresión de la proteína ácida fibrilar glial (GFAP) y la infiltración celular. Esta sustancia química muestra efectos protectores en un modelo experimental de diabetes tipo 2 en ratas Goto-Kakizaki. El tratamiento con esta (200 mg/kg) disminuye la glucosa en sangre tanto en ayunas como en estado de alimentación. Este compuesto inhibe fuertemente la acumulación de fructosamina y la pérdida de sensibilidad al dolor (en un 75 %) y también mejora la respuesta contráctil aumentada de los anillos aórticos de ratas Goto-Kakizaki a la fenilefrina. Además, en los corazones tratados con esta sustancia química, la zona de necrosis después de la oclusión coronaria disminuye significativamente en un 30 %. |
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
