solo para uso en investigación
Toremifene Citrate (NK 622) Estrogen/progestogen Receptor modulador
Cat. No.S1776
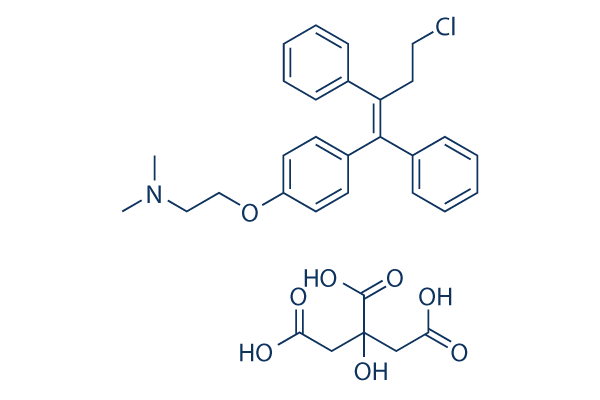
Estructura química
Peso molecular: 598.08
Control de calidad
| Dianas relacionadas | Adrenergic Receptor GPR Androgen Receptor Glucocorticoid Receptor ACE RAAS Progesterone Receptor Opioid Receptor PGES THR |
|---|---|
| Otros Estrogen/progestogen Receptor Inhibidores | Elacestrant (RAD1901) Dihydrochloride Vepdegestrant (ARV-471) MPP dihydrochloride Kaempferol Cholesterol G15 Endoxifen HCl Licochalcone A Chrysin Pregnenolone |
Información química, almacenamiento y estabilidad
| Peso molecular | 598.08 | Fórmula | C32H36ClNO8 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 89778-27-8 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | NSC 613680,NK 622 Citrate | Smiles | CN(C)CCOC1=CC=C(C=C1)C(=C(CCCl)C2=CC=CC=C2)C3=CC=CC=C3.C(C(=O)O)C(CC(=O)O)(C(=O)O)O | ||
Solubilidad
|
In vitro |
DMSO
: 100 mg/mL
(167.2 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
Estrogen receptor
|
|---|---|
| In vitro |
El toremifeno (7,5 mM) provoca que aproximadamente el 60% de las células exhiban características morfológicas típicas de las células que sufren muerte programada, o apoptosis, en células de cáncer de mama humanas. El toremifeno (5-10 mM) resulta en niveles elevados de ARNm de TRPM-2 y TGF beta 1 en células tumorales cultivadas in vitro o in vivo. El toremifeno causa la inhibición del crecimiento de células de cáncer de mama sensibles al estrógeno al inducir la apoptosis en algunas células y al inhibir la entrada en mitosis de otras. El toremifeno induce un nivel de aductos dependiente de la dosis que es menor que el observado para el TAM. El toremifeno mejora significativamente la formación de aductos de ADN endógenos. El toremifeno afecta la renovación celular al inhibir la actividad mitótica y modificar una abundante apoptosis espontánea en el carcinoma mamario de rata inducido por DMBA.
|
| In vivo |
El toremifeno, a la dosis más alta probada, aumenta la incidencia de carcinomas hepatocelulares en los grupos iniciados con DEN a un nivel un tercio del observado con la administración de tamoxifeno a ratas iniciadas con DEN. El toremifeno aumenta la incidencia de hipernefromas en ratas previamente iniciadas con DEN. El toremifeno produce aneuploidía en el 50% de las células examinadas y se compara con el nivel del 85% inducido por el tamoxifeno en ratas Sprague-Dawley hembra.
|
Referencias |
|
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT01214291 | Withdrawn | Risk of Bone Fracture Occurrences |
GTx|Ipsen |
March 2011 | Phase 3 |
| NCT00267553 | Terminated | Breast Neoplasms|Neoplasms Hormone-Dependent |
Intarcia Therapeutics |
November 2005 | Phase 3 |
| NCT00106691 | Completed | Preneoplastic Conditions|Prostatic Intraepithelial Neoplasia |
GTx |
January 2005 | Phase 3 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
