solo para uso en investigación
AMD3465 hexahydrobromide CXCR antagonista
Cat. No.S2879
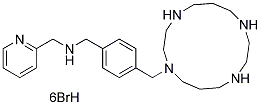
Estructura química
Peso molecular: 896.07
Control de calidad
- Citado en Nature Medicine por su máxima calidad
- COA
- NMR
- HPLC
- SDS
- Hoja de datos
| Dianas relacionadas | Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas GPR |
|---|---|
| Otros CXCR Inhibidores | AZD5069 SB 225002 Reparixin (Repertaxin) WZ811 Navarixin (SCH-527123) LIT-927 AMG 487 SX-682 LY2510924 Danirixin (GSK1325756) |
Información química, almacenamiento y estabilidad
| Peso molecular | 896.07 | Fórmula | C24H38N6.6HBr |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 185991-07-5 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | N/A | Smiles | C1CNCCNCCCN(CCNC1)CC2=CC=C(C=C2)CNCC3=CC=CC=N3.Br.Br.Br.Br.Br.Br | ||
Solubilidad
|
In vitro |
Water : 98 mg/mL
DMSO
: 2 mg/mL
(2.23 mM)
Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
CXCR4
|
|---|---|
| In vitro |
AMD3465 bloquea la unión de CXCL12 con una CI50 de 18 nM en células SupT1. AMD3465 inhibe la señalización de calcio inducida por CXCL12 en células SupT1 con una CI50 de 17 nM y también inhibe la fosforilación de MAPK. Sin embargo, AMD3465 no pudo bloquear los flujos de calcio intracelulares provocados por los ligandos de CCR5 RANTES, LD78β y MIP-1β en células U87.CD4.CCR5. AMD3465 suprime la quimiotaxis inducida por CXCL12 de células T-linfoides humanas SupT1 y previene la internalización de CXCR4 inducida por quimiocinas en células U87.CD4. Además, AMD3465 demuestra ser activo contra las cepas X4 de VIH-1 IIIB, NL4.3, RF y HE con una CI50 de 6-12 nM. AMD3465 suprime las cepas de VIH-2 ROD y EHO con una CI50 de 12.3 nM. AMD3465 inhibe la unión del ligando SDF-1α con un Ki de 41.7 nM utilizando la línea celular CCRF-CEM. La inhibición de las vías de señalización de CXCR4 por AMD3465 se demuestra mediante la inhibición del flujo de calcio estimulado por SDF-1α y la unión de GTP con una CI50 de 12.07 nM y 10.38 nM, respectivamente. Además, AMD3465 es capaz de inhibir la respuesta fisiológica mediada por CXCR4, la quimiotaxis celular, con una CI50 de 8.7 nM. Además, AMD3465 no tiene efecto inhibidor sobre el flujo de calcio mediado por MIP1α, MCP-1, TARC, RANTES, MIP-3β o IP10, ligandos para CCR1, CCR2b, CCR4, CCR5, CCR7 y CXCR3 respectivamente, o la unión de LTB4 a BLT1, lo que indica que AMD3465 es un inhibidor selectivo de CXCR4 sobre otros receptores de quimiocinas. En un estudio separado, se muestra que AMD3465 inhibe la internalización de CXCR4 mediada por SDF-1 en células que expresan CXCR4 unido a GFP, y no causa la internalización del receptor cuando se incuba con las células solas.
|
| In vivo |
La farmacocinética de AMD3465 se investiga en ratones y perros. La absorción es rápida después de la administración subcutánea. AMD3465 se elimina del plasma canino de manera bifásica con una vida media terminal de 1.56-4.63 h. AMD3465 muestra una biodisponibilidad del 100% después de la administración subcutánea en comparación con la exposición a las dosis intravenosas y subcutáneas. AMD3465 causa leucocitosis cuando se administra por vía subcutánea en ratones y perros, con una movilización máxima que ocurre entre 0.5 h y 1.5 h después de la dosis subcutánea en ratones y con una concentración plasmática máxima del compuesto que precede a la movilización máxima en perros, lo que indica que AMD3465 tiene el potencial de movilizar células madre hematopoyéticas. AMD3465 anula la formación de granuloma tipo 2 y la movilización de eosinófilos a dosis de 6 y 30 mg/kg. El tratamiento con AMD3465 podría causar una reducción de ~90% en los niveles de transcripción de CXCR4 en pulmones con lesiones tipo 2.
|
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
