solo para uso en investigación
Ranitidine Hydrochloride Histamine Receptor antagonista
Cat. No.S1801
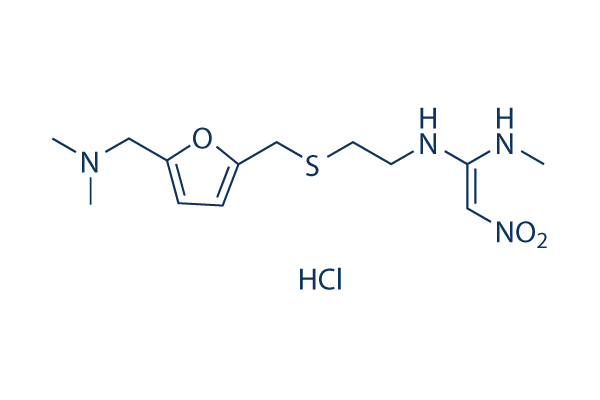
Estructura química
Peso molecular: 350.86
Control de calidad
- Citado en Nature Medicine por su máxima calidad
- COA
- NMR
- HPLC
- SDS
- Hoja de datos
| Dianas relacionadas | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Otros Histamine Receptor Inhibidores | GSK2879552 Dihydrochloride JNJ-7777120 Ebastine Ciproxifan Maleate Mianserin HCl Astemizole Lafutidine Mizolastine Rupatadine Fumarate Betahistine 2HCl |
Información química, almacenamiento y estabilidad
| Peso molecular | 350.86 | Fórmula | C13H22N4O3S.HCl |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 66357-59-3 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | AH19065 | Smiles | CNC(=C[N+](=O)[O-])NCCSCC1=CC=C(O1)CN(C)C.Cl | ||
Solubilidad
|
In vitro |
DMSO
: 70 mg/mL
(199.5 mM)
Water : 70 mg/mL Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
Histamine H2 receptor
|
|---|---|
| In vitro |
Ranitidine sensibiliza los hepatocitos a la destrucción por productos citotóxicos de neutrófilos activados, mientras que la Famotidine carece de esta capacidad. Ranitidine inhibe la producción del factor de necrosis tumoral alfa (TNF-alfa) en monocitos estimulados con lipopolisacárido in vitro. Ranitidine reduce la Kel de la morfina de forma dosis-dependiente con un efecto máximo del 50 %, y aumenta la concentración relativa de morfina-6-glucurónido a morfina-3-glucurónido en hepatocitos aislados de cobaya. Ranitidine disminuye gradualmente la relación morfina-3-glucurónido/morfina-6-glucurónido hasta en un 21 %.
|
| In vivo |
Ranitidine provoca daño hepático, como lo demuestra el aumento de las actividades séricas de alanina aminotransferasa, aspartato aminotransferasa y gamma-glutamil transferasa dentro de las 6 horas posteriores a la administración de Ranitidine en ratas. Ranitidine inhibe el aumento inducido por isquemia/reperfusión hepática en los niveles de TNF-alfa en el tejido hepático, el quimioatrayente de neutrófilos inducido por citocinas y la acumulación hepática de neutrófilos en ratas. El cotratamiento con Ranitidine mejora la coagulación inducida por LPS antes de la lesión hepática, y los anticoagulantes reducen el daño hepático en ratas tratadas con LPS/RAN. Las ratas tratadas con Ranitidine/LPS dan como resultado la formación de coágulos de fibrina en los sinusoides hepáticos, y la prevención de la deposición de fibrina asociada con una lesión hepatocelular reducida. El cotratamiento con Ranitidine mejora el aumento de TNF inducido por LPS antes del inicio de la lesión hepatocelular en ratas. Ranitidine muestra efectos ansiolíticos en el laberinto elevado en cruz, como lo indica un aumento del tiempo pasado en los brazos abiertos, un mayor escaneo de los brazos abiertos y más excursiones finales en ratas.
|
Referencias |
|
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT05399927 | Completed | Music Therapy|Cardiovascular Diseases|Critical Care|Emergencies |
Universidad Miguel Hernandez de Elche |
July 2015 | Not Applicable |
| NCT01539655 | Completed | Medullary Thyroid Cancer |
Sanofi |
February 2012 | Phase 1 |
| NCT01017198 | Completed | Advanced Solid Tumors |
Biogen |
November 2009 | Phase 1 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
