solo para uso en investigación
Sitagliptin DPP inhibidor
Cat. No.S5079
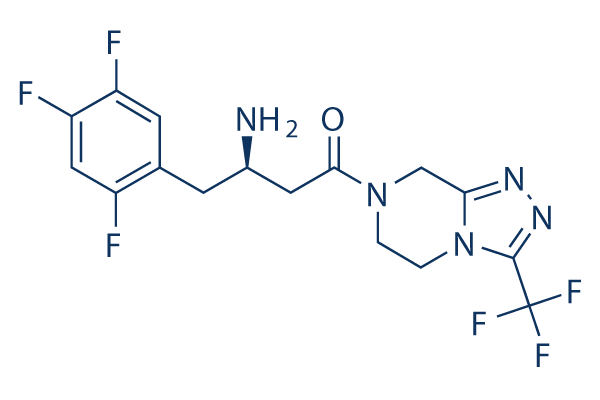
Estructura química
Peso molecular: 407.31
Control de calidad
Información química, almacenamiento y estabilidad
| Peso molecular | 407.31 | Fórmula | C16H15F6N5O |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 486460-32-6 | -- | Almacenamiento de soluciones madre |
|
|
| Sinónimos | MK-0431 | Smiles | C1CN2C(=NN=C2C(F)(F)F)CN1C(=O)CC(CC3=CC(=C(C=C3F)F)F)N | ||
Solubilidad
|
In vitro |
DMSO
: 81 mg/mL
(198.86 mM)
Ethanol : 81 mg/mL Water : 5 mg/mL (Ultrasonic and heating for 10 minutes, at 60℃.) |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
DPP-4
(Cell-free) 18 nM
|
|---|---|
| In vitro |
Sitagliptin exhibe un margen de selectividad > 2600 veces mayor frente a DPP8, DPP9 y otros miembros de la familia de la dipeptidil peptidasa (es decir, potencia frente a DPP-4 vs. DPP8/9). Este compuesto reduce la migración in vitro de células T CD4 esplénicas aisladas a través de una vía que involucra la activación de cAMP/PKA/Rac1. Ejerce una acción novedosa y directa para estimular la secreción de GLP-1 por la célula L intestinal a través de una vía independiente de DPP-4 y dependiente de la proteína quinasa A y MEK-ERK1/2. Por lo tanto, reduce el efecto de la autoinmunidad en la supervivencia del injerto.
|
| In vivo |
Sitagliptin se absorbe bien después de la administración oral con una biodisponibilidad del 87%. Tiene una vida media terminal aparente de 10 a 12 h a dosis de 25 a 100 mg y se excreta principalmente (≈ 80%) como compuesto inalterado por los riñones. Este compuesto no interfiere con las enzimas del citocromo P450 ni se han reportado interacciones significativas entre medicamentos. Se ha demostrado que inhibe la actividad de DPP-4 en > 90% dentro de 1-2 h de la administración. Tiene una vida media corta en ratones (1-2 h). El tratamiento crónico con sitagliptin en un modelo de ratón no genético de diabetes tipo 2 provoca una mejora significativa en el control glucémico. La mejora de la homeostasis de la glucosa se correlaciona con la restauración de la masa, la arquitectura y la capacidad de secreción de insulina de las células de los islotes (células α y β) en respuesta a la estimulación de la glucosa. Este compuesto prolonga la supervivencia del injerto de islotes en ratones NOD y en ratones inducidos por estreptozotocina. La administración in vivo de este químico reduce la migración de células T CD4+ de los ganglios linfáticos y el bazo, medida in vitro, a través de efectos mediados por incretinas y no incretinas, respectivamente, y las células T CD4+ esplénicas respondedoras a sDPP-IV y las células T CD4+ no respondedoras a incretinas de los ganglios linfáticos infiltraron selectivamente los islotes de ratones NOD diabéticos, después de la inyección en la vena de la cola. Suprimió significativamente la epileptogénesis en las convulsiones inducidas por PTZ (pentilentetrazol). Este compuesto contrarrestó el daño neuronal y todas las alteraciones bioquímicas e histoquímicas inducidas por PTZ. La sitagliptina oral puede promover la neurogénesis hipocampal, contrarrestar el estrés oxidativo hipocampal y prevenir el deterioro de la cognición en ratones.
|
Referencias |
|
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT05219409 | Not yet recruiting | Type 1 Diabetes |
University of Milan |
July 2023 | Phase 2|Phase 3 |
| NCT05403281 | Completed | Healthy Subjects |
Dong Wha Pharmaceutical Co. Ltd. |
November 5 2021 | Phase 1 |
| NCT03790839 | Completed | Patients |
Hua Medicine Limited |
January 31 2019 | Phase 1 |
| NCT03359590 | Completed | Pharmacological Action |
Profil Institut für Stoffwechselforschung GmbH|Merck Sharp & Dohme LLC |
March 21 2018 | Phase 2 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
