solo para uso en investigación
Diazoxide ADC Cytotoxin inhibidor
Cat. No.S4630
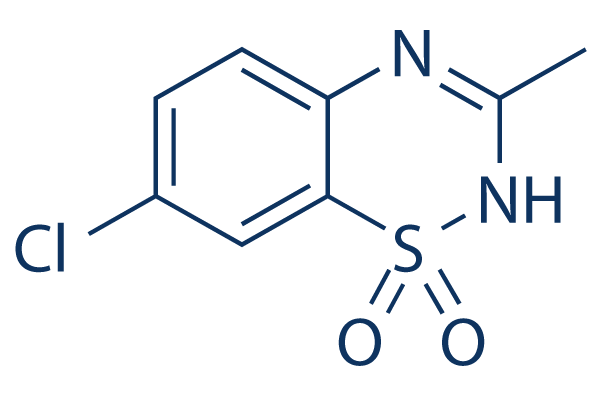
Estructura química
Peso molecular: 230.67
Control de calidad
| Dianas relacionadas | CFTR CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase |
|---|---|
| Otros ADC Cytotoxin Inhibidores | Triptolide SN-38 Luteolin (+)-Bicuculline Rutin Artemisinin BHQ Pinocembrin Harmine hydrochloride Luteoloside |
Información química, almacenamiento y estabilidad
| Peso molecular | 230.67 | Fórmula | C8H7ClN2O2S |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 364-98-7 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | Sch-6783, SRG-95213 | Smiles | CC1=NS(=O)(=O)C2=C(N1)C=CC(=C2)Cl | ||
Solubilidad
|
In vitro |
DMSO
: 46 mg/mL
(199.41 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
KATP channels
|
|---|---|
| In vitro |
Diazoxide inhibe la actividad inflamatoria microglial. Este tratamiento compuesto inhibe parcialmente el patrón inflamatorio inducido por LPS/IFN-γ en células microgliales, induciendo una disminución en la producción de NO que podría deberse a la disminución de la expresión de iNOS detectada. No tiene efecto sobre la fagocitosis microglial.
|
| In vivo |
Diazoxide es beneficioso para la mejora en tareas cognitivas, la reducción de la ansiedad, la disminución en la acumulación de oligómeros de amiloide-beta y la hiperfosforilación de proteínas tau. Este compuesto también puede ejercer efectos neuroprotectores independientemente de la activación del canal K+ al disminuir la excitabilidad neuronal y la activación de los receptores de N-metil-D-aspartato (NMDA) o al aumentar las corrientes a través de los receptores de ácido α-amino-3-hidroxi-5-metil-4-isoxazolpropiónico (AMPA). Los animales tratados con este químico muestran una disminución en la gravedad de la enfermedad unos días después de la observación de los primeros signos clínicos, lo que corresponde a la fase inflamatoria aguda de la enfermedad. La administración oral diaria de este compuesto en ratones EAE durante la fase efectora de la enfermedad reduce la gravedad de los signos clínicos sin ningún efecto adverso aparente. Disminuye la desmielinización y la pérdida axonal, reduce el daño tisular, inhibe la activación microglial/macrofágica y astrocítica y preserva la integridad neuronal. No se observan efectos sobre el número de linfocitos B y T que infiltran la médula espinal.
|
Referencias |
|
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT03941236 | Active not recruiting | Congenital Hyperinsulinism |
Zealand Pharma |
May 1 2019 | Phase 3 |
| NCT00901823 | Withdrawn | Hypertriglyceridemia |
Essentialis Inc. |
March 2011 | Phase 1 |
| NCT00696475 | Completed | Hypertriglyceridemia |
Essentialis Inc.|Medpace Inc. |
June 2008 | Phase 2 |
| NCT00688857 | Completed | Hypertriglyceridemia |
Essentialis Inc.|Cetero Research San Antonio |
May 2008 | Phase 1 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
