solo para uso en investigación
Bosentan Hydrate Endothelin Receptor antagonista
Cat. No.S3051
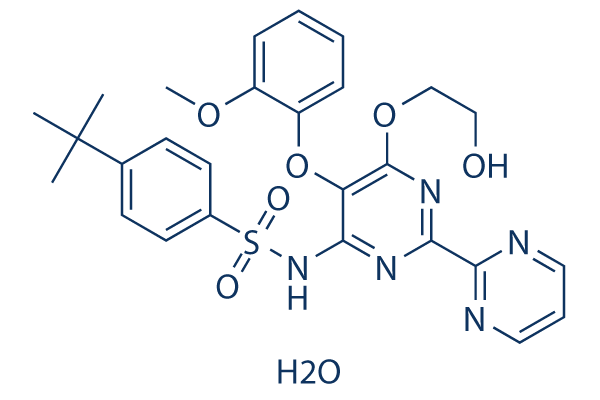
Estructura química
Peso molecular: 569.63
Control de calidad
| Dianas relacionadas | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| Otros Endothelin Receptor Inhibidores | BQ-123 Zibotentan (ZD4054) Sparsentan (PS-433540, RE-021) Carperitide Acetate Lu-135252 Pearl Extract Aprocitentan Atrasentan |
Información química, almacenamiento y estabilidad
| Peso molecular | 569.63 | Fórmula | C27H29N5O6S.H2O |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 157212-55-0 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | Ro 47-0203 | Smiles | CC(C)(C)C1=CC=C(C=C1)S(=O)(=O)NC2=C(C(=NC(=N2)C3=NC=CC=N3)OCCO)OC4=CC=CC=C4OC.O | ||
Solubilidad
|
In vitro |
DMSO
: 100 mg/mL
(175.55 mM)
Ethanol : 2 mg/mL Water : 0.001 mg/mL |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
ET-A
4.7 nM(Ki)
ET-B
95 nM(Ki)
|
|---|---|
| In vitro |
Bosentan antagoniza competitivamente la unión específica de ET-1 marcado con [125 I] en células de músculo liso humano (receptores ET-A) y placenta humana (receptores ET-B). Bosentan también inhibe la unión de ligandos selectivos de ET-B en tráquea porcina. Las contracciones inducidas por ET-1 en aorta aislada de rata (ET-A) y por el agonista selectivo de ET-B sarafotoxina S6C en tráquea de rata son inhibidas competitivamente por Bosentan (pA2= 7,2 y 6,0, respectivamente), al igual que la relajación dependiente del endotelio a sarafotoxina S6C en la arteria mesentérica superior de conejo (pA2= 6,7). La unión de otros 40 péptidos, prostaglandinas, iones y neurotransmisores no se ve significativamente afectada por Bosentan, lo que demuestra su especificidad por los receptores ET.
|
| In vivo |
Bosentan inhibe la respuesta presora a big ET-1 tanto después de la administración i.v. como oral, con una larga duración de acción y sin actividad agonista intrínseca. Bosentan también inhibe el efecto depresor y presor de ET-1 y sarafotoxina S6C. Su perfil farmacológico convierte a Bosentan en un fármaco potencialmente útil en el manejo de trastornos clínicos asociados con la vasoconstricción. Bosentan es el primer antagonista oral no peptídico mixto de los receptores ETA/B. El tratamiento a largo plazo con Bosentan ha aumentado notablemente la supervivencia, la hemodinámica y la remodelación cardíaca en ratas con insuficiencia cardíaca congestiva (ICC). Bosentan disminuye la PA arterial en un grado similar al de un inhibidor de la enzima convertidora de angiotensina (ECA). La administración de Bosentan en ratas con ICC después de un IM agudo disminuye significativamente la PA arterial y tiene un efecto aditivo al de un inhibidor de la ECA. El tratamiento agudo y crónico con Bosentan también mejora la hemodinámica sistémica y pulmonar mediante una disminución de la resistencia vascular periférica y pulmonar, y un aumento del gasto cardíaco en pacientes con ICC.
|
Referencias |
|
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT05072106 | Unknown status | Advanced Solid Tumor |
PharmaMar |
January 14 2021 | Phase 1 |
| NCT04991207 | Completed | Pulmonary Arterial Hypertension |
Bial - Portela C S.A. |
February 6 2018 | Phase 1 |
| NCT01929213 | Unknown status | Healthy Volunteers |
Dong-A Pharmaceutical Co. Ltd.|Dong-A ST Co. Ltd. |
August 2013 | Phase 1 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
