solo para uso en investigación
Rivaroxaban Factor Xa inhibidor
Cat. No.S3002
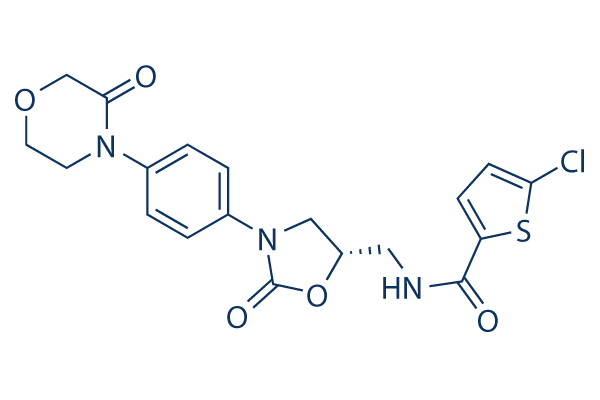
Estructura química
Peso molecular: 435.88
Control de calidad
| Dianas relacionadas | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Otros Factor Xa Inhibidores | Asundexian |
Información química, almacenamiento y estabilidad
| Peso molecular | 435.88 | Fórmula | C19H18ClN3O5S |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 366789-02-8 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | BAY 59-7939 | Smiles | C1COCC(=O)N1C2=CC=C(C=C2)N3CC(OC3=O)CNC(=O)C4=CC=C(S4)Cl | ||
Solubilidad
|
In vitro |
DMSO
: 87 mg/mL
(199.59 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
Factor Xa
(Cell-free assay) 0.7 nM
Prothrombinase
(Cell-free assay) 2.1 nM
|
|---|---|
| In vitro |
Rivaroxaban es un inhibidor oral directo del Factor Xa (FXa), que se está desarrollando para la prevención y el tratamiento de la trombosis arterial y venosa con un Ki de 0,4 nM. Este compuesto también inhibe la actividad de la protrombinasa con una IC50 de 2,1 nM. También muestra una afinidad similar por el FXa humano y de conejo purificados (IC50 0,7 nM y 0,8 nM, respectivamente), pero una menor potencia contra el FXa de rata purificado (IC50 3,4 nM). El FXa humano y de conejo endógeno en plasma es inhibido en una medida similar por este químico (IC50 21 nM y 21 nM, respectivamente), mientras que se requieren concentraciones 14 veces más altas en plasma de rata (IC50 290 nM). Exhibe alta permeabilidad y transporte polarizado a través de células Caco-2 como sustrato de la P-gp, pero no muestra ningún efecto inhibidor sobre el transporte de fármacos mediado por la P-gp hasta concentraciones de 100 μM in vitro.
|
| Ensayo de quinasa |
Actividad del Factor Xa
|
|
La actividad de Rivaroxaban contra serina proteasas purificadas se mide utilizando sustratos cromogénicos o fluorogénicos en microplacas de 96 pocillos. Las enzimas se incuban con este compuesto o su solvente, dimetil sulfóxido (DMSO), durante 10 minutos. Las reacciones se inician mediante la adición del sustrato, y el color o la fluorescencia se monitoriza continuamente a 405 nm utilizando un lector Spectra Rainbow Thermo, o a 630/465 nm utilizando un SPECTRAfluor plus, respectivamente, durante 20 minutos. La actividad enzimática se analiza en los siguientes tampones (concentraciones finales): FXa humano (0,5 nM), FXa de conejo (2 nM), FXa de rata (10 nM), o urocinasa (4 nM) en tampón Tris–HCl 50 mM pH 8,3, 150 mM NaCl y 0,1% de albúmina sérica bovina (BSA); Pefachrome FXa (50–800 μM) o cromozima U (250 μM) con trombina (0,69 nM), tripsina (2,2 nM) o plasmina (3,2 nM) en 0,1 μM Tris–HCl, pH 8,0, y 20 mM CaCl2; cromozima TH (200 μM), cromozima plasmina (500 μM) o cromozima tripsina (500 μM) con FXIa (1 nM) o APC (10 nM) en tampón fosfato 50 mM, pH 7,4, 150 mM NaCl; y S 2366 (150 o 500 μM) con FVIIa (1 nM) y factor tisular (3 nM) en tampón Tris–HCl 50 mM, pH 8,0, 100 mM NaCl, 5 mM CaCl2 y 0,3% BSA, H-D-Phe-Pro-Arg-6-amino-1-naftaleno-bencil-sulfonamida-H2O (100 μM) y se mide durante 3 horas. El ensayo FIXaβ/FX, que comprende FIXaβ (8,8 nM) y FX (9,5 nM) en tampón Tris–HCl 50 mM, pH 7,4, 100 mM NaCl, 5 mM CaCl2 y 0,1% BSA, se inicia con la adición de I-1100 (50 μM) y se mide durante 60 minutos. La constante inhibidora (Ki) contra el FXa se calcula según la ecuación de Cheng–Prusoff. La IC50 es la cantidad de inhibidor requerida para disminuir la velocidad inicial del control en un 50 %.
|
|
| In vivo |
Rivaroxaban reduce la trombosis venosa de forma dosis-dependiente (ED50 0,1 mg/kg i.v.) en un modelo de estasis venosa en ratas. Este compuesto reduce la formación de trombos arteriales en un shunt arteriovenoso (AV) en ratas (ED50 5,0 mg/kg p.o.) y conejos (ED50 0,6 mg/kg p.o.). La farmacocinética plasmática de este compuesto químico es lineal en el rango de dosis investigado (1-10 mg/kg en ratas, 0,3-3 mg/kg en perros). El aclaramiento plasmático es bajo: 0,4 L/kg/h en ratas y 0,3 L/kg/h en perros; el volumen de distribución (V(ss)) es moderado: 0,3 L/kg en ratas y 0,4 L/kg en perros. La vida media de eliminación después de la administración oral es corta en ambas especies (0,9-2,3 horas).
|
Referencias |
|
Información del ensayo clínico
(datos de https://clinicaltrials.gov, actualizado el 2024-05-22)
| Número NCT | Reclutamiento | Condiciones | Patrocinador/Colaboradores | Fecha de inicio | Fases |
|---|---|---|---|---|---|
| NCT06193863 | Not yet recruiting | Prevention of Venous Thromboembolism|Congenital Heart Disease|Fontan Procedure|Children |
Bayer|Janssen Research & Development LLC |
May 31 2024 | -- |
| NCT06195540 | Not yet recruiting | Venous Thromboembolism|Deep Vein Thrombosis|Pulmonary Embolism|Lower Limb Trauma|Thromboprophylaxis|Immobilisation |
University Hospital Angers |
May 31 2024 | Phase 3 |
| NCT06314763 | Completed | Drug Drug Interaction Study |
Radboud University Medical Center|Amgen |
November 9 2023 | Phase 4 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
