solo para uso en investigación
Chelerythrine Chloride (NSC 646662) PKC inhibidor
Cat. No.S1292
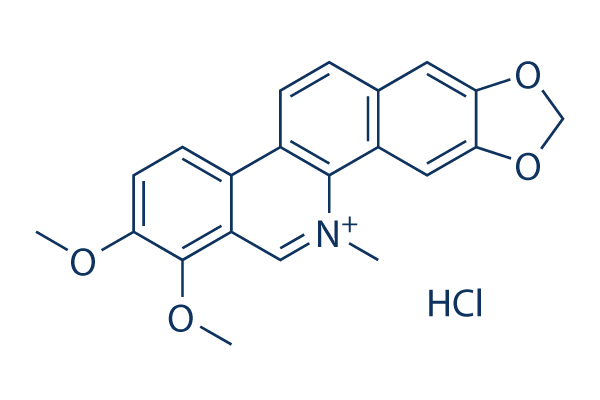
Estructura química
Peso molecular: 384.83
Control de calidad
Información química, almacenamiento y estabilidad
| Peso molecular | 384.83 | Fórmula | C21H18NO4.HCl |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 3895-92-9 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | Broussonpapyrine chloride | Smiles | C[N+]1=C2C(=C3C=CC(=C(C3=C1)OC)OC)C=CC4=CC5=C(C=C42)OCO5.[Cl-] | ||
Solubilidad
|
In vitro |
DMSO
: 3 mg/mL
(7.79 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Características |
Chelerythrine is at least 100-fold more selective for PKCs than for other kinases.
|
|---|---|
| Targets/IC50/Ki |
PKC
(Cell-free assay) 0.66 μM
|
| In vitro |
El cloruro de cheleritrina (NSC 646662) interactúa con el dominio catalítico de la PKC, es un inhibidor competitivo con respecto al aceptor de fosfato (histona IIIS) con un valor de Ki de 0,7 μM y un inhibidor no competitivo con respecto al ATP. Muestra potentes efectos citotóxicos contra las células L-1210 con una IC50 de 0,53 μM. Este compuesto no altera ninguna actividad de PKA, TPK y Ca/CM-PK, y su efecto inhibidor sobre la actividad de la PKC no varía entre los diversos sustratos, incluidos GS, MLC, MBP y Fibrinógeno. Inhibe la actividad de la PKC en extractos celulares crudos de células SQ-20B de manera dosis-dependiente. La cheleritrina disminuye la viabilidad celular, según lo determinado por el ensayo MTT, de manera dosis-dependiente en las células SCC35, JSQ3, SQ20B y SCC61. A 5 μM, suprime la expresión inducida por VEGF de ICAM-1, VCAM-1 y E-selectina en HUVECs. También suprime la actividad de NF-κB inducida por VEGF en HUVECs a la misma concentración y suprime la adhesividad leucocitaria basal e inducida por VEGF en HUVECs. A concentraciones de 6 mM-30 mM, induce rápidamente picnosis, encogimiento y posterior muerte celular en miocitos cardíacos. La muerte de miocitos inducida por cheleritrina (30 μM) se acompaña de fragmentación nuclear y activación de caspasa-3 y -9 en el cultivo primario de miocitos ventriculares de rata neonatal. A 10 μM, provoca la liberación de citocromo c de las mitocondrias, lo que sugiere que las ROS median la liberación de citocromo c inducida por cheleritrina en los miocitos cardíacos. Desplaza el péptido del dominio BH3 marcado fluorescentemente de una proteína de fusión recombinante GST-BcLXL con una IC50 de 1,5 μM. A 2,5 μM y 5 μM durante 16 horas, induce una disminución sustancial del potencial mitocondrial, como lo indica un aumento de la fluorescencia verde de JC-1 en células de neuroblastoma humano SH-SY5Y. A 5 μM, también induce la aparición de ADN sub-G1, lo que es indicativo de apoptosis en células SH-SY5Y. A 10 μM, induce un cambio en el potencial mitocondrial y la liberación de CytC de las mitocondrias en células SH-SY5Y. |
| Ensayo de quinasa |
ensayo para la proteína quinasa C
|
|
La proteína quinasa C purificada se prepara a partir de cerebro de rata. Brevemente, la mezcla de incubación (200 μL) contiene 20 mM de tampón Tris/HCl (pH 7,5), 10 mM de MgCl2, 200 μg/mL de histonas, micelas preparadas con 700 μM de fosfatidilserina y 180 μM de 1,2-dioleína en 0,3% de triton X100, 0,2 mM de CaCl2, 100 μM de ATP, [γ-32P ]-ATP (105 dpm), Chelerythrine Chloride (NSC 646662) a probar (solubilizado en dimetilsulfóxido) y la enzima (0,5 μg de proteína). Después de la incubación a 30°C durante 3 minutos, la reacción se termina con la adición de 3 mL de ácido tricloroacético al 20%. Los materiales precipitables con ácido se recogen en filtros Whatman GFE y se lavan extensamente con ácido tricloroacético al 20% helado. La radioactividad en los filtros se mide usando un contador de centelleo líquido. La actividad de la proteína quinasa C se corrige para la actividad no específica mediante el ensayo en ausencia de micelas y CaCl2.
|
|
| In vivo |
El cloruro de cheleritrina (NSC 646662) (5 mg/kg i.p.) provoca un retraso en el crecimiento tumoral en ratones con xenoinjertos SQ-20B. El tratamiento con este compuesto (5 mg/kg) aumenta significativamente los núcleos TUNEL-positivos en el miocardio, así como las formas clivadas de caspasa-3 y -9 en ratas adultas. |
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
