solo para uso en investigación
WHI-P154 JAK inhibidor
Cat. No.S2867
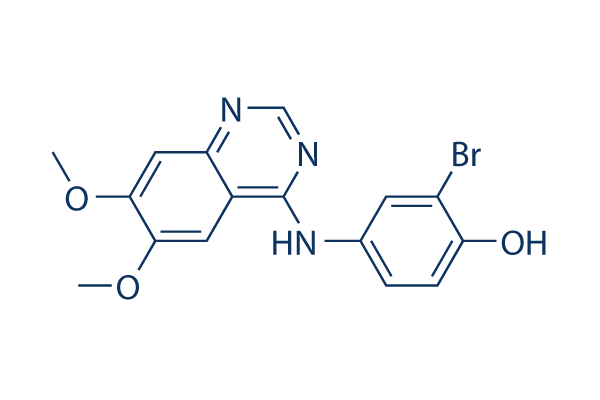
Estructura química
Peso molecular: 376.2
Control de calidad
- Citado en Nature Medicine por su máxima calidad
- COA
- NMR
- SDS
- Hoja de datos
| Dianas relacionadas | EGFR STAT Pim |
|---|---|
| Otros JAK Inhibidores | BMS-986165 (Deucravacitinib) AZD1480 WP1066 Momelotinib (CYT387) Filgotinib (GLPG0634) AT9283 Gandotinib (LY2784544) Pacritinib TG101209 Cerdulatinib (PRT062070) hydrochloride |
Información química, almacenamiento y estabilidad
| Peso molecular | 376.2 | Fórmula | C16H14BrN3O3 |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 211555-04-3 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | N/A | Smiles | COC1=C(C=C2C(=C1)C(=NC=N2)NC3=CC(=C(C=C3)O)Br)OC | ||
Solubilidad
|
In vitro |
DMSO
: 75 mg/mL
(199.36 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
EGFR
4 nM
VEGFR
100 nM
Src
100 nM
JAK3
1.8 μM
|
|---|---|
| In vitro |
WHI-P154 se describe por primera vez como un inhibidor de JAK3 que no muestra actividad en JAK1 o JAK2. Este compuesto inhibe la activación de STAT1, la expresión de iNOS y la producción de NO en macrófagos in vitro. Pero se ha demostrado que este químico también inhibe otras quinasas comunes, incluyendo EGFR, Src, Abl, VEGFR, MAPK y PI3-K, e induce apoptosis en líneas celulares de glioblastoma humano. Inhibe la adhesión y migración de células de glioblastoma en el contexto de la MEC. Este compuesto exhibe una citotoxicidad significativa contra las líneas celulares de glioblastoma humano U373 y U87, causando la muerte celular apoptótica a concentraciones micromolares. La actividad antiglioblastoma in vitro de este químico se amplifica > 200 veces y se vuelve selectiva por conjugación con el factor de crecimiento epidérmico humano recombinante (EGF). El tratamiento in vitro con EGF-P154 resulta en la muerte de células de glioblastoma a concentraciones nanomolares con una IC50 de 813 nM, mientras que no se observa citotoxicidad contra las células de leucemia negativas para EGF-R, incluso a concentraciones tan altas como 100 mM.
|
| Ensayo de quinasa |
Ensayos de quinasas
|
|
WHI-P154 se prueba en ensayos de quinasas. El panel de quinasas se selecciona para cubrir ampliamente el quinoma, proporcionando una buena aproximación de la especificidad. Para todas las quinasas, se utilizan proteínas de fusión de dominio de quinasa GST o de longitud completa, recombinantes de rata (IKKβ) o humanas (todas las demás). Este compuesto es inactivo (concentración que inhibe la respuesta en un 50% [IC50] > 30 μM) para las siguientes quinasas: AKT, AuroraA, cdk2, cdk6, CHK1, FGFR1, GSK3b, IKKb, IKKi, INSR, MAPK1, MAPKAP-K2, MASK, MET, PAK4, PDK1, PKCb, ROCK1, TaoK3, TrkA.
|
|
| In vivo |
La administración in vivo de EGF-P154 resulta en un retraso en la progresión tumoral y una mejora en la supervivencia libre de tumores en un modelo de xenoinjerto de glioblastoma de ratón inmunodeficiente combinado severo. Mientras que ninguna de las ratones de control permanece viva libre de tumores más allá de los 33 días (supervivencia mediana libre de tumores, 19 días) y todas las ratones de control tienen tumores que progresan rápidamente hasta alcanzar un tamaño promedio de > 500 mm3 a los 58 días, el 40% de las ratones tratadas durante 10 días consecutivos con 1 mg/kg/día de este compuesto permanecen vivas y libres de tumores detectables durante más de 58 días con una supervivencia mediana libre de tumores de 40 días. Los tumores que se desarrollan en el 60% restante de las ratones nunca alcanzan un tamaño > 50 mm3.
|
Referencias |
|
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
