solo para uso en investigación
OSU-03012 (AR-12) PDPK1 inhibidor
Cat. No.S1106
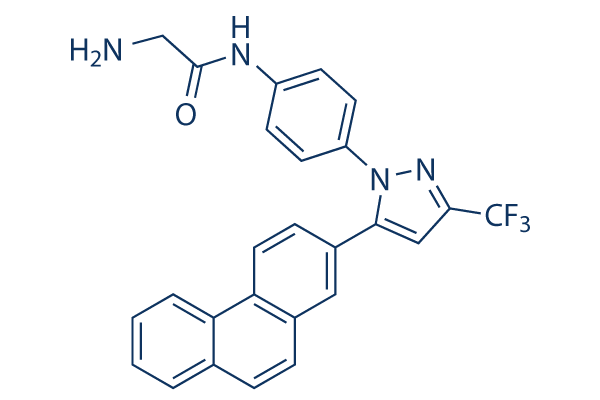
Estructura química
Peso molecular: 460.45
Control de calidad
Cultivo celular, tratamiento y concentración de trabajo
| Líneas celulares | Tipo de ensayo | Concentración | Tiempo de incubación | Formulación | Descripción de la actividad | PMID |
|---|---|---|---|---|---|---|
| mouse RAW264.7 cells | Function assay | 8 h | Antimicrobial activity against Salmonella enterica serovar Typhimurium ATCC 14028 infected in mouse RAW264.7 cells assessed as inhibition of intracellular bacterial growth after 8 hrs, IC50=0.2 μM | |||
| mouse RAW264.7 cells | Cytotoxic assay | 24 h | Cytotoxicity against mouse RAW264.7 cells assessed as cell viability after 24 hrs by MTT assay, IC50=10 μM | |||
| Haga clic para ver más datos experimentales de líneas celulares | ||||||
Información química, almacenamiento y estabilidad
| Peso molecular | 460.45 | Fórmula | C26H19F3N4O |
Almacenamiento (Desde la fecha de recepción) | |
|---|---|---|---|---|---|
| Nº CAS | 742112-33-0 | Descargar SDF | Almacenamiento de soluciones madre |
|
|
| Sinónimos | N/A | Smiles | C1=CC=C2C(=C1)C=CC3=C2C=CC(=C3)C4=CC(=NN4C5=CC=C(C=C5)NC(=O)CN)C(F)(F)F | ||
Solubilidad
|
In vitro |
DMSO
: 11 mg/mL
(23.88 mM)
Water : Insoluble Ethanol : Insoluble |
Calculadora de Molaridad
|
In vivo |
|||||
Calculadora de formulación in vivo (Solución clara)
Paso 1: Introduzca la información a continuación (Recomendado: Un animal adicional para tener en cuenta la pérdida durante el experimento)
Paso 2: Introduzca la formulación in vivo (Esto es solo la calculadora, no la formulación. Por favor, contáctenos primero si no hay una formulación in vivo en la sección de Solubilidad.)
Resultados del cálculo:
Concentración de trabajo: mg/ml;
Método para preparar el líquido maestro de DMSO: mg fármaco predissuelto en μL DMSO ( Concentración del líquido maestro mg/mL, Por favor, contáctenos primero si la concentración excede la solubilidad del DMSO del lote del fármaco. )
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadirμL PEG300, mezclar y clarificar, luego añadirμL Tween 80, mezclar y clarificar, luego añadir μL ddH2O, mezclar y clarificar.
Método para preparar la formulación in vivo: Tomar μL DMSO líquido maestro, luego añadir μL Aceite de maíz, mezclar y clarificar.
Nota: 1. Por favor, asegúrese de que el líquido esté claro antes de añadir el siguiente disolvente.
2. Asegúrese de añadir el (los) disolvente(s) en orden. Debe asegurarse de que la solución obtenida, en la adición anterior, sea una solución clara antes de proceder a añadir el siguiente disolvente. Se pueden utilizar métodos físicos como el vórtice, el ultrasonido o el baño de agua caliente para ayudar a la disolución.
Mecanismo de acción
| Targets/IC50/Ki |
PDPK1
(Cell-free assay) 5 μM
|
|---|---|
| In vitro |
OSU-03012 (AR-12) induce la muerte apoptótica en células PC-3 con una IC50 de 5 µM y reduce la actividad de la p70S6K inmunoprecipitada. Suprime completamente el crecimiento celular en una amplia gama de líneas celulares tumorales a concentraciones de 3–5 μm, en comparación con la concentración de al menos 50 μm. Este compuesto promueve la muerte celular en mayor medida en células de glioma que en astrocitos no transformados. Causa una inducción dosis-dependiente de la muerte celular que no se altera por la mutación p53, la expresión de ERBB1 VIII, o la pérdida de la función de la fosfatasa y la tensina debido a una deleción homóloga en el cromosoma 10. OSU-03012 y la radiación ionizante causan una elevación aditiva e independiente de caspasas en la muerte celular. Su letalidad como agente único o cuando se combina con moduladores de señalización no se modifica en células que carecen de expresión de BIM o de BAX/BAK. Promueve la liberación de catepsina B del compartimento lisosomal y de AIF de las mitocondrias. La letalidad de este compuesto se atenúa en células con deficiencia de proteína quinasa R-like endoplasmic reticulum kinase-/-, lo que se correlacionó con la reducción de la escisión de BID y la supresión de la liberación de catepsina B y AIF en el citosol. Inhibe la proliferación y migración de células de cáncer de tiroides (células NPA, WRO y ARO) e induce la apoptosis, lo que resulta en un aumento de células en fase S sin un aumento de células en G2. OSU-03012 es un inhibidor competitivo de ATP de la actividad de PAK y suprime la fosforilación de AKT en células de cáncer de tiroides. Inhibe el crecimiento celular de líneas celulares de carcinoma hepatocelular, incluidas las células Huh7, Hep3B y HepG2, con valores de IC50 inferiores a 1 μM. Este compuesto no suprime la actividad de PDK1 o AKT ni induce la apoptosis celular, pero induce la autofagia en las células Huh7. Además, se detecta una acumulación de especies reactivas de oxígeno (ROS) después de su tratamiento. Un estudio reciente muestra que podría mejorar la susceptibilidad de las líneas celulares mutantes (Bcr)-Abl a la apoptosis inducida. |
| Ensayo de quinasa |
Ensayo de la quinasa PDK-1
|
|
Este ensayo in vitro se realiza utilizando un kit de ensayo de la quinasa PDK-1. Este ensayo sin células se basa en la capacidad de la PDK-1 recombinante, en presencia de vehículo DMSO o OSU-03012 (AR-12), para activar su quinasa regulada por suero y glucocorticoides corriente abajo que, a su vez, fosforila el sustrato peptídico específico de la quinasa Akt/suero y regulada por glucocorticoides RPRAATF con [γ-32P]ATP. El sustrato peptídico 32P-fosforilado se separa luego del [γ-32P]-ATP residual utilizando papel de fosfocelulosa P81 y se cuantifica en un contador de centelleo después de tres lavados con ácido fosfórico al 0,75 %.
|
|
| In vivo |
OSU-03012 (AR-12) suprime el crecimiento tumoral en un 57,59 % y aumenta la LC3 escindida en xenoinjertos tumorales de Huh7 a 200 mg/kg. Este compuesto disminuye notablemente la expresión de la proteína EGFR en los tumores en un 48 % en comparación con los controles de vehículo y también evita que YB-1 se una al promotor de EGFR en xenoinjertos MDA-MB-435/LCC6. Es bien tolerado e inhibe el crecimiento de xenoinjertos de schwannoma HMS-97 en un 55 % después de la administración oral. |
Referencias |
|
Aplicaciones
| Métodos | Biomarcadores | Imágenes | PMID |
|---|---|---|---|
| Western blot | p-Akt / Akt |

|
18413750 |
| Growth inhibition assay | Cell viability |
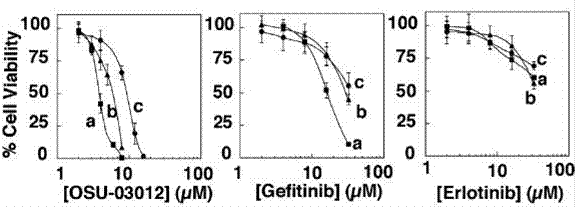
|
18413750 |
Soporte técnico
Tel: +1-832-582-8158 Ext:3
Si tiene alguna otra consulta, por favor deje un mensaje.
