réservé à la recherche
TAS-102 (Trifluridine/Tipiracil Hydrochloride Mixture) Agent Antitumoral Nucléosidique
N° Cat.S8539
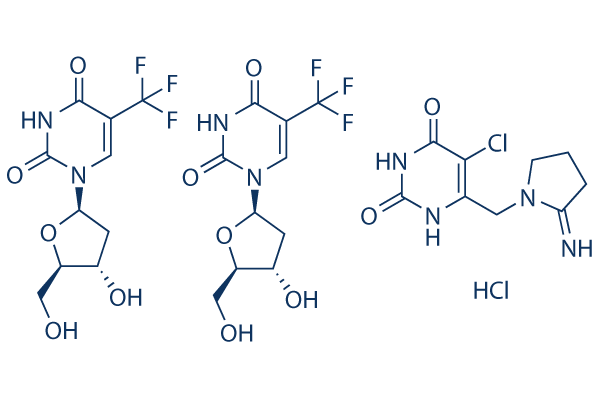
Structure chimique
Poids moléculaire: 435.76
Contrôle qualité
| Cibles apparentées | HDAC PARP ATM/ATR DNA-PK WRN DNA/RNA Synthesis Topoisomerase PPAR Sirtuin Casein Kinase |
|---|---|
| Autre Thymidylate Synthase Inhibiteurs | Raltitrexed |
Informations chimiques, stockage et stabilité
| Poids moléculaire | 435.76 | Formule | C10H11F3N2O5.0.5C9H11ClN4O2.0.5HCl |
Stockage (À partir de la date de réception) | |
|---|---|---|---|---|---|
| N° CAS | 733030-01-8 | Télécharger le SDF | Stockage des solutions mères |
|
|
| Synonymes | Trifluridine-Tipiracil Hydrochloride Mixture | Smiles | Cl.OCC1OC(CC1O)N2C=C(C(=O)NC2=O)C(F)(F)F.OCC3OC(CC3O)N4C=C(C(=O)NC4=O)C(F)(F)F.ClC5=C(CN6CCCC6=N)NC(=O)NC5=O | ||
Solubilité
|
In vitro |
DMSO
: 87 mg/mL
(199.65 mM)
Water : 29 mg/mL Ethanol : Insoluble |
Calculateur de molarité
|
In vivo |
|||||
Calculateur de formulation in vivo (Solution claire)
Étape 1 : Entrez les informations ci-dessous (Recommandé : Un animal supplémentaire pour tenir compte des pertes pendant lexpérience)
Étape 2 : Entrez la formulation in vivo (Ceci nest que le calculateur, pas la formulation. Veuillez nous contacter dabord sil ny a pas de formulation in vivo dans la section Solubilité.)
Résultats du calcul :
Concentration de travail : mg/ml;
Méthode de préparation du liquide maître DMSO : mg médicament prédissous dans μL DMSO ( Concentration du liquide maître mg/mL, Veuillez nous contacter dabord si la concentration dépasse la solubilité du DMSO du lot de médicament. )
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuiteμL PEG300, mélanger et clarifier, ajouter ensuiteμL Tween 80, mélanger et clarifier, ajouter ensuite μL ddH2O, mélanger et clarifier.
Méthode de préparation de la formulation in vivo : Prendre μL DMSO liquide maître, ajouter ensuite μL Huile de maïs, mélanger et clarifier.
Remarque : 1. Assurez-vous que le liquide est clair avant dajouter le solvant suivant.
2. Assurez-vous dajouter le(s) solvant(s) dans lordre. Vous devez vous assurer que la solution obtenue lors de lajout précédent est une solution claire avant de procéder à lajout du solvant suivant. Des méthodes physiques telles que le vortex, les ultrasons ou le bain-marie peuvent être utilisées pour faciliter la dissolution.
Mécanisme daction
| In vitro |
TAS-102 est un médicament combiné oral composé de trifluridine (FTD), qui est un analogue nucléosidique à base de thymidine, et de chlorhydrate de tipiracil (TPI), qui améliore la biodisponibilité du FTD en inhibant son catabolisme par la thymidine phosphorylase (TP). La forme phosphorylée de la trifluridine est incorporée dans l'ADN, entraînant une dysfonction de l'ADN et un arrêt du cycle cellulaire. L'inhibiteur de la thymidine phosphorylase inhibe la dégradation du FTD et inhibe l'angiogenèse. Ainsi, ce traitement composé entraîne une incorporation massive de trifluridine dans l'ADN et une activation de voies de réponse aux dommages de l'ADN similaires, qui impliquent la phosphorylation de Chk1 et l'arrêt du cycle pendant la phase G2/M. |
|---|---|
| In vivo |
La demi-vie d'élimination du FTD après administration intraveineuse chez l'homme est très rapide (18 minutes), en raison de la dégradation rapide du FTD en son métabolite majeur, le 5-trifluorométhyl-2,4(1H,3H)-pyrimidinedione. Chez les singes, le niveau plasmatique de FTD après administration orale seule est très faible, suggérant un métabolisme de premier passage étendu par la TPase hépatique et intestinale. Cependant, l'ajout de TPI (chlorhydrate de tipiracil) permet l'administration orale. En inhibant la TP, le TPI inhibe la dégradation du FTD dans le foie et les intestins après administration orale et améliore ainsi sa biodisponibilité. L'enzyme TP catalyse la phosphorolyse des 2'-désoxynucléosides de pyrimidine tels que le FTD. Des études utilisant des xénogreffes tumorales de CCR humain chez des souris déterminent que l'activité antitumorale maximale est atteinte avec un rapport molaire de 1:0,5, et des études chez des souris et des singes montrent que la concentration plasmatique maximale de FTD est presque atteinte avec le même rapport. De plus, ce rapport produit un équilibre favorable entre l'activité antitumorale et la toxicité. Une toxicité plus faible chez les souris est observée avec la co-administration de TPI qu'avec le FTD seul. Ce composé peut surmonter la résistance acquise au 5-FU car le mécanisme principal de cette substance chimique n'est pas associé aux principales enzymes métaboliques du 5-FU, telles que TS et OPRT. Il a démontré son efficacité dans les cancers réfractaires au 5-FU. |
Références |
|
Informations sur lessai clinique
(données de https://clinicaltrials.gov, mis à jour le 2024-05-22)
| Numéro NCT | Recrutement | Conditions | Sponsor/Collaborateurs | Date de début | Phases |
|---|---|---|---|---|---|
| NCT06039202 | Not yet recruiting | Metastatic Colorectal Cancer |
Holy Stone Healthcare Co. Ltd |
January 2024 | Phase 2 |
| NCT05343013 | Recruiting | Colorectal Cancer |
M.D. Anderson Cancer Center|Taiho |
June 6 2022 | Phase 2 |
| NCT04868773 | Active not recruiting | Colorectal Cancer|Colorectal Carcinoma|Metastatic Cancer|CRC |
University of California Irvine |
July 16 2021 | Phase 1 |
| NCT04074343 | Completed | Gastric Adenocarcinoma|GastroEsophageal Cancer |
University of California Irvine|Taiho Pharmaceutical Co. Ltd. |
August 26 2019 | Phase 1 |
Support technique
Tel: +1-832-582-8158 Ext:3
Si vous avez dautres questions, veuillez laisser un message.
