Datos técnicos
| Fórmula | C23H24O8 |
||||||
| Peso molecular | 428.43 | Número CAS | 19545-26-7 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 85 mg/mL (198.39 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | La Wortmannina es el primer inhibidor de PI3K descrito con una IC50 de 3 nM en un ensayo sin células, con poca selectividad dentro de la familia PI3K. La Wortmannina bloquea la formación de autofagosomas e inhibe potentemente DNA-PK/ATM con una IC50 de 16 nM y 150 nM en ensayos sin células. La Wortmannina también inhibe la actividad de PLK1. | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
||||||||
| In vitro | La inhibición de MLCK por Wortmannina no se ve afectada por la calmodulina ni el substrato peptídico, mientras que se reduce por una alta concentración de ATP. Este compuesto interactúa directamente con el dominio catalítico de MLCK y conduce a una pérdida irreversible de la actividad enzimática. No tiene efecto inhibidor sobre la proteína quinasa dependiente de cAMP, la proteína quinasa dependiente de cGMP y la proteína quinasa II dependiente de calmodulina, y tiene poco efecto sobre la actividad de la proteína quinasa C. Este inhibidor inhibe la formación de PtdInsP3 (fosfatidilinositol 3,4,5-trifosfato) estimulada por N-formilmetionil-leucilfenilalanina (fMLP) con una IC50 de 5 nM y esta inhibición se anula completamente cuando se pretrata con 100 nM de este compuesto en neutrófilos humanos, con niveles aumentados de PtdInsP2 y sin efectos sobre los contenidos celulares de PtdInsP y PtdIns. Podría desarrollar cambios oscilatorios en el contenido de F-actina y no inhibe la polimerización de actina estimulada por fMLP en neutrófilos. Este químico inhibe irreversiblemente la actividad de la fosfatidilinositol 3-quinasa (PI3-quinasa) uniéndose a la proteína de 110-kDa (IC50 de 3 nM) y no tiene efecto sobre la PI4-quinasa en células RBL-2H3. También inhibe la liberación de leucotrienos, sin efecto sobre la activación de la tirosina quinasa Lyn. Este compuesto anula completamente la captación de hexosa inducida en adipocitos de rata aislados a 0.1 μM, sin afectar la actividad lipolítica estimulada. Suprime la producción inducida de óxido nítrico en un 50% a 500 nM en células endoteliales de vena umbilical humana, lo que responde al IGF-1. Este químico suprime la reparación de rupturas de doble hebra de ADN (DSB) y no tiene efecto sobre los niveles de DSB o la cinética de reparación de rupturas de hebra simple (SSB) en células de ovario de hámster chino a 50 μM. Podría potenciar la citotoxicidad inducida por radiación ionizante (IR) sin toxicidad por sí mismo. Este inhibidor inhibe la actividad de la polo-like kinase (PLK1) con una IC50 de 24 nM en células intactas arrestadas en G2/M. Aumenta la acumulación de IL-6 mediada por el receptor tipo Toll (TLR) en macrófagos humanos con una EC50 de 50 nM. Mientras tanto, este compuesto mejora significativamente la expresión de óxido nítrico sintasa inducible (iNOS) mediada por TLR y la acumulación de nitrito en macrófagos de ratón. Activa el factor nuclear-κB y regula al alza la producción de ARNm de citoquinas. Este químico también inhibe Polo-like kinase (PlK) 1 y PlK3, que desempeñan papeles importantes en la mitosis. Su tratamiento podría llevar a una reducción en la fosforilación de p53 en serina 20 inducida por daño en el ADN. Suprime la fosforilación de Akt inducida por hialuronano y la motilidad/migración celular en células SW1990. |
||||||||
| In vivo | La Wortmannina inhibe la metástasis peritoneal de SW1990 en ratones a 1 mg/kg, sin pérdida de peso. Este compuesto inhibe la fosforilación de fosfatidilinositida 3-quinasa-proteína quinasa B (PKB)/Akt tanto en tejidos normales (homogenados de pulmón, corazón y cerebro) como en tejido tumoral en ratones, sin mortalidad ni toxicidad aguda a 0.7 mg/kg. En combinación con LY188011, este químico aumenta significativamente la apoptosis e inhibe el crecimiento tumoral en tumores ortotópicos, mientras que ambas monoterapias no pudieron. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
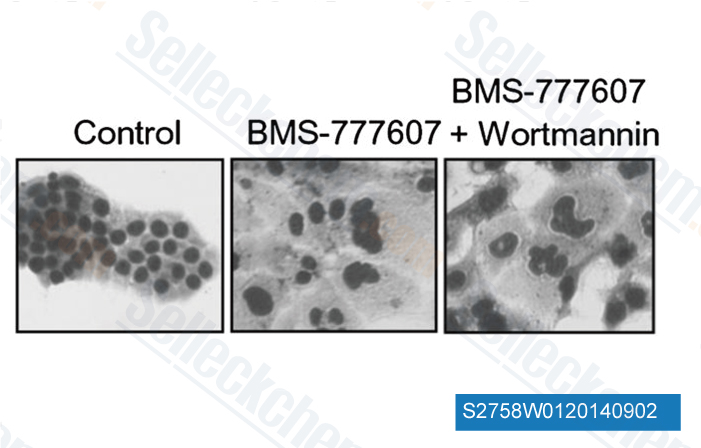
-
Datos de [ Mol Cancer Ther , 2014 , 13(1), 37-48 ]
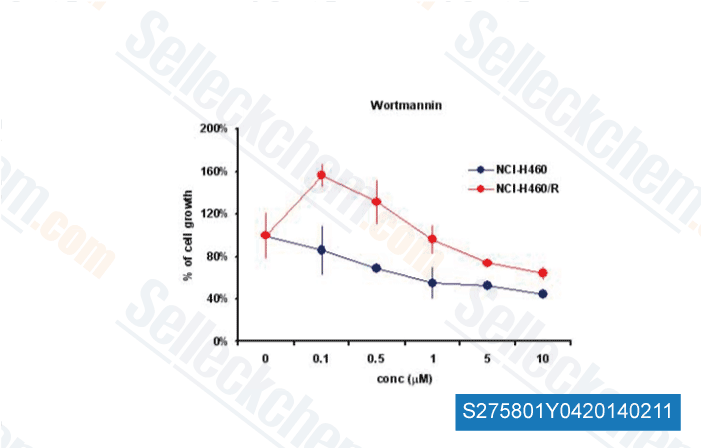
-
, 2014 , Dr.Milica Pesic from Institute for Biological Research
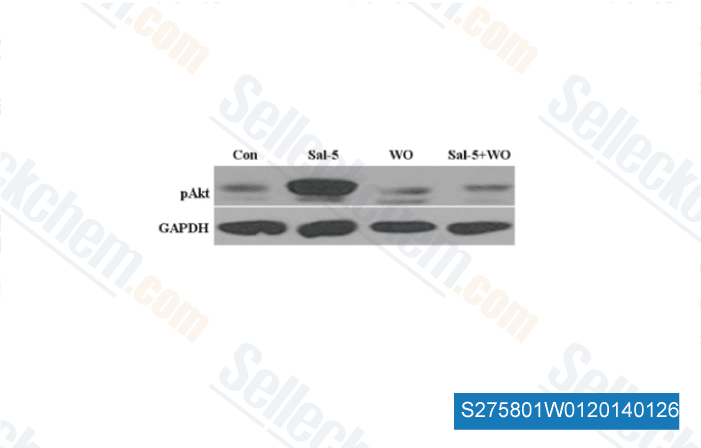
-
Datos de [ Int J Mol Sci , 2013 , 14(9), 17304-18 ]
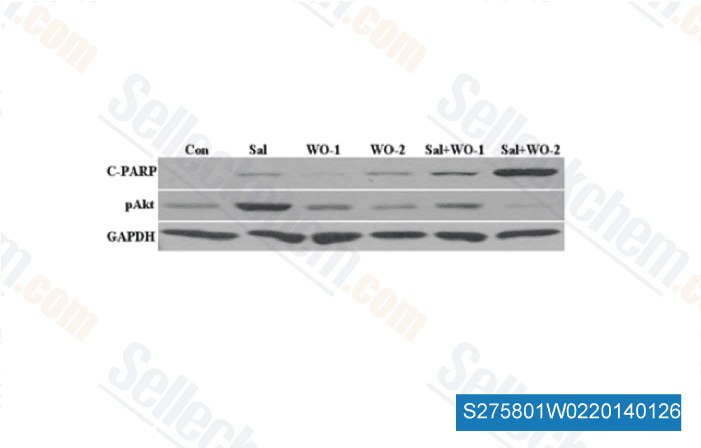
-
Datos de [ Int J Mol Sci , 2013 , 14(9), 17304-18 ]
Sellecks Wortmannin (SL-2052) Ha sido citado por 343 Publicaciones
| USP5 stabilizes YTHDF1 to control cancer immune surveillance through mTORC1-mediated phosphorylation [ Nat Commun, 2025, 16(1):1313] | PubMed: 39900921 |
| Cardiolipin inhibits the non-canonical inflammasome by preventing LPS binding to caspase-4/11 [ EMBO J, 2025, 10.1038/s44318-025-00507-z] | PubMed: 40670771 |
| Selective tubulin-binding drugs induce pericyte phenotype switching and anti-cancer immunity [ EMBO Mol Med, 2025, 10.1038/s44321-025-00222-6] | PubMed: 40140727 |
| Mechanical force-induced oncostatin M secretion by Jun-positive neutrophils promotes craniofacial bone regeneration for midface hypoplasia treatment [ Stem Cell Res Ther, 2025, 16(1):330] | PubMed: 40598376 |
| Siramesine induced cell death of glioblastoma through inactivating the STAT3-MGMT signaling pathway [ J Transl Med, 2025, 23(1):780] | PubMed: 40640878 |
| Depleting the action of EZH2 through PI3K-mTOR inhibition to overcome metastasis and immunotherapy resistance in triple-negative breast cancer [ Mol Cancer Ther, 2025, 10.1158/1535-7163.MCT-24-0693] | PubMed: 40497697 |
| Cepharanthine hydrochloride: a novel ferroptosis-inducing agent for prostate cancer treatment [ Front Pharmacol, 2025, 16:1536375] | PubMed: 40066333 |
| Intracellular Sphingosine-1-Phosphate Induces Lipolysis Through Direct Activation of Protein Kinase C Zeta [ FASEB J, 2025, 39(7):e70528] | PubMed: 40193069 |
| Vegfr3 activation of Pkd2l1+ CSF-cNs triggers the neural stem cell response in spinal cord injury [ Cell Signal, 2025, 130:111675] | PubMed: 39986360 |
| RhFGF21 protected PC12 cells against mitochondrial apoptosis triggered by H2O2 via the AKT-mediated ROS signaling pathway [ Exp Cell Res, 2025, 445(1):114417] | PubMed: 39793749 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
