Datos técnicos
| Fórmula | C23H18ClF2N3O3S |
||||||
| Peso molecular | 489.92 | Número CAS | 918504-65-1 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 98 mg/mL (200.03 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Vemurafenib (PLX4032, RG7204, RO5185426) es un nuevo y potente inhibidor de B-RafV600E con una IC50 de 31 nM en un ensayo sin células. 10 veces más selectivo para B-RafV600E que para B-Raf de tipo salvaje en ensayos enzimáticos y la selectividad celular puede superar las 100 veces. Vemurafenib (PLX4032, RG7204) induce la Autophagy. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
|||||||||||
| In vitro | Vemurafenib (PLX4032) inhibe B-RAFV600E, C-RAF, así como B-RAF de tipo salvaje, con IC50 de 31 nM, 48 nM y 100 nM, respectivamente. Este compuesto también inhibe varias quinasas no RAF, incluyendo ACK1, KHS1 y SRMS, con IC50 de 18 nM a 51 nM. En las líneas celulares de melanoma, el efecto inhibidor depende del estado mutacional de B-RAF, ya que inhibe potentemente aquellas que albergan mutantes B-RAF V600, incluyendo V600E, V600D, V600K y V600R, pero no el tipo salvaje u otros mutantes. Los valores de IC50 en estas células, incluyendo MALME-3M, Colo829, Colo38, A375, SK-MEL28 y A2058, oscilan entre 20 nM y 1 μM. En estas células, Vemurafenib (0,1 μM a 30 μM) también inhibe la fosforilación de MEK1/2 y ERK1/2. Es muy eficaz en el tratamiento del melanoma, por su capacidad de inhibir B-RAFV600E. Sin embargo, este compuesto muestra un efecto limitado en pacientes con cáncer de colon que también portan la oncoproteína B-RAFV600E. La razón de esto es que, en las células de cáncer de colon, la inhibición de B-RAFV600E por él da como resultado una rápida activación por retroalimentación del EGFR, que compensa la proliferación celular inhibida por PLX4032. | |||||||||||
| In vivo | En modelos de xenoinjertos de ratones con mutación B-RAFV600E, Vemurafenib (PLX4032) (6 mg/kg–20 mg/kg) inhibe el crecimiento tumoral. En modelos de xenoinjertos de ratones de células LOX, Colo829 y A375, este compuesto (12,5 mg/kg–100 mg/kg) inhibe el crecimiento tumoral y prolonga la supervivencia de los ratones. | |||||||||||
| Características | Un nuevo y potente inhibidor de la oncoproteína B-RAFV600E. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
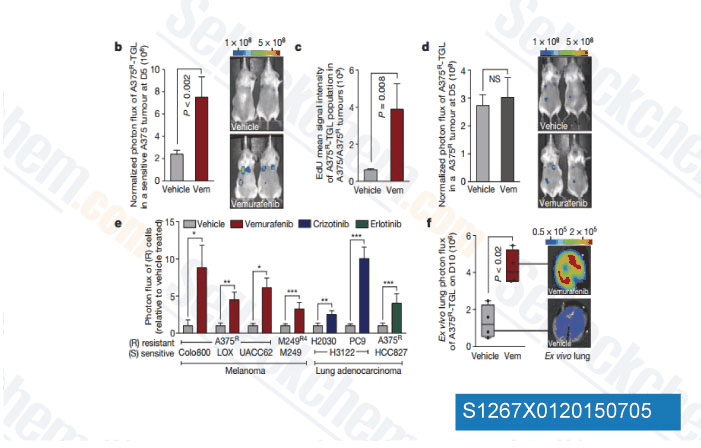
-
Datos de [ Nature , 2015 , 520(7547), 368-72 ]
![FRA1 downregulation during RAFi treatment drives the reactive secretome. c, Relative mRNA levels of FRA1 during vemurafenib exposure [0.1-1 uM]. d, Representative immunofluorescence staining of A375/A375R tumours for GFP (A375R, green) and FRA1 (red) after vehicle or vemurafenib treatment (5 days). DAPI, 49,6-diamidino-2-phenylindole. Scale bars, 50 um.](https://file.selleckchem.com/downloads/review/700px/Vemurafenib-S1267X0220150705.gif)
-
Datos de [ Nature , 2015 , 520(7547), 368-72 ]

-
Datos de [ Oncogene , 2015 , 10.1038/onc.2015.97 ]

-
Datos de [ Nature , 2014 , 508(7494), 118-22 ]
Sellecks PLX4032 (Vemurafenib) Ha sido citado por 714 Publicaciones
| Pan-inhibition of super-enhancer-driven oncogenic transcription by next-generation synthetic ecteinascidins yields potent anti-cancer activity [ Nat Commun, 2025, 16(1):512] | PubMed: 39779693 |
| Blocking interplay between TERT and c-Myc: a new therapeutic strategy for BRAFV600E/pTERT double mutated tumors [ Int J Biol Sci, 2025, 21(11):4961-4978] | PubMed: 40860184 |
| Downregulated ALDH2 Contributes to Tumor Progression and Targeted Therapy Resistance in Human Metastatic Melanoma Cells [ Cells, 2025, 14(12)913] | PubMed: 40558540 |
| Inter-Relationship Between Melanoma Vemurafenib Tolerance Thresholds and Metabolic Pathway Choice [ Cells, 2025, 14(12)923] | PubMed: 40558548 |
| Exploiting Paradoxical Activation of Oncogenic MAPK Signaling by Targeting Mitochondria to Sensitize NRAS Mutant-Melanoma to Vemurafenib [ Int J Mol Sci, 2025, 26(6)2675] | PubMed: 40141318 |
| Acquired resistance to vemurafenib restrains thyroid cancer stem cell self-renewal by suppressing STAT3 activation [ Cell Signal, 2025, 133:111845] | PubMed: 40345509 |
| Dihydrotanshinone I enhanced BRAF mutant melanoma treatment efficacy by inhibiting the STAT3/SOX2 signaling pathway [ Front Oncol, 2025, 15:1429018] | PubMed: 39944829 |
| Suppression of Sebum Production by Vemurafenib Through Paradoxical ERK Activation Resulted in the Inhibition of the mTOR Pathway in 5α-Dihydrotestosterone-Differentiated Hamster Sebocytes In Vitro [ Exp Dermatol, 2025, 34(8):e70150] | PubMed: 40817681 |
| Selective inhibition of p300 by a novel small molecule EPS496 promotes cell death in vemurafenib-resistant BRAFV600E mutated melanoma cells [ Biochem Biophys Res Commun, 2025, 750:151382] | PubMed: 39884005 |
| Increased Mitochondrial Superoxide Level Is Partially Associated With Vemurafenib-Induced Renal Tubular Toxicity [ Basic Clin Pharmacol Toxicol, 2025, 136(4):e70015] | PubMed: 40018909 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
