Datos técnicos
| Fórmula | C26H24F3N7O3S |
||||||||||
| Peso molecular | 571.57 | Número CAS | 1439399-58-2 | ||||||||
| Solubilidad (25°C)* | In vitro | DMSO | 100 mg/mL (174.95 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Telaglenastat (CB-839) es un inhibidor potente, selectivo y biodisponible por vía oral de la glutaminase con una IC50 de 24 nM para el GAC humano recombinante. Induce Autophagy y tiene actividad antitumoral. Fase 1. | ||
|---|---|---|---|
| Objetivos |
|
||
| In vitro | Telaglenastat (CB-839) exhibe una cinética tiempo-dependiente y lentamente reversible. Sus valores de IC50 para la inhibición de Glutaminase después de la preincubación con rHu-GAC durante 1 hora son < 50 nmol/L, al menos 13 veces menores que con BPTES. Este compuesto tiene actividad antiproliferativa en una línea celular de cáncer de mama triple negativo (TNBC), HCC-1806, mientras que no se observa actividad antiproliferativa en una línea celular con receptores de estrógeno positivos, T47D. |
||
| In vivo | En el modelo murino de TNBC, el Telaglenastat (CB-839) como agente único (200 mg/kg, p.o.) suprime el crecimiento tumoral en un 61 % en relación con el control del vehículo. En el modelo de xenoinjerto JIMT-1 murino, este compuesto solo (200 mg/kg, p.o.) produce una inhibición del crecimiento tumoral (TGI) del 54 % en relación con el control del vehículo, mientras que su combinación con NSC 125973 (10 mg/kg, p.o.) suprime en gran medida el nuevo crecimiento de los tumores, lo que resulta en una TGI del 100 % en relación con el control del vehículo. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
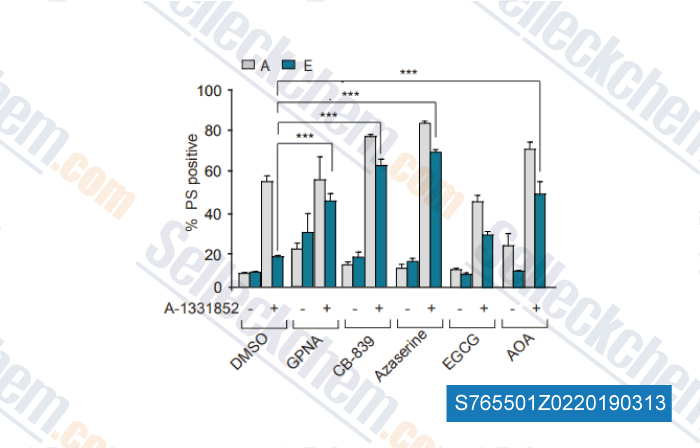
-
Datos de [ , , Haematologica, 2018, doi:10.3324/haematol.2018.204701 ]
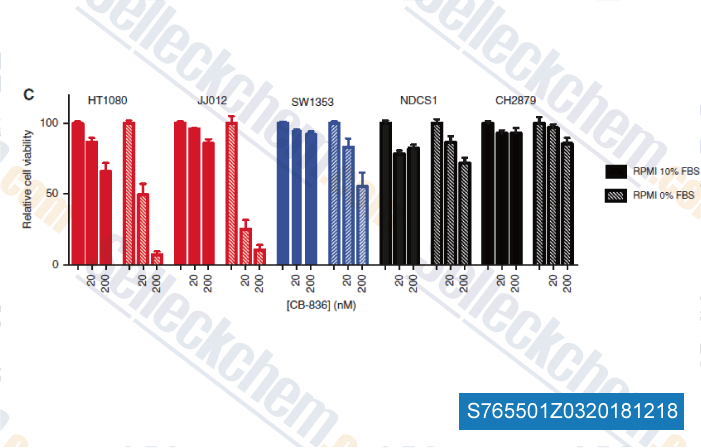
-
Datos de [ , , Br J Cancer, 2018, 118(8):1074-1083 ]
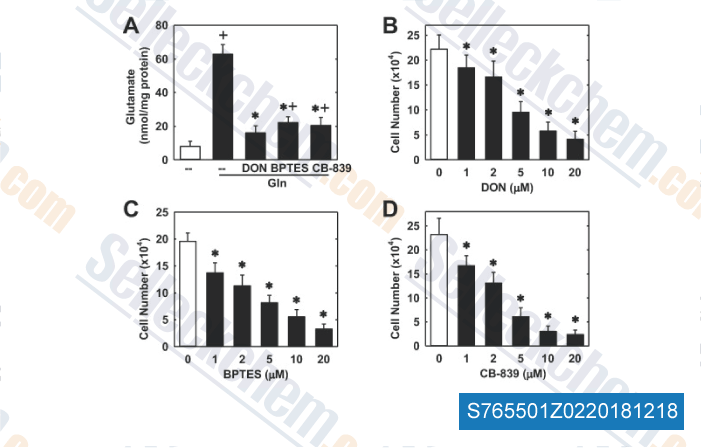
-
Datos de [ , , Biochem Pharmacol, 2018, 156:204-214 ]

-
Datos de [ , , Tumor Biol, 2016, 37:11007-11015. ]
Sellecks Telaglenastat (CB-839) Ha sido citado por 118 Publicaciones
| High fructose consumption aggravates inflammation by promoting effector T cell generation via inducing metabolic reprogramming [ Signal Transduct Target Ther, 2025, 10(1):271] | PubMed: 40854873 |
| Chaperone-mediated autophagy directs a dual mechanism to balance premature senescence and senolysis to prevent intervertebral disc degeneration [ Bone Res, 2025, 13(1):62] | PubMed: 40506462 |
| GDH1-dependent α-ketoglutarate promotes HBV transcription by modulating histone methylations on the cccDNA minichromosome [ Clin Mol Hepatol, 2025, 10.3350/cmh.2024.0694] | PubMed: 39905842 |
| The metabolic shift of glutaminase 2 to glutaminase 1 promotes LGR5 + progenitor cell proliferation in liver cirrhosis [ Cell Mol Life Sci, 2025, 82(1):251] | PubMed: 40550888 |
| Glutaminase as a metabolic target of choice to counter acquired resistance to Palbociclib by colorectal cancer cells [ Oncogene, 2025, 44(36):3386-3406] | PubMed: 40696167 |
| Endogenous protein S100A14 stabilizes glutaminase to render hepatocellular carcinoma resistant to sorafenib [ J Transl Med, 2025, 23(1):435] | PubMed: 40217256 |
| Autophagic flux-lipid droplet biogenesis cascade sustains mitochondrial fitness in colorectal cancer cells adapted to acidosis [ Cell Death Discov, 2025, 11(1):21] | PubMed: 39856069 |
| Imaging the uptake and metabolism of glutamine in prostate tumor models using CEST MRI [ Npj Imaging, 2025, 3(1):34] | PubMed: 40750673 |
| Distinct malignant cell states and myeloid glutamate signaling associated with aggressive pancreatic neuroendocrine tumors [ bioRxiv, 2025, 2025.07.15.664730] | PubMed: 40791359 |
| PP2A activation drives aberrant macropinocytosis and cell death in pancreatic ductal adenocarcinoma [ bioRxiv, 2025, 2025.07.14.664742] | PubMed: 40791444 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
