Datos técnicos
| Fórmula | C14H8N2O |
||||||
| Peso molecular | 220.23 | Número CAS | 129-56-6 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 44 mg/mL (199.79 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | SP600125 (Nsc75890) es un inhibidor de amplio espectro de JNK para JNK1, JNK2 y JNK3 con una IC50 de 40 nM, 40 nM y 90 nM en ensayos sin células, respectivamente; una selectividad 10 veces mayor contra MKK4, 25 veces mayor contra MKK3, MKK6, PKB y PKCα, y una selectividad 100 veces mayor contra ERK2, p38, Chk1, EGFR, etc. Este compuesto es también un inhibidor de amplio espectro de serine/threonine kinases incluyendo Aurora kinase A, FLT3 y TRKA con una IC50 de 60 nM, 90 nM y 70 nM. Inhibe la autophagy y activa la apoptosis. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
|||||||||||
| In vitro | SP600125 se caracteriza originalmente como un inhibidor selectivo competitivo de ATP de la c-Jun N-terminal kinase JNK. En células T Jurkat, este compuesto inhibe la fosforilación de c-Jun con una IC50 de 5 μM a 10 μM. En células CD4+, como las células Th0 aisladas de sangre de cordón humano o sangre periférica, bloquea la activación y diferenciación celular e inhibe la expresión de genes inflamatorios COX-2, IL-2, IL-10, IFN-γ y TNF-α, con una IC50 de 5 μM a 12 μM. Sin embargo, estudios posteriores revelan que este químico también suprime el receptor de hidrocarburos arílicos (AhR) , Mps1 , y un panel de otras serine/threonine kinases, incluyendo Aurora kinase A, FLT3, MELK y TRKA . En células beta de ratón MIN6, este compuesto (20 μM) induce la fosforilación de p38 MAPK y la activación de su promotor dependiente de CREB. En células HCT116, (20 μM) bloquea la transición de la fase G2 a la mitosis e induce la endorreduplicación. Esta capacidad de este inhibidor es independiente de la inhibición de JNK, pero debido a su inhibición de la activación de CDK1-ciclina B aguas arriba de Aurora A y Polo-like kinase 1. |
|||||||||||
| In vivo | En ratones, SP600600125 (15 mg/kg o 30 mg/kg) inhibe significativamente la expresión de TNF-α inducida por lipopolisacárido (LPS) y la apoptosis de timocitos CD4+ CD8+ inducida por anti-CD3. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
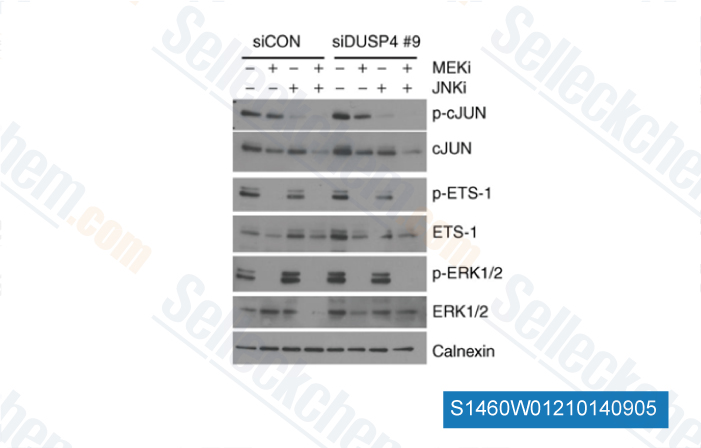
-
Datos de [ Cancer Res , 2013 , 73(20):6346-58 ]
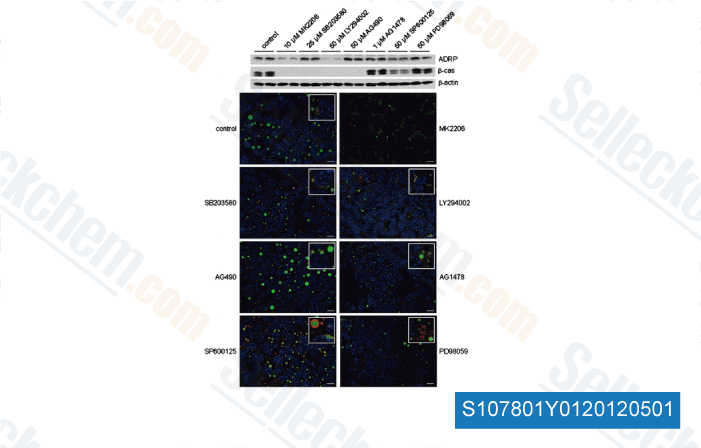
-
Datos de [ Biochim Biophys Acta , 2012 , 1823(5), 987-96 ]
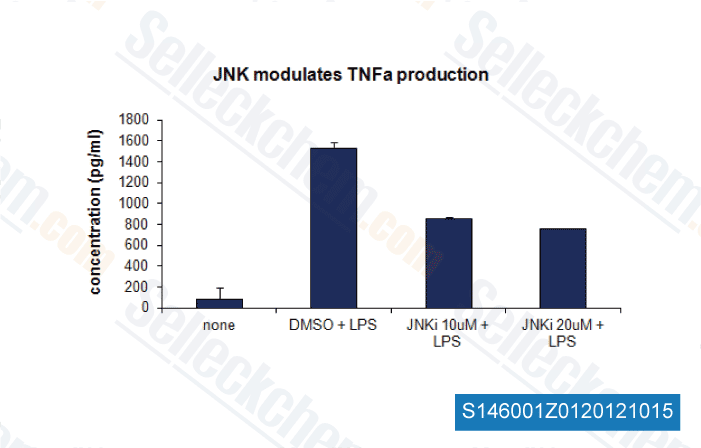
-
, , Lee lay hoon from National University of Singapore
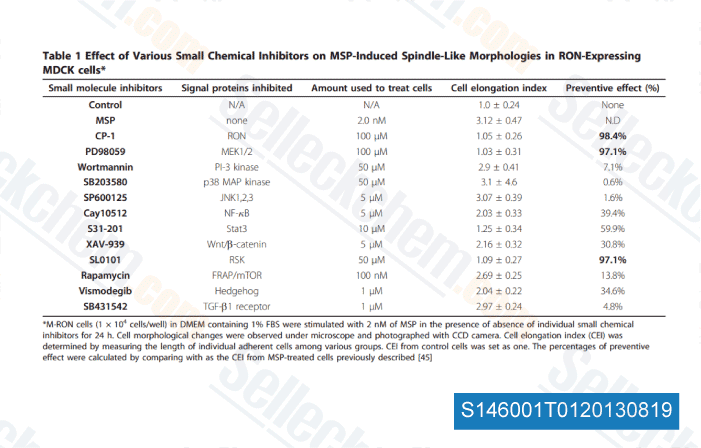
-
,
Sellecks SP600125 Ha sido citado por 1098 Publicaciones
| Nucleus-translocated glucokinase functions as a protein kinase to phosphorylate TAZ and promote tumour growth [ Nat Commun, 2025, 16(1):7156] | PubMed: 40759645 |
| Gut Microbiota Modulates Obesity-Associated Skeletal Deterioration Through Macrophage Aging and Grancalcin Secretion [ Adv Sci (Weinh), 2025, 12(28):e2502634] | PubMed: 40349163 |
| Orosomucoid 1 Ameliorates Temporomandibular Joint Osteoarthritis by Maintaining Cartilage Homeostasis [ Adv Sci (Weinh), 2025, 12(36):e00028] | PubMed: 40583170 |
| Enhancing radiosensitivity of osteosarcoma by ITGB3 knockdown: a mechanism linked to enhanced osteogenic differentiation status through JNK/c-JUN/RUNX2 pathway activation [ J Exp Clin Cancer Res, 2025, 44(1):159] | PubMed: 40410897 |
| Hypoxia-induced degradation of FTO promotes apoptosis by unmasking RACK1-mediated activation of MTK1-JNK1/2 pathway [ J Adv Res, 2025, S2090-1232(25)00038-4] | PubMed: 39805423 |
| FNDC5/irisin-enriched sEVs conjugated with bone-targeting aptamer alleviate osteoporosis: a potential alternative to exercise [ J Nanobiotechnology, 2025, 23(1):504] | PubMed: 40652239 |
| Lipin3 deficiency aggravates cisplatin induced acute kidney injury via activating Sirt1-p21-Caspase 3-GSDME pyroptosis pathway [ Int J Biol Sci, 2025, 21(12):5185-5205] | PubMed: 40959286 |
| RNA polymerase II subunit 5-mediating protein limits TLR4-induced innate immune activation in macrophages by inhibiting IKKβ/NF-κB signaling during sepsis [ Cell Commun Signal, 2025, 23(1):274] | PubMed: 40495190 |
| CDO1 phosphorylation is required for IL-6-induced tumor cell proliferation through governing cysteine availability [ Cell Commun Signal, 2025, 23(1):194] | PubMed: 40269955 |
| M2 macrophage-derived extracellular vesicles protect against abdominal aortic aneurysm by modulating macrophage polarization through miR221-5p [ Cell Mol Biol Lett, 2025, 30(1):96] | PubMed: 40784924 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
