Datos técnicos
| Fórmula | C26H22N2O2 |
||||||||||
| Peso molecular | 394.47 | Número CAS | 410536-97-9 | ||||||||
| Solubilidad (25°C)* | In vitro | DMSO | 23 mg/mL (58.3 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Sirtinol es un inhibidor específico de SIRT1 y SIRT2 con IC50 de 131 μM y 38 μM en ensayos libres de células, respectivamente. | ||||
|---|---|---|---|---|---|
| Objetivos |
|
||||
| In vitro | Sirtinol inhibe potentemente la actividad de Sir2p de levadura recombinante in vitro con una IC50 de 68 μM. A diferencia de la TSA, este compuesto no ha mostrado ningún efecto sobre la HDAC1 humana, lo que indica que es un inhibidor selectivo de Sirtuin. A diferencia de la TSA, el tratamiento de fibroblastos primarios humanos con este químico no causa cambios globales en la acetilación de histonas y tubulina, ni induce un cambio morfológico en la línea celular tumoral HeLa. El tratamiento con este inhibidor a 100 μM durante 24 horas causa una detención del crecimiento sostenida en células MCF-7 y H1299 durante hasta 9 días después de su retirada. Este tratamiento induce un aumento de la actividad SA-β-gal y la expresión de PAI-1 en ambas células MCF-7 y H1299, más potentemente que Splitomicina. Inhibe la formación de colonias a concentraciones de 33 μM y superiores en células MCF-7 y H1299, más eficazmente en comparación con Splitomicina. Este compuesto (100 μM) atenúa significativamente la fosforilación tanto basal como estimulada por EGF o IGF-I de ERK, JNK/SAPK y p38 MAPK en células MCF-7 y H1299. Bloquea la activación basal y estimulada por EGF de Ras. Consistentemente, la fosforilación basal y estimulada por EGF o IGF-I de Raf-1, MEK, SEK1/MKK4 y MKK7 se atenúa en células tratadas con este inhibidor. La inhibición de Sirt1 por este químico mejora la acetilación de p53 inducida por UV y H2O2 para aumentar la muerte celular en queratinocitos de piel cultivados. El bloqueo de Sirt1 mediante este tratamiento resulta en una inhibición significativa del crecimiento y la viabilidad de las células PCa humanas, sin afectar a las células epiteliales prostáticas normales. | ||||
| In vivo | La administración de Sirtinol a 1 mg/kg atenúa la producción de citocinas proinflamatorias y protege contra la lesión hepática después de un traumatismo-hemorragia en ratas Sprague-Dawley macho. | ||||
| Características | Sirtinol no inhibe las HDAC de clase I y clase II. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
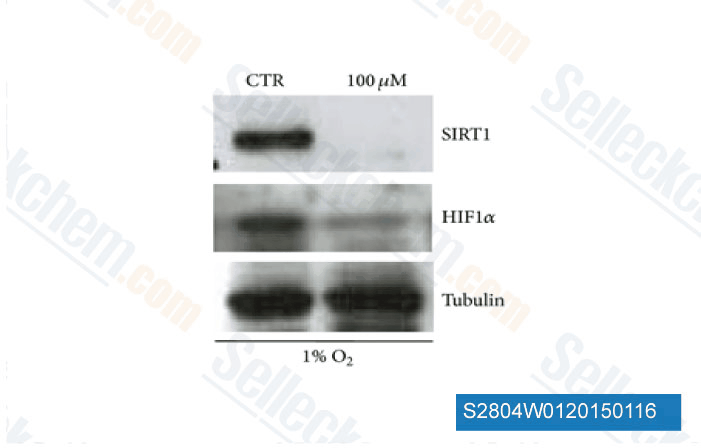
-
Datos de [ Biomed Res Int , 2014 , 783459 ]
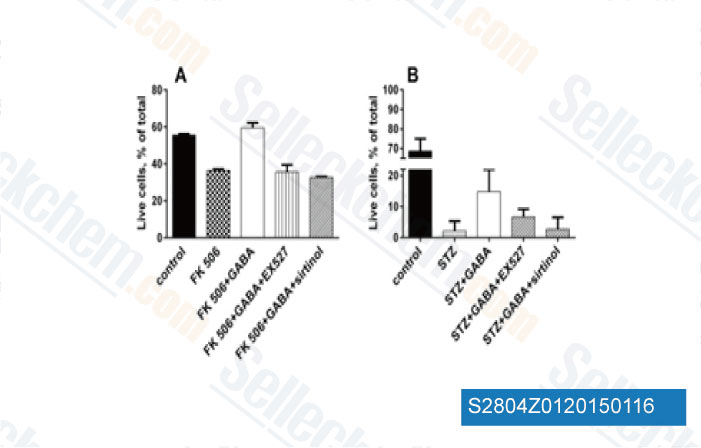
-
Datos de [ Biochem Biophys Res Commun , 2014 , 452(3), 649-54 ]
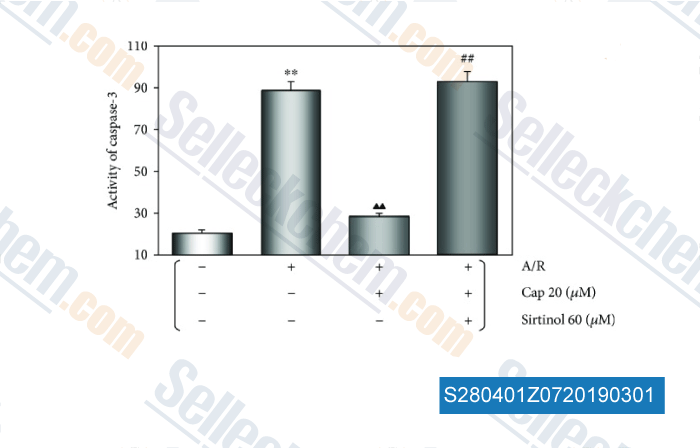
-
Datos de [ , , Oxid Med Cell Longev, 2017, 2017:1035702 ]
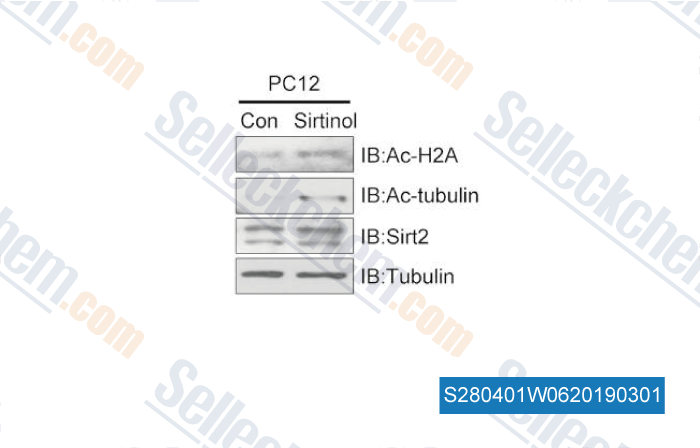
-
Datos de [ , , Sci Rep, 2016, 6:21857 ]
Sellecks Sirtinol Ha sido citado por 44 Publicaciones
| α-Mangostin Inhibited M1 Polarization of Macrophages/Monocytes in Antigen-Induced Arthritis Mice by Up-Regulating Silent Information Regulator 1 and Peroxisome Proliferators-Activated Receptor γ Simultaneously [ Drug Des Devel Ther, 2023, 17:563-577] | PubMed: 36860800 |
| A COMPARATIVE ANALYSIS TO DETERMINE THE OPTIMUM HISTONE DEACETYLASE INHIBITORS AND ADMINISTRATION ROUTE FOR IMPROVING SURVIVAL AND ORGAN INJURY IN RATS AFTER HEMORRHAGIC SHOCK [ Shock, 2023, 60(1):75-83] | PubMed: 37141162 |
| Protective effect of HDACIs in improves survival and organ injury after CLP-induced sepsis [ Surg Open Sci, 2023, 12:35-42] | PubMed: 36936452 |
| Epigenetic alterations of CXCL5 in Cr(VI)-induced carcinogenesis [ Sci Total Environ, 2022, 838(Pt 1):155713] | PubMed: 35660107 |
| Targeting the MITF/APAF-1 axis as salvage therapy for MAPK inhibitors in resistant melanoma [ Cell Rep, 2022, 41(6):111601] | PubMed: 36351409 |
| Nicotinamide improves in vitro lens regeneration in a mouse capsular bag model [ Stem Cell Res Ther, 2022, 13(1):198] | PubMed: 35550648 |
| Effects of Hst3p inhibition in <i>Candida albicans</i>: a genome-wide H3K56 acetylation analysis [ Front Cell Infect Microbiol, 2022, 12:1031814] | PubMed: 36389164 |
| Nicotinamide n-Oxide Attenuates HSV-1-Induced Microglial Inflammation through Sirtuin-1/NF-κB Signaling [ Int J Mol Sci, 2022, 23(24)16085] | PubMed: 36555725 |
| Arylamine N-Acetyltransferase 1 Activity is Regulated by the Protein Acetylation Status [ Front Pharmacol, 2022, 13:797469] | PubMed: 35153780 |
| Screening Health-Promoting Compounds for Their Capacity to Induce the Activity of FOXO3 [ J Gerontol A Biol Sci Med Sci, 2022, 77-8:1485-1493] | PubMed: 34508571 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
