Datos técnicos
| Fórmula | C17H18N6 |
||||||
| Peso molecular | 306.37 | Número CAS | 941678-49-5 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 61 mg/mL (199.1 mM) | ||||
| Ethanol | 61 mg/mL (199.1 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Ruxolitinib (INCB18424) es el primer inhibidor potente y selectivo de JAK1/2 en entrar en la clínica con una IC50 de 3,3 nM/2,8 nM en ensayos libres de células, >130 veces la selectividad para JAK1/2 frente a JAK3. Este compuesto mata las células tumorales a través de Mitophagy tóxica. Induce Autophagy y mejora Apoptosis related. | ||||
|---|---|---|---|---|---|
| Objetivos |
|
||||
| In vitro | Ruxolitinib (INCB18424) inhibe de forma potente y selectiva la señalización y proliferación mediada por JAK2V617F en células Ba/F3 y células HEL. Este compuesto aumenta marcadamente la apoptosis de forma dosis-dependiente en células Ba/F3. A 64 nM, produce una duplicación de células con mitocondrias despolarizadas en células Ba/F3. Este químico inhibe la proliferación de progenitores eritroides de donantes normales y pacientes con policitemia vera con IC50 de 407 nM y 223 nM, respectivamente. Demuestra una potencia notable contra la formación de colonias eritroides con una IC50 de 67 nM. | ||||
| In vivo | INCB018424 (180 mg/kg, oral, dos veces al día) da como resultado una tasa de supervivencia superior al 90% en el día 22 en un modelo de ratón impulsado por JAK2V617F. Este compuesto (180 mg/kg, oral, dos veces al día) reduce marcadamente la esplenomegalia y los niveles circulantes de citocinas inflamatorias, y elimina preferentemente las células neoplásicas, lo que resulta en una supervivencia significativamente prolongada sin efectos mielosupresores o inmunosupresores en un modelo de ratón impulsado por JAK2V617F. En el ensayo doble ciego de mielofibrosis, el criterio de valoración principal se alcanza en el 41,9% de los pacientes del grupo de Ruxolitinib (INCB18424) en comparación con el 0,7% en el grupo de placebo. Esto da como resultado el mantenimiento de la reducción del volumen del bazo y una mejora del 50% o más en la puntuación total de los síntomas. Un total del 28% de los pacientes del grupo que recibió este compuesto (15 mg dos veces al día) tuvo una reducción de al menos el 35% en el volumen del bazo en la semana 48 en pacientes con mielofibrosis, en comparación con el 0% en el grupo que recibió la mejor terapia disponible. La longitud media palpable del bazo disminuyó en un 56% con él, pero aumentó en un 4% con la mejor terapia disponible en la semana 48. Los pacientes del grupo de ruxolitinib tuvieron una mejora en las medidas generales de calidad de vida y una reducción de los síntomas asociados con la mielofibrosis. |
Protocolo (de referencia)
| Ensayo de quinasa:[1] |
|
|---|---|
| Ensayo celular:[1] |
|
| Estudio en animales:[1] |
|
Referencias
|
Validación de productos por parte del cliente
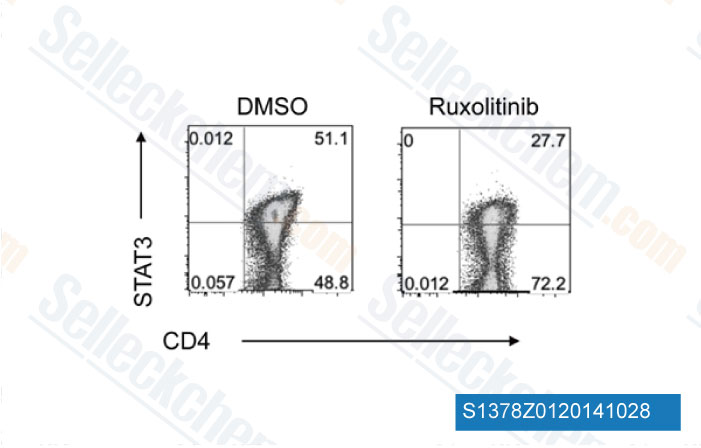
-
Datos de [ Blood , 2014 , 123(24), 3832-42 ]
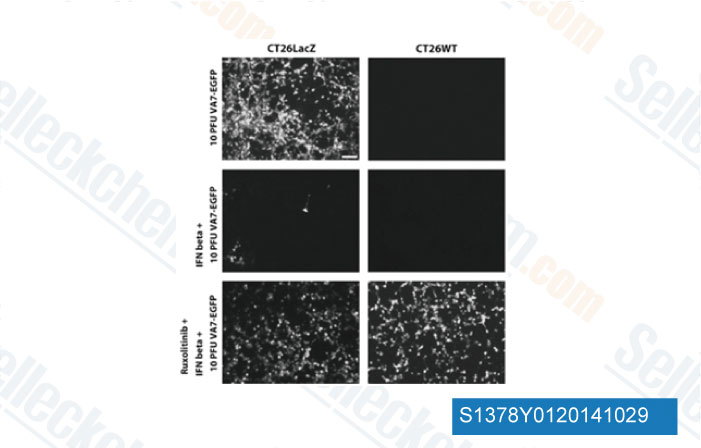
-
Datos de [ Gene Ther , 2014 , 10.1038/gt.2014.83 ]
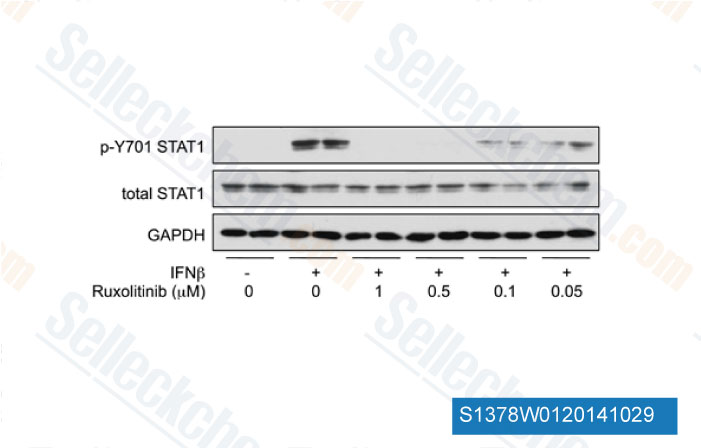
-
Datos de [ J Immunol , 2012 , 189(6), 2784-92 ]
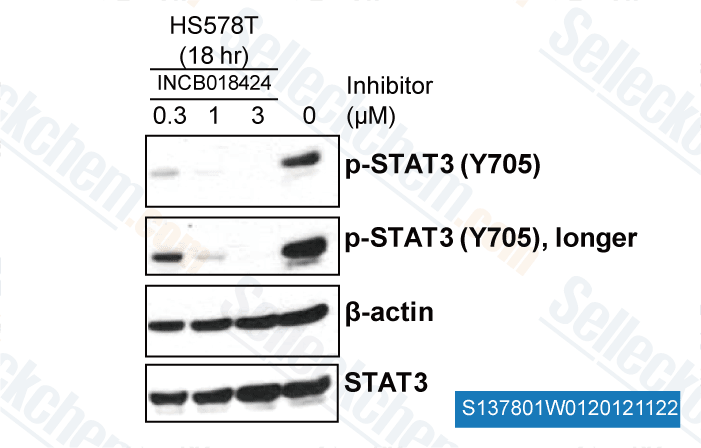
-
, , Yong Weon Yi Georgetown University
Sellecks Ruxolitinib (INCB18424) Ha sido citado por 661 Publicaciones
| Microbial metabolite drives ageing-related clonal haematopoiesis via ALPK1 [ Nature, 2025, 10.1038/s41586-025-08938-8] | PubMed: 40269158 |
| Macrophage-derived amphiregulin induces myofibroblast transition in adipogenic lineage precursors near Staphylococcus aureus abscess in bone marrow [ Nat Commun, 2025, 16(1):8409] | PubMed: 40998791 |
| RSK1 is an exploitable dependency in myeloproliferative neoplasms and secondary acute myeloid leukemia [ Nat Commun, 2025, 16(1):492] | PubMed: 39820365 |
| Severe inflammation and lineage skewing are associated with poor engraftment of engineered hematopoietic stem cells in patients with sickle cell disease [ Nat Commun, 2025, 16(1):3137] | PubMed: 40169559 |
| Inhibition of the STAT3/Fanconi anemia axis is synthetic lethal with PARP inhibition in breast cancer [ Nat Commun, 2025, 16(1):2159] | PubMed: 40038300 |
| A patient-derived T cell lymphoma biorepository uncovers pathogenetic mechanisms and host-related therapeutic vulnerabilities [ Cell Rep Med, 2025, S2666-3791(25)00102-8] | PubMed: 40147445 |
| Enhanced regenerative and developmental potential of embryonal and stem cell-derived platelets compared to adult platelets [ Cell Rep Med, 2025, 6(8):102297] | PubMed: 40795844 |
| ADH5/ALDH2 dehydrogenases and DNA polymerase theta protect normal and malignant hematopoietic cells from formaldehyde challenge: therapeutic implications [ Leukemia, 2025, 39(9):2152-2162] | PubMed: 40640557 |
| Adipocytes-induced ANGPTL4/KLF4 axis drives glycolysis and metastasis in triple-negative breast cancer [ J Exp Clin Cancer Res, 2025, 44(1):192] | PubMed: 40616161 |
| Dual targeting of CDK6 and LSD1 is synergistic and overcomes differentiation blockade in AML [ EMBO Mol Med, 2025, 10.1038/s44321-025-00296-2] | PubMed: 40883610 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
