Datos técnicos
| Fórmula | C13H11N3O4 |
||||||
| Peso molecular | 273.24 | Número CAS | 19171-19-8 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 55 mg/mL (201.28 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Pomalidomide inhibe la liberación de TNF-α inducida por LPS con una IC50 de 13 nM en PBMC. Pomalidomide puede ser utilizado en PROTAC como ligando para la diana E3 ligasa e inhibir la proteína E3 ligasa cereblon (CRBN). Pomalidomide promueve la apoptosis y el arresto del ciclo celular. | ||||
|---|---|---|---|---|---|
| Objetivos |
|
||||
| In vitro | Pomalidomide inhibe la liberación de TNF-alpha estimulada por lipopolisacáridos (LPS) en PBMC humanos y en sangre total humana con valores de IC50 de 13 nM y 25 nM, respectivamente. Este compuesto inhibe el crecimiento de las células T reguladoras que es estimulado por IL-2 con una IC50 de ~1 μM. El tratamiento con este químico (6,4 nM-10 μM) aumenta la producción de IL-2 en células T de sangre periférica humana, y es ligeramente más potente en el subconjunto CD4+ que en el subconjunto CD8+. Es significativamente más potente que CC-5013 en la elevación de los niveles de IL-2, IL-5 e IL-10, pero solo ligeramente más potente que CC-5013 en la elevación de los niveles de IFN-γ. Este agente mejora la actividad transcripcional de AP-1 inducida por las células SEE y Raji en las células Jurkat de manera dosis-dependiente, con una mejora máxima de 4 veces a 1 μM. La exposición de las células Raji a diversas concentraciones de este compuesto (2,5-40 μg/mL) durante 48 horas conduce a una disminución significativa en la proliferación celular y la síntesis de ADN. Hay una reducción de aproximadamente el 40% en comparación con los controles tratados con vehículo. |
||||
| In vivo | Pomalidomide mejora el efecto antitumoral de rituximab contra linfomas de células B en ratones inmunodeficientes combinados graves. La administración de este compuesto en combinación con rituximab, otorga a los ratones un período de supervivencia mediano de 74 días en comparación con los 58 días del tratamiento con CC5013/rituximab y los 45 días de la monoterapia con rituximab. El efecto sinérgico de este compuesto y rituximab puede ser completamente abrogado por la depleción de células NK, apoyando la propuesta de que la expansión de células NK es un mecanismo por el cual este compuesto puede aumentar la actividad antitumoral de rituximab. |
||||
| Características | Un derivado de la talidomida y hasta 10.000 veces más potente que la talidomida. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
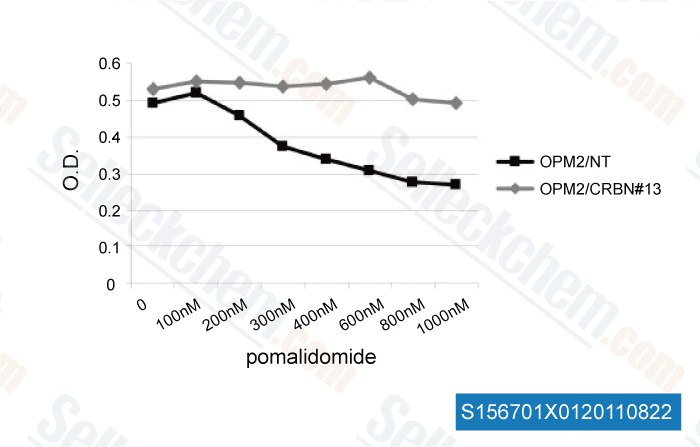
-
Datos de [ Blood , 2011 , 118, 4771-4779 ]
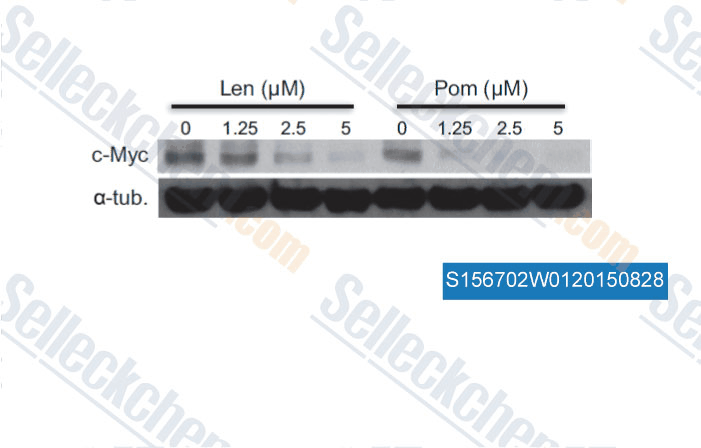
-
Datos de [ , , Blood Cancer Journal, 2015, 5: e312 ]
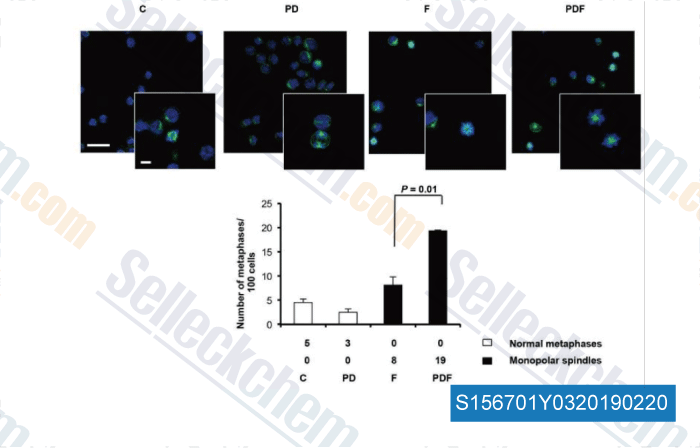
-
Datos de [ , , Haematologica, 2017, 102(12):2113-2124 ]
Sellecks Pomalidomide (CC-4047) Ha sido citado por 124 Publicaciones
| Systematic comparison and base-editing-mediated directed protein evolution and functional screening yield superior auxin-inducible degron technology [ Nat Commun, 2025, 16(1):6631] | PubMed: 40681502 |
| A patient-derived T cell lymphoma biorepository uncovers pathogenetic mechanisms and host-related therapeutic vulnerabilities [ Cell Rep Med, 2025, S2666-3791(25)00102-8] | PubMed: 40147445 |
| Novel Cereblon-Binding Immunomodulators Have Increased Potency Against Gammaherpesvirus- Associated Lymphomas In Vitro [ J Med Virol, 2025, 97(8):e70537] | PubMed: 40767544 |
| The Prolonged Half-Life of the p53 Missense Variant R248Q Promotes Accumulation and Heterotetramer Formation with Wildtype p53 to Exert the Dominant-Negative Effect [ Cancer Res, 2025, 10.1158/0008-5472.CAN-24-1136] | PubMed: 40163352 |
| Controlling CRISPR-Cas9 genome editing in human cells using a molecular glue degrader [ Mol Ther Nucleic Acids, 2025, 36(3):102640] | PubMed: 40799508 |
| Enhancing T cell cytotoxicity in multiple myeloma with bispecific αPD-L1 × αCD3 T cell engager-armed T cells and low-dose bortezomib therapy [ Biomed Pharmacother, 2025, 184:117878] | PubMed: 39891948 |
| Discovery of Novel, Potent, and Orally Bioavailable SMARCA2 Proteolysis-Targeting Chimeras with Synergistic Antitumor Activity in Combination with Kirsten Rat Sarcoma Viral Oncogene Homologue G12C Inhibitors [ J Med Chem, 2025, 68(9):9202-9219] | PubMed: 40280558 |
| Pharmacologically induced proteolysis of histone deacetylase-6 attenuates influenza virus replication despite limited anti-tumor effects [ Life Sci, 2025, 363:123401] | PubMed: 39814129 |
| Rapid and high-throughput screening of proteolysis targeting chimeras using a dual-reporter system expressing fluorescence protein and luciferase [ BMC Biol, 2025, 23(1):51] | PubMed: 39985000 |
| Role of Rac1 in p53-Related Proliferation and Drug Sensitivity in Multiple Myeloma [ Cancers (Basel), 2025, 17(3)461] | PubMed: 39941828 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
