Datos técnicos
| Fórmula | C23H25ClN6O3 |
||||||||||
| Peso molecular | 468.94 | Número CAS | 761437-28-9 | ||||||||
| Solubilidad (25°C)* | In vitro | DMSO | 47 mg/mL (100.22 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | TAE226 (NVP-TAE226) es un potente inhibidor de FAK con una IC50 de 5,5 nM y modestamente potente para Pyk2, ~10 a 100 veces menos potente contra InsR, IGF-1R, ALK y c-Met. Este compuesto induce apoptosis. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
|||||||||||
| In vitro | NVP-TAE226 (< 1 μM) inhibe la autofosforilación de FAK (Tyr397) inducida por la matriz extracelular en células U87 privadas de suero. Este compuesto (< 1 μM) también inhibe la fosforilación de IGF-1R inducida por IGF-I y la actividad de sus genes diana posteriores como MAPK y Akt en células U87 y U251. Este químico (<10 μM) retrasa el crecimiento de las células tumorales y atenúa la progresión del ciclo celular en G(2)-M, lo que se asocia con una disminución de la expresión de la ciclina B1 y de la proteína cdc2 fosforilada (Tyr15) en ambas células U87 y U251. Este compuesto (1 μM) inhibe la invasión de las células tumorales en al menos un 50 % en comparación con el control en un ensayo de invasión Matrigel in vitro en líneas celulares de glioma. El tratamiento con este químico (1 μM) en líneas celulares de glioma que contienen p53 de tipo salvaje exhibe principalmente un arresto en G(2)-M, mientras que las líneas celulares de glioma que portan p53 mutado experimentan apoptosis, como lo demuestra la detección de la activación de la caspasa-3/7 y la escisión de la poli(ADP-ribosa) polimerasa y mediante un ensayo de apoptosis con Anexina V. Este compuesto (5 μM) inhibe la fosforilación de FAK en la línea celular de neuroblastoma humano SK-N-AS. El tratamiento con este químico (<10 μM) en la línea celular de neuroblastoma humano SK-N-AS conduce a una disminución de la viabilidad celular, un arresto del ciclo celular y un aumento de la apoptosis. Este compuesto (0,1 μM-10 μM) inhibe la formación de tubos de células HMEC1. | |||||||||||
| In vivo | NVP-TAE226 (75 mg/kg) aumenta significativamente la tasa de supervivencia de ratones con xenoinjertos de glioma intracraneal. Este compuesto (100 mg/kg, oral) ejerce una disminución significativa en la densidad de microvasos en un modelo de cáncer de colon humano en ratones SCID. Este químico (100 mg/kg, oral) inhibe eficientemente el crecimiento del tumor pancreático humano MIA PaCa-2 sin pérdida de peso corporal en un modelo in vivo. Inhibe el crecimiento del tumor mamario murino 4T1 y la metástasis al pulmón de manera dosis-dependiente en un modelo in vivo, asociado con la inhibición de la autofosforilación de FAK en Y397 y la fosforilación de Akt en Serine473. |
Protocolo (de referencia)
| Ensayo celular:[1] |
|
|---|---|
| Estudio en animales:[1] |
|
Referencias
|
Validación de productos por parte del cliente
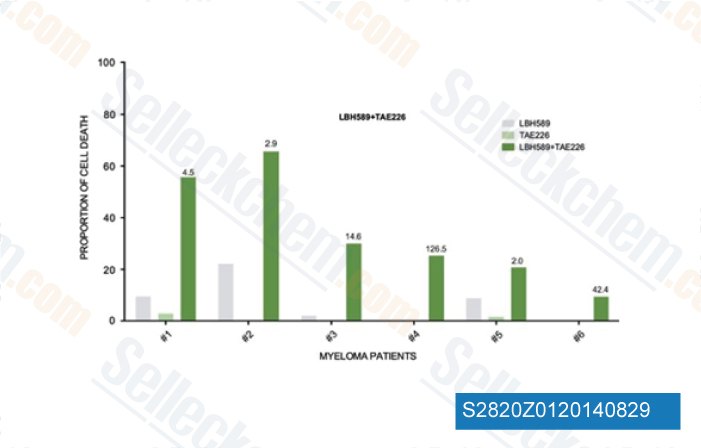
-
Datos de [ Cell Death Dis , 2014 , 5, e1134 ]
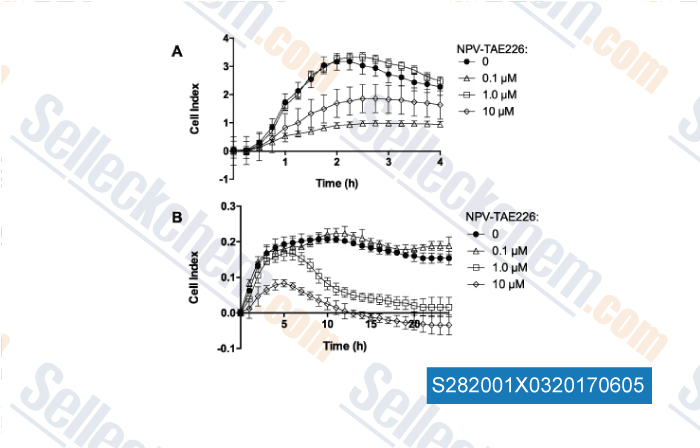
-
Datos de [ , , J Inorg Biochem, 2016, 160:225-35 ]
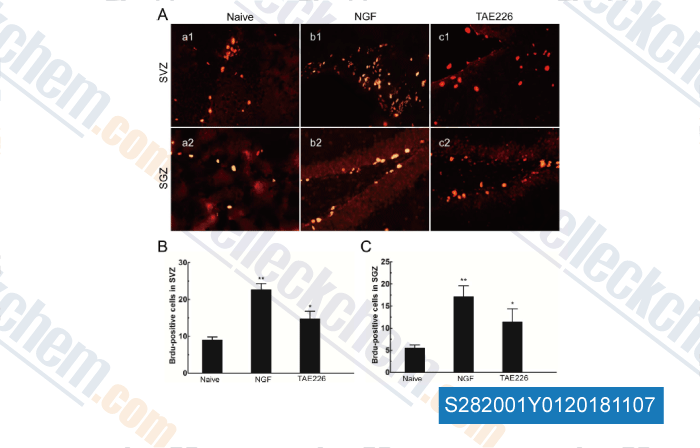
-
Datos de [ , , Neurosci Lett, 2018, 672:96-102 ]
Sellecks TAE226 (NVP-TAE226) Ha sido citado por 26 Publicaciones
| Aurora kinase A promotes epithelial‑mesenchymal transition by regulating P130 and P107 molecules in thyroid cancer cells [ Exp Ther Med, 2025, 29(5):93] | PubMed: 40162054 |
| Overexpression of BACH1 mediated by IGF2 facilitates hepatocellular carcinoma growth and metastasis via IGF1R and PTK2 [ Theranostics, 2022, 12(3):1097-1116] | PubMed: 35154476 |
| Mechanical coupling of supracellular stress amplification and tissue fluidization during exit from quiescence [ Proc Natl Acad Sci U S A, 2022, 119(32):e2201328119] | PubMed: 35914175 |
| Integrin αvβ3 Induces HSP90 Inhibitor Resistance via FAK Activation in KRAS-Mutant Non-Small Cell Lung Cancer [ Cancer Res Treat, 2022, 54(3):767-781] | PubMed: 34607394 |
| Three subtypes of lung cancer fibroblasts define distinct therapeutic paradigms [ Cancer Cell, 2021, S1535-6108(21)00492-X] | PubMed: 34624218 |
| TLR4 signalling via Piezo1 engages and enhances the macrophage mediated host response during bacterial infection [ Nat Commun, 2021, 12(1):3519] | PubMed: 34112781 |
| Focal adhesion kinase inhibition synergizes with nab-paclitaxel to target pancreatic ductal adenocarcinoma [ J Exp Clin Cancer Res, 2021, 91-2021)] | PubMed: None |
| Focal adhesion kinase inhibition synergizes with nab-paclitaxel to target pancreatic ductal adenocarcinoma [ J Exp Clin Cancer Res, 2021, 40(1):91] | PubMed: 33750427 |
| A first-in-class anticancer dual HDAC2/FAK inhibitors bearing hydroxamates/benzamides capped by pyridinyl-1,2,4-triazoles [ Eur J Med Chem, 2021, 222:113569] | PubMed: 34111829 |
| Campylobacter jejuni Triggers Signaling through Host Cell Focal Adhesions To Inhibit Cell Motility [ mBio, 2021, 12(4):e0149421] | PubMed: 34425711 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
