Datos técnicos
| Fórmula | C19H20N4O |
||||||||||
| Peso molecular | 320.39 | Número CAS | 1038915-60-4 | ||||||||
| Solubilidad (25°C)* | In vitro | DMSO | 64 mg/mL (199.75 mM) | ||||||||
| Ethanol | 64 mg/mL (199.75 mM) | ||||||||||
| Water | Insoluble | ||||||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Niraparib (MK-4827) es un inhibidor selectivo de PARP1/2 con una IC50 de 3,8 nM/2,1 nM, con gran actividad en células cancerosas con BRCA-1 y BRCA-2 mutantes. Es >330 veces selectivo frente a PARP3, V-PARP y Tank1. Este compuesto puede formar complejos PARP-ADN que provocan daño en el ADN, apoptosis y muerte celular. Fase 3. | ||||
|---|---|---|---|---|---|
| Objetivos |
|
||||
| In vitro | En un ensayo de células enteras, Niraparib (MK-4827) inhibió la actividad de PARP con un EC50 = 4 nM e inhibió la proliferación de células cancerosas con BRCA-1 y BRCA-2 mutantes con un CC50 en el rango de 10-100 nM. Se demostró que era un inhibidor potente y selectivo de PARP-1 y PARP-2 con IC50=3,8 y 2,1 nM, respectivamente. Además, este compuesto mostró al menos una selectividad 100 veces mayor sobre PARP-3, V-PARP y tankyrase-1, con IC50 = 1300, 330 y 570 nM, respectivamente. Además de inhibir el crecimiento de células HeLa deficientes en BRCA-1 debido al silenciamiento por interferencia de ARN, es capaz de inhibir la proliferación de líneas celulares cancerosas que portan mutaciones naturales de BRCA-1 o BRCA-2. En células de adenocarcinoma de glándula mamaria humana MDA-MB-436 que portan mutaciones de BRCA-1, mostró un CC50 = 18 nM, mientras que en células de adenocarcinoma pancreático humano CAPAN-1, que son mutantes de BRCA-2, mostró un CC50 = 90 nM. En contraste, las células epiteliales normales de próstata y mama humanas son resistentes a MK-4827, mostrando efectos antiproliferativos en el rango micromolar, demostrando así la muy alta citotoxicidad selectiva de estos inhibidores de PARP en células cancerosas mutantes BRCA-1 y -2 en comparación con el tejido circundante. | ||||
| In vivo | Niraparib (MK-4827), un nuevo inhibidor de PARP-1 y PARP-2 biodisponible por vía oral, mejoró fuertemente el efecto de la radiación en una variedad de xenoinjertos de tumores humanos, tanto p53 de tipo salvaje como p53 mutante. Fue bien tolerado in vivo y demostró eficacia como agente único en un modelo de xenoinjerto de cáncer deficiente en BRCA-1. |
Protocolo (de referencia)
| Ensayo celular:[2] |
|
|---|---|
| Estudio en animales:[1] |
|
Referencias
|
Validación de productos por parte del cliente
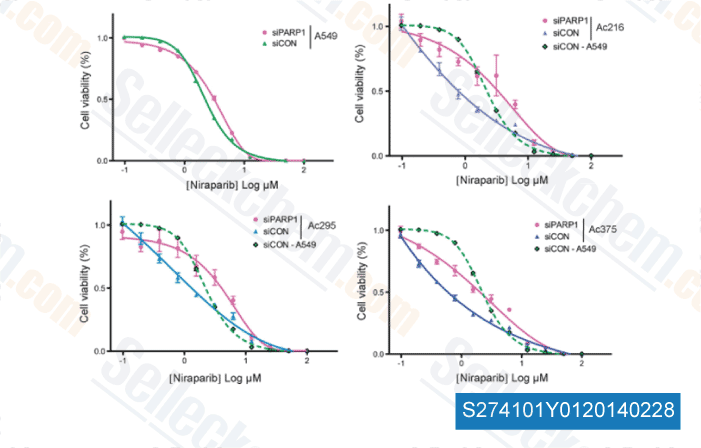
-
Datos de [ Oncogene , 2013 , 32(47):5377-87 ]
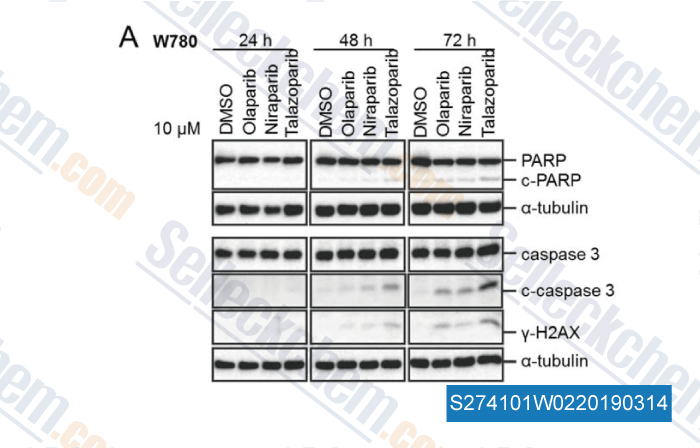
-
Datos de [ , , Theranostics, 2017, 7(17):4340-4349 ]
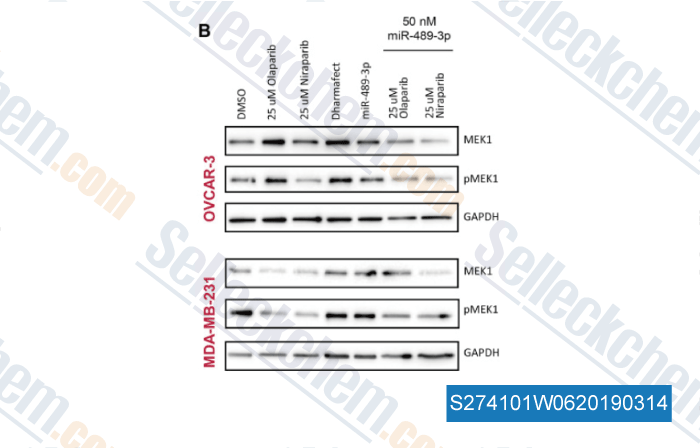
-
Datos de [ , , Cancer Lett, 2018, 432:84-92 ]
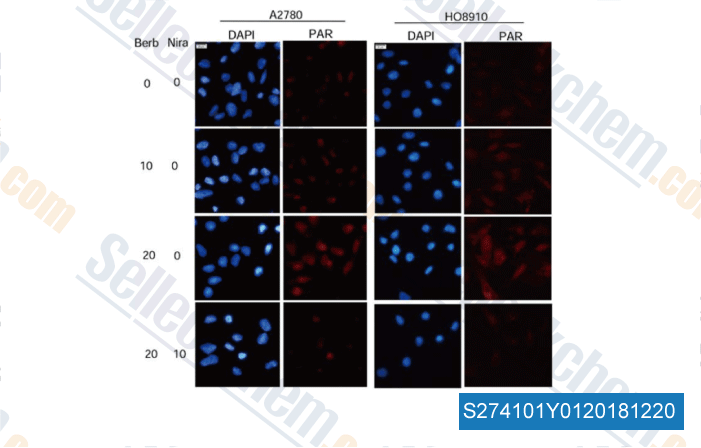
-
Datos de [ , , Cell Death Dis, 2017, 8(10):e3070 ]
Sellecks Niraparib (MK-4827) Ha sido citado por 112 Publicaciones
| HR eye & MMR eye: one-day assessment of DNA repair-defective tumors eligible for targeted therapy [ Nat Commun, 2025, 16(1):4239] | PubMed: 40355434 |
| Unfolded protein response kinase PERK supports survival and metastasis of circulating tumor cell clusters via SAM synthesis and H3K4me3-dependent PDGFB signaling [ Cancer Commun (Lond), 2025, 45(12):1706-1733.] | PubMed: 41212905 |
| Germline analysis of an international cohort of pediatric diffuse midline glioma patients [ Neuro Oncol, 2025, noaf061] | PubMed: 40072012 |
| XRCC1 mediates PARP1- and PAR-dependent recruitment of PARP2 to DNA damage sites [ Nucleic Acids Res, 2025, 53(4)gkaf086] | PubMed: 39970298 |
| Niraparib restricts intraperitoneal metastases of ovarian cancer by eliciting CD36-dependent ferroptosis [ Redox Biol, 2025, 80:103528] | PubMed: 39922130 |
| Combining Multiplexed CRISPR/Cas9-Nickase and PARP Inhibitors Efficiently and Precisely Targets Cancer Cells [ Cancer Res, 2025, 10.1158/0008-5472.CAN-24-2938] | PubMed: 40327605 |
| ZNF251 haploinsufficiency confers PARP inhibitors resistance in BRCA1-mutated cancer cells through activation of homologous recombination [ Cancer Lett, 2025, 613:217505] | PubMed: 39892701 |
| PARP inhibitor-induced anti-tumour chemokine response is suppressed by dipeptidyl peptidase 4 (DPP4) in ovarian cancer [ Br J Cancer, 2025, 10.1038/s41416-025-03076-4] | PubMed: 40579444 |
| LEF1 confers resistance to DNA-damaging chemotherapies through upregulation of PARP1 and NUMA1 in ovarian cancer [ Oncogene, 2025, 10.1038/s41388-025-03561-3] | PubMed: 40931049 |
| PARP inhibitors elicit distinct transcriptional programs in homologous recombination competent castration-resistant prostate cancer [ Mol Oncol, 2025, 10.1002/1878-0261.70098] | PubMed: 40915979 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
