Datos técnicos
| Fórmula | C26H33FN4O3S |
||||||
| Peso molecular | 500.63 | Número CAS | 1005342-46-0 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 100 mg/mL (199.74 mM) | ||||
| Ethanol | 100 mg/mL (199.74 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | LCL-161, un mimético de molécula pequeña second mitochondrial activator of caspase (SMAC), se une potentemente e inhibe múltiples IAPs (es decir, XIAP, c-IAP). | ||
|---|---|---|---|
| Objetivos |
|
||
| In vitro | LCL161 se une a los inhibidores de las proteínas de la apoptosis (IAPs) con alta afinidad e inicia la destrucción de cIAP1 y cIAP2, lo que induce aún más la apoptosis a través de la activación de caspasas. Este compuesto inhibe modestamente el crecimiento de células que expresan FLT3-ITD cuando se administra solo, con una IC50 que oscila entre ~0,5 μM (células Ba/F3-FLT3-ITD) y ~4 μM (células MOLM13-luc+). La potencia de este agente contra la mutante D835Y se observa considerablemente mayor, con una IC50 de ~50 nM cuando se prueba contra células Ba/F3-D835Y. El tratamiento de células MOLM13-luc+ con una combinación de este compuesto y PKC412 conduce a una destrucción significativamente mayor de células que cualquiera de los agentes solos, con índices de combinación de Calcusyn que sugieren sinergia. PKC412 y este químico inducen la apoptosis de células MOLM13-luc+. La combinación de PKC412 y este agente conduce a una mayor inducción de apoptosis que cualquiera de los agentes solos. Es capaz de anular el rescate mediado por el estroma de células que expresan FLT3 mutante a través de una combinación positiva con PKC412. Este compuesto inhibe el crecimiento de células Ba/F3.p210 con una IC50 de ~100 nM. También ha demostrado actividad contra células resistentes a fármacos que expresan mutaciones puntuales en las proteínas objetivo. Este agente a 1000 nM es capaz de matar en gran parte o completamente las líneas celulares derivadas de Ba/F3 que confieren resistencia a PKC412, las cuales expresan FLT3-ITD que albergan mutaciones puntuales en el bolsillo de unión a ATP de FLT3. También muestra actividad en concentraciones que van de 100 a 1000 nM contra células Ba/F3 que expresan diversas. Este compuesto se evalúa contra las 23 líneas celulares del panel in vitro del Programa Pediátrico de Pruebas Preclínicas (PPTP) usando 96 h. Logra una inhibición del 50% del crecimiento contra solo 3 de las 23 líneas celulares PPTP probadas bajo una concentración de 10 μM. Las tres líneas celulares incluyen dos líneas celulares de ALL de células T (COG-LL-317 y CCRF-CEM) y una línea celular de linfoma anaplásico de células grandes (Karpas-299), con CCRF-CEM y Karpas-299 mostrando los valores de IC50 relativos más bajos (0,25 y 1,6 μM, respectivamente). Muestra propiedades inmunomoduladoras en subconjuntos inmunes humanos. Los linfocitos T tratados con este compuesto demuestran una secreción de citoquinas significativamente mejorada tras la activación, con poco efecto sobre la supervivencia o proliferación de linfocitos T CD4 y CD8. El tratamiento con este agente de células mononucleares de sangre periférica mejora significativamente la activación de linfocitos T ingenuos con péptidos sintéticos in vitro. Las células dendríticas mieloides sufren maduración fenotípica con este químico y demuestran una capacidad reducida para presentar de forma cruzada una vacuna basada en antígenos tumorales. Estos efectos están potencialmente mediados por una activación observada de las vías NF-κB canónicas y no canónicas, después de este compuesto con una subsiguiente regulación al alza de moléculas antiapoptóticas. |
||
| In vivo | LCL161 mejora significativamente la capacidad de PKC412 para inhibir el crecimiento de células Ba/F3-FLT3-ITD-luc+ in vivo. También se demuestra que este compuesto se combina positivamente con los agentes quimioterapéuticos estándar, Ara-c y doxorrubicina, contra células que expresan FLT3-ITD y contra células que expresan D835Y. Se logra un efecto aditivo al combinar ambos químicos en la supresión del crecimiento de la leucemia. Este agente (100 mg/kg) mejora los efectos in vivo de dosis altas a moderadas sobre la carga de leucemia en ratones. Este compuesto se prueba contra los paneles in vivo del Programa Pediátrico de Pruebas Preclínicas (PPTP) (30 o 75 mg/kg [tumores sólidos] o 100 mg/kg [ALL]) administrado por vía oral dos veces por semana. Induce diferencias significativas en la distribución de EFS en aproximadamente un tercio de los xenoinjertos de tumores sólidos (osteosarcoma y glioblastoma), pero no en los xenoinjertos de ALL. No se observan respuestas tumorales objetivas. In vivo, este químico demuestra una actividad de agente único limitada contra los modelos preclínicos pediátricos estudiados. |
Protocolo (de referencia)
| Ensayo celular: |
|
|---|---|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
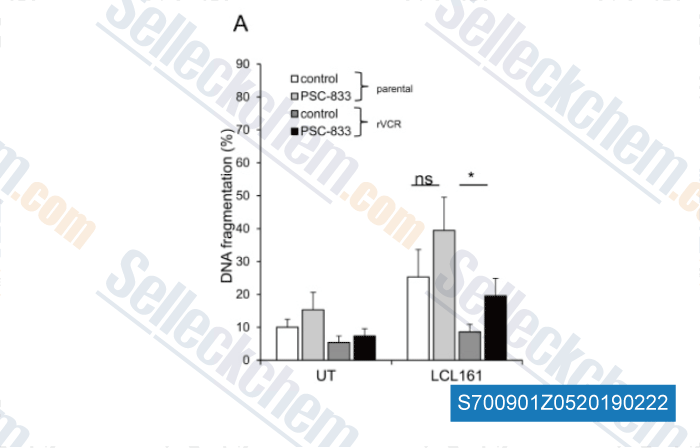
-
Datos de [ , , Cancer Lett, 2018, 440-441:126-134 ]
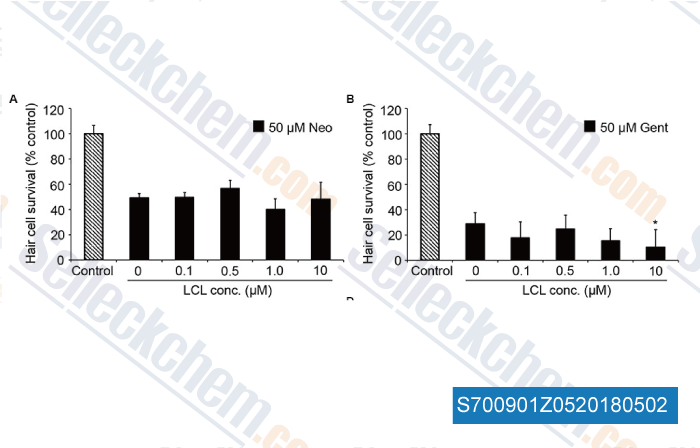
-
Datos de [ , , Front Cell Neurosci, 2017, https://doi.org/10.3389/fncel.2017.00326 ]
Sellecks LCL161 Ha sido citado por 48 Publicaciones
| Single-cell transcriptomic and functional studies identify glial state changes and a role for inflammatory RIPK1 signaling in ALS pathogenesis [ Immunity, 2025, 58(4):961-979.e8] | PubMed: 40132594 |
| Ferroptosis-activating metabolite acrolein antagonizes necroptosis and anti-cancer therapeutics [ Nat Commun, 2025, 16(1):4919] | PubMed: 40425585 |
| Targeting cIAP2 in a novel senolytic strategy prevents glioblastoma recurrence after radiotherapy [ EMBO Mol Med, 2025, 10.1038/s44321-025-00201-x] | PubMed: 39972068 |
| Astrocytes and the tumor microenvironment inflammatory state dictate the killing of glioblastoma cells by Smac mimetic compounds [ Cell Death Dis, 2024, 15(8):592] | PubMed: 39147758 |
| Combination of bazedoxifene with chemotherapy and SMAC-mimetics for the treatment of colorectal cancer [ Cell Death Dis, 2024, 15(4):255] | PubMed: 38600086 |
| Complex IIa formation and ABC transporters determine sensitivity of OSCC to Smac mimetics [ Cell Death Dis, 2024, 15(11):855] | PubMed: 39578442 |
| SPOP-mediated RIPK3 destabilization desensitizes LPS/sMAC/zVAD-induced necroptotic cell death [ Cell Mol Life Sci, 2024, 81(1):451] | PubMed: 39540935 |
| A comparative study of apoptosis, pyroptosis, necroptosis, and PANoptosis components in mouse and human cells [ PLoS One, 2024, 19(2):e0299577] | PubMed: 38412164 |
| Single-molecule fingerprinting of protein-drug interaction using a funneled biological nanopore [ Nat Commun, 2023, 14(1):1461] | PubMed: 37015934 |
| Dimethyl fumarate inhibits necroptosis and alleviates systemic inflammatory response syndrome by blocking the RIPK1-RIPK3-MLKL axis [ Pharmacol Res, 2023, 189:106697] | PubMed: 36796462 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
