Datos técnicos
| Fórmula | C29H31N7O |
||||||
| Peso molecular | 493.6 | Número CAS | 152459-95-5 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 98 mg/mL (198.54 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Imatinib es un inhibidor multi-objetivo de la tirosina quinasa con inhibición para v-Abl, c-Kit y PDGFR; los valores de IC50 son 0,6 μM, 0,1 μM y 0,1 μM en ensayos sin células o basados en células, respectivamente. Imatinib (STI571) induce la autofagia. | ||||||
|---|---|---|---|---|---|---|---|
| Objetivos |
|
||||||
| In vitro | Los ensayos in vitro para la inhibición de un panel de proteínas quinasas de tirosina y serina/treonina muestran que Imatinib inhibe potentemente la tirosina quinasa v-Abl y PDGFR con una IC50 de 0,6 y 0,1 μM, respectivamente. Este compuesto inhibe la activación dependiente de SLF de la actividad de la quinasa c-Kit de tipo salvaje con una IC50 para estos efectos de aproximadamente 0,1 μM, lo que es similar a la concentración requerida para la inhibición de PDGFR. Exhibe actividad inhibidora del crecimiento en la línea celular de carcinoide bronquial humana NCI-H727 y la línea celular de carcinoide pancreático humana BON-1 con una IC50 de 32,4 y 32,8 μM, respectivamente. Un estudio reciente muestra que este químico tiene el potencial de ejercer sus efectos antileucémicos en la leucemia mielógena crónica mediante la regulación a la baja de los canales K(+) hERG1, que se expresan altamente en las células leucémicas y parecen de excepcional importancia para favorecer la leucemogénesis. |
||||||
| In vivo | Imatinib produce un efecto antitumoral diferente en tres tumores xenoinjertados derivados de muestras quirúrgicas de cánceres de pulmón de células pequeñas humanos frescos, con una inhibición del crecimiento del 80 %, 40 % y 78 % de los tumores SCLC6, SCLC61 y SCLC108, respectivamente, y ninguna inhibición significativa del crecimiento de SCLC74. En ratones ApoE(-/-) alimentados con una dieta alta en grasas, este compuesto reduce significativamente el área de tinción lipídica inducida por la dieta alta en grasas en un 30 %, 27 % y 35 % en comparación con los controles no tratados con dieta alta en grasas cuando se administra por sonda a 10, 20 y 40 mg/kg, respectivamente, y suprime la acumulación de lípidos en la arteria carótida. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
Referencias
|
Validación de productos por parte del cliente
![<p> </p><p>Inhibition of thymidine (a and b) and cytarabine (c and d) uptake with imatinib. K562 cells (a and c) and MEG-01 cells (b and d) were incubated at 37 ◦C for 15 min with imatinib transport buffer, and then incubated with 0.5 Ci of [3H] thymidine or [3H] cytarabine for an additional 5 min in presence of imatinib. Cells were then washed 3 times, lysed and radioactivity associated to cell pellets was quantified. DMSO, dimethylsulfoxide; DPD, dipyridamole.</p>](https://file.selleckchem.com/downloads/review/700px/Imatinib-S247501Z0120130501.gif)
-
Datos de [ Leukemia Res , 2012 , 36, 1311-1314 ]
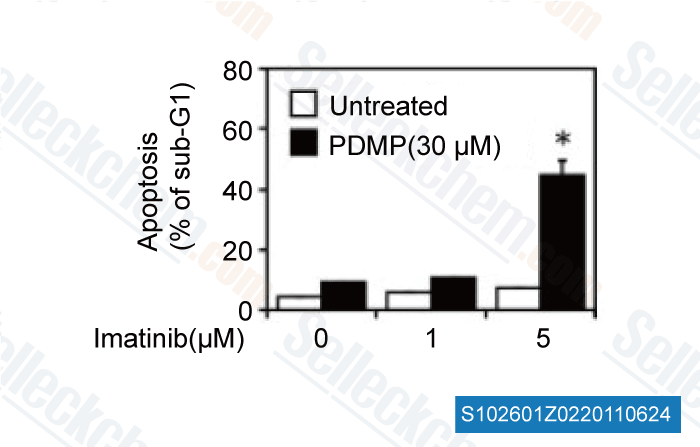
-
Datos de [ FASEB J , 2011 , 25, 3661-3673 ]
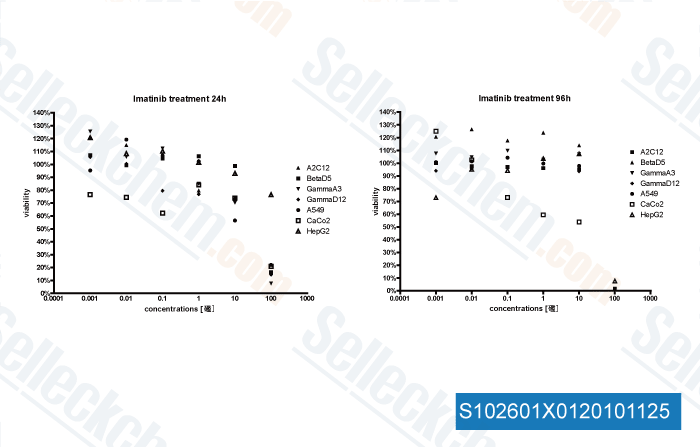
-
, , Dr. Thomas Kruwel of Fraunhofer
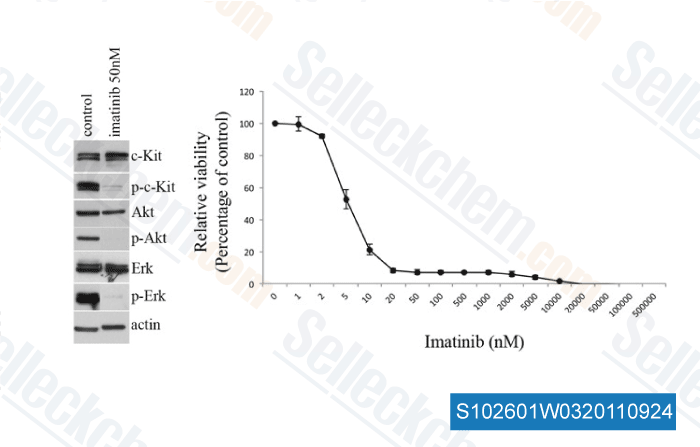
-
, , Dr. Helen Rizos from the university of Sydney
Sellecks Imatinib (STI571) Ha sido citado por 326 Publicaciones
| Proteogenomic characterization of non-functional pancreatic neuroendocrine tumors unravels clinically relevant subgroups [ Cancer Cell, 2025, 43(4):776-796.e14] | PubMed: 40185092 |
| CD19-targeted HSP90 inhibitor nanoparticle combined with TKIs reduces tumor burden and enhances T-cell immunity in murine B-cell malignancies [ Theranostics, 2025, 15(8):3589-3609] | PubMed: 40093890 |
| The landcape of Helicobacter pylori-mediated DNA breaks links bacterial genotoxicity to its oncogenic potential [ Genome Med, 2025, 17(1):14] | PubMed: 39994739 |
| Haploinsufficiency of miR-143 and miR-145 reveal targetable dependencies in resistant del(5q) myelodysplastic neoplasm [ Leukemia, 2025, 39(4):917-928] | PubMed: 40000845 |
| Systematic analysis of ZDHHC9 as a potential prognostic and immunotherapy biomarker in breast cancer [ Front Immunol, 2025, 16:1609621] | PubMed: 40740766 |
| Methylstat sensitizes ovarian cancer cells to PARP-inhibition by targeting the histone demethylases JMJD1B/C [ Cancer Gene Ther, 2025, 10.1038/s41417-025-00874-z] | PubMed: 39915607 |
| Activation of TMEM16E scramblase induces ligand independent growth factor receptor signaling and macropinocytosis for membrane repair [ Commun Biol, 2025, 8(1):35] | PubMed: 39794444 |
| Characterization of the Temporal Dynamics of the Endothelial-Mesenchymal-like Transition Induced by Soluble Factors from Dengue Virus Infection in Microvascular Endothelial Cells [ Int J Mol Sci, 2025, 26(5)2139] | PubMed: 40076764 |
| Senataxin and DNA-PKcs redundantly promote non-homologous end joining repair of DNA double strand breaks during V(D)J recombination [ Sci Adv, 2025, 11(25):eads5272] | PubMed: 40540553 |
| Utility of the Base Editing System for Introducing Drug-Resistant Gene Mutations Into Human Leukemia Cellular Models [ Cureus, 2025, 17(4):e81889] | PubMed: 40342439 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
