Datos técnicos
| Fórmula | C19H12ClN3O2 |
||||||
| Peso molecular | 349.77 | Número CAS | 1009820-21-6 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 69 mg/mL (197.27 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Silmitasertib (CX-4945) es un inhibidor potente y selectivo de CK2 (casein kinase 2) con una IC50 de 1 nM en un ensayo sin células, aunque es menos potente contra Flt3, Pim1 y CDK1 (inactivo en ensayo basado en células). Este compuesto induce Autophagy y promueve la apoptosis. Fase 1/2. | ||
|---|---|---|---|
| Objetivos |
|
||
| In vitro | Silmitasertib (CX-4945) es selectivo para CK2, ya que solo inhibe 7 de las 238 quinasas en más del 90% a una concentración de 0,5 μM, que es 500 veces mayor que el IC50 de CK2. Aunque en sistemas libres de células este compuesto inhibe FLT3, PIM1 y CDK1 con IC50 de 35 nM, 46 nM y 56 nM, respectivamente, el tratamiento a 10 μM es inactivo contra FLT3, PIM1 y CDK1 en ensayos funcionales basados en células. Exhibe un amplio espectro de actividad antiproliferativa, y las líneas celulares de cáncer de mama muestran el rango más amplio de sensibilidad a este con un EC50 de 1,71-20,01 μM. La actividad antiproliferativa de CX-4945 se correlaciona con los niveles de ARNm y proteínas de CK2α, pero no con la subunidad catalítica CK2α', la subunidad reguladora CK2β y el estado mutacional de PI3K/Akt o PTEN. Inhibe la señalización de PI3K/Akt bloqueando directamente la fosforilación de Akt en Serina 129 por CK2 en lugar de mediante la activación de PTEN. El tratamiento con este compuesto provoca una fosforilación reducida de p21 (T145), un aumento de los niveles totales de p21 y p27, y la inducción de la actividad de la caspasa 3/7. Induce una detención del ciclo celular G2/M en células BT-474 y una detención G1 en células BxPC-3. Este compuesto inhibe la proliferación, migración y formación de tubos de HUVEC con un IC50 de 5,5 μM, 2 μM y 4 μM, respectivamente. En condiciones hipóxicas en células BT-474 y BxPC-3, previene la regulación a la baja de p53 y pVHL y reduce la activación de la transcripción de HIF-1α. Inhibe potentemente la actividad intracelular endógena de CK2 con un IC50 de 0,1 μM en células Jurkat. |
||
| In vivo | La administración oral de Silmitasertib (CX-4945) a 25 mg/kg o 75 mg/kg dos veces al día muestra una potente actividad antitumoral en el modelo BT-474, con un TGI del 88 % y 97 %, respectivamente, y 2 de 9 animales en cada grupo mostrando una reducción de más del 50 % en el tamaño del tumor en comparación con el volumen tumoral inicial. En el modelo BxPC-3, el tratamiento con este compuesto a 75 mg/kg dos veces al día muestra un TGI del 93 % con 3 animales sin evidencia de tumor restante al final del período de tratamiento. En el modelo de xenoinjerto PC3, la administración del mismo a 25 mg/kg, 50 mg/kg o 75 mg/kg causa una inhibición del crecimiento tumoral con un TGI del 19 %, 40 % y 86 %, respectivamente. |
||
| Características | Primer inhibidor clínico de CK2. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
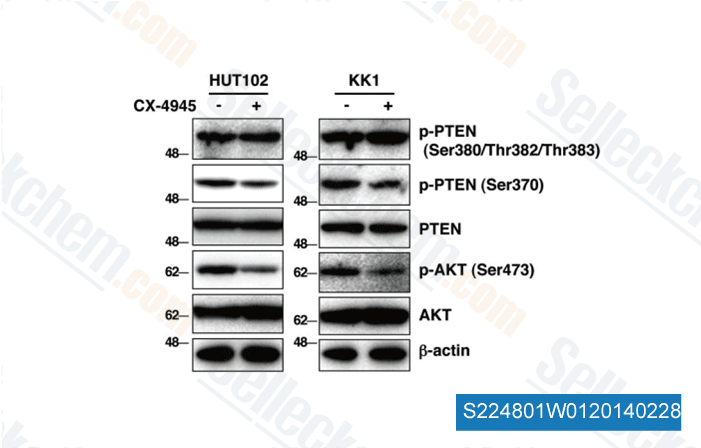
-
Datos de [ Nat Commun , 2014 , 5, 3393 ]
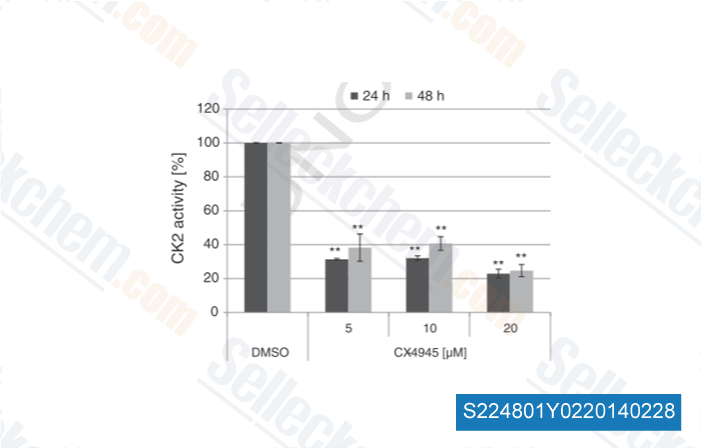
-
Datos de [ Cell Signal , 2014 , 26(7), 1567-75 ]
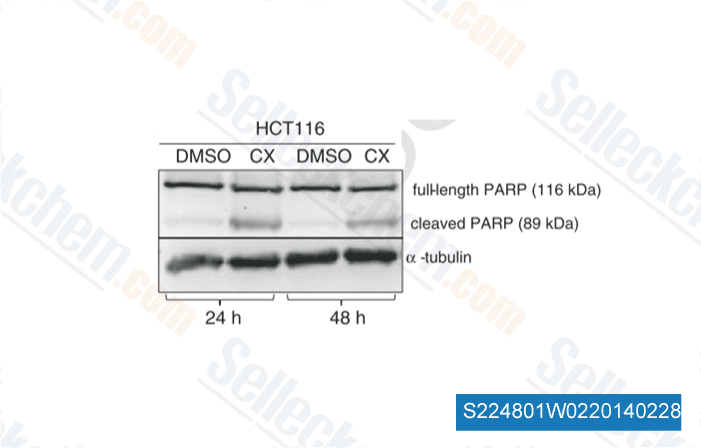
-
Datos de [ Cell Signal , 2014 , 26(7), 1567-75 ]
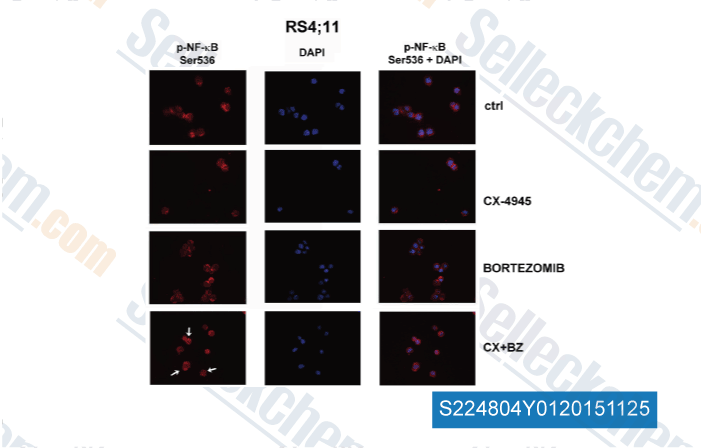
-
, , Oncotarget, 2015, 51: S659-S660
Sellecks Silmitasertib (CX-4945) Ha sido citado por 153 Publicaciones
| Reconstitution of BNIP3/NIX-mitophagy initiation reveals hierarchical flexibility of the autophagy machinery [ Nat Cell Biol, 2025, 27(8):1272-1287] | PubMed: 40715440 |
| Phosphorylation-dependent WRN-RPA interaction promotes recovery of stalled forks at secondary DNA structure [ Nat Commun, 2025, 16(1):997] | PubMed: 39870632 |
| Body weight control via protein kinase CK2: diet-induced obesity counteracted by pharmacological targeting [ Metabolism, 2025, 162:156060] | PubMed: 39521118 |
| CK2 regulates somatostatin expression in pancreatic delta cells [ Islets, 2025, 17(1):2515332] | PubMed: 40474387 |
| CK2 activity is crucial for proper glucagon expression [ Diabetologia, 2024, 10.1007/s00125-024-06128-1] | PubMed: 38503901 |
| Rutaecarpine alleviates inflammation and fibrosis by targeting CK2α in diabetic nephropathy [ Biomed Pharmacother, 2024, 180:117499] | PubMed: 39353318 |
| Protein kinase CK2α is overexpressed in classical hodgkin lymphoma, regulates key signaling pathways, PD-L1 and may represent a new target for therapy [ Front Immunol, 2024, 15:1393485] | PubMed: 38807597 |
| Mcam stabilizes a luminal progenitor-like breast cancer cell state via Ck2 control and Src/Akt/Stat3 attenuation [ NPJ Breast Cancer, 2024, 10(1):80] | PubMed: 39277578 |
| Protein kinase CK2 sustains de novo fatty acid synthesis by regulating the expression of SCD-1 in human renal cancer cells [ Cancer Cell Int, 2024, 24(1):432] | PubMed: 39726006 |
| Casein Kinase 2 Inhibitor, CX-4945, Induces Apoptosis and Restores Blood-Brain Barrier Homeostasis in In Vitro and In Vivo Models of Glioblastoma [ Cancers (Basel), 2024, 16(23)3936] | PubMed: 39682125 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
