Datos técnicos
| Fórmula | C22H17N3O6 |
||||||||||
| Peso molecular | 419.39 | Número CAS | 1009817-63-3 | ||||||||
| Solubilidad (25°C)* | In vitro | DMSO | 48 mg/mL (114.45 mM) | ||||||||
| Water | Insoluble | ||||||||||
| Ethanol | Insoluble | ||||||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | b-AP15 (NSC687852) es un inhibidor de deubiquitinases para la actividad de proteasomas 19S de la escisión de Ub-AMC con una IC50 de 2.1 μM. | ||||
|---|---|---|---|---|---|
| Objetivos |
|
||||
| In vitro | b-AP15 inhibe la actividad de dos DUBs asociadas a la partícula reguladora 19S, la Ubiquitin C-terminal hydrolase 5 (UCHL5) y la Ubiquitin-specific peptidase 14 (USP14), lo que resulta en la acumulación de poliubiquitina. Este compuesto provoca una acumulación dosis-dependiente del reportero UbG76V-YFP con una IC50 de 0.8 μM, lo que indica una degradación proteasomal deteriorada. (1 μM) provoca una rápida acumulación de proteínas poliubiquitinadas en células de carcinoma de colon humano HCT-116. Este químico (2.2 μM) aumenta las cantidades de las quinasas dependientes de ciclinas CDKN1A y CDKNIB y del supresor tumoral TP53 de manera dosis-dependiente sin alterar las cantidades de ornitina descarboxilasa 1 (ODC1) en células HCT-116. (1 μM) provoca una detención del ciclo celular en fase G2/M en células HCT-116, consistente con la acumulación de inhibidores del ciclo celular. El tratamiento con este compuesto aumenta el número de células hipodiploides y se asocia con un aumento en las cantidades de marcadores apoptóticos, incluyendo caspasa-3 activada, polimerasa de poli-ADP ribosa (PARP) escindida por caspasa y citoqueratina-18 (CK18). Es más tóxico para las células HCT-116 en comparación con las células epiteliales inmortalizadas (hTERT-RPE1) o las células mononucleares de sangre periférica. Este inhibidor inhibe la actividad de desubiquitinación utilizando una variedad de sustratos, incluyendo Ub-AMC, Ub-GFP22, el homólogo de la proteína de unión a p53 ubiquitinada (HDM2) y las cadenas tetraméricas de Ubiquitin unidas por K48 y K63. Es un inhibidor del UPS que indujo la muerte celular a través de la inducción de la vía de apoptosis lisosomal de manera dependiente de la catepsina-D. Este compuesto provoca defectos característicos del UPS, incluyendo la acumulación de conjugados de Ubiquitin e inhibidores del ciclo celular como p21, p27 y el supresor tumoral p53. Inhibe la actividad DUB de ambas DUBs de cisteína, siendo USP14 ligeramente más sensible que UCHL5. Este químico induce apoptosis en células que sobreexpresan la proteína antiapoptótica Bcl-2 y en células que carecen del gen p53. (1 μM) inhibe la liberación de IL-1β inducida por ATP de macrófagos peritoneales cebados con LPS. Este compuesto (1 μM) reduce los niveles de muerte celular inducidos por el tratamiento con nigericina en células THP-1. (1 μM) reduce significativamente el número de cuerpos ASC formados después del tratamiento con nigericina en células THP-1 cebadas con LPS. | ||||
| In vivo | b-AP15 (5 mg/kg) muestra una actividad antitumoral significativa en ratones SCID con xenoinjertos de carcinoma de células escamosas FaDu. Este compuesto retrasa significativamente la aparición del tumor en ratones con xenoinjertos de carcinoma de colon HCT-116. | ||||
| Características | No es un inhibidor general de DUB. Tiene una inhibición mínima sobre las DUBs de cisteína recombinantes y citosólicas no proteasomales. |
Protocolo (de referencia)
| Estudio en animales: |
|
|---|
Referencias
|
Validación de productos por parte del cliente
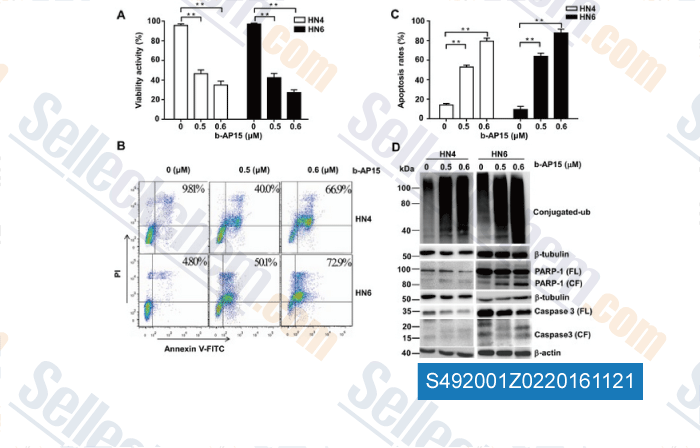
-
Datos de [ , , Int J Biochem Cell Biol, 2016, 79:350-359. ]
Sellecks b-AP15 Ha sido citado por 23 Publicaciones
| A chaperone-proteasome-based fragmentation machinery is essential for aggrephagy [ Nat Cell Biol, 2025, 27(9):1448-1464] | PubMed: 40866512 |
| Macrophage-targeting nano-formulated bicalutamide alleviates colitis by inducing MAP3K1-mediated degradation of NLRP3 [ J Control Release, 2025, 380:417-432] | PubMed: 39892647 |
| PSMC6 regulation of ovarian cancer cisplatin resistance unravels a new mode for proteasome targeting [ Int J Biol Sci, 2025, 21(5):2258-2274] | PubMed: 40083690 |
| Ubiquitin-specific protease 14 targets PFKL-mediated glycolysis to promote the proliferation and migration of oral squamous cell carcinoma [ J Transl Med, 2024, 22(1):193] | PubMed: 38388430 |
| A carboxy-terminal ubiquitylation site regulates androgen receptor activity [ Commun Biol, 2024, 7(1):25] | PubMed: 38182874 |
| An abundance of free regulatory (19S) proteasome particles regulates neuronal synapses [ Science, 2023, 380(6647):eadf2018] | PubMed: 37228199 |
| FAAH served a key membrane-anchoring and stabilizing role for NLRP3 protein independently of the endocannabinoid system [ Cell Death Differ, 2022, 10.1038/s41418-022-01054-4] | PubMed: 36104448 |
| Inhibition of proteasomal deubiquitinases USP14 and UCHL5 overcomes tyrosine kinase inhibitor resistance in chronic myeloid leukaemia [ Clin Transl Med, 2022, 12(9):e1038] | PubMed: 36082692 |
| Treatment with b-AP15 to Inhibit UCHL5 and USP14 Deubiquitinating Activity and Enhance p27 and Cyclin E1 for Tumors with p53 Deficiency [ Technol Cancer Res Treat, 2022, 21:15330338221119745] | PubMed: 35971329 |
| SF3B1 homeostasis is critical for survival and therapeutic response in T cell leukemia [ Sci Adv, 2022, 8(3):eabj8357] | PubMed: 35061527 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
