Datos técnicos
| Fórmula | C30H30O8.C2H4O2 |
||||||
| Peso molecular | 578.61 | Número CAS | 866541-93-7 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 116 mg/mL (200.48 mM) | ||||
| Ethanol | 89 mg/mL (153.81 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | El ácido (R)-(-)-Gossypol (AT-101) acético, el enantiómero R-(-) del ácido Gossypol acético, se une a Bcl-2, Bcl-xL y Mcl-1 con Ki de 0,32 μM, 0,48 μM y 0,18 μM en ensayos libres de células; no inhibe el dominio BIR3 y BID. El AT-101 desencadena simultáneamente apoptosis y un tipo citoprotector de autophagy. Fase 2. | ||||||
|---|---|---|---|---|---|---|---|
| Objetivos |
|
||||||
| In vitro | El AT-101 inhibe un panel de diferentes neoplasias linfoproliferativas con un IC50 que oscila entre 1,2 μM y 7,4 μM. El AT-101 (10 μM) altera el Δψm de manera dependiente de la concentración y el tiempo en líneas de linfoma difuso de células B grandes y de linfoma de células del manto. El AT-101 (1 μM o 2 μM) combinado con carfilzomib (6 nM o 10 nM) induce la apoptosis en las líneas celulares HBL-2 y Granta. El AT-101 (20 μM durante 24 horas) produce una apoptosis mediana del 72 % y una regulación a la baja de Mcl-1 en linfocitos de LLC tanto en cultivo en suspensión como en cocultivo estromal. Las células estromales expresan niveles indetectables de antiapoptóticos, pero niveles altos de proteínas ERK y AKT activadas y tienen poca o ninguna apoptosis con AT-101. El AT-101 induce la apoptosis de manera dependiente del tiempo y la dosis, con valores de ED50 de 1,9 mM y 2,4 mM en células Jurkat T y U937, respectivamente. El AT-101 (10 μM) combinado con radiación (32 Gy) induce más apoptosis que la radiación sola y excede la suma de los efectos causados por los tratamientos de agente único. El AT-101 activa SAPK/JNK de manera dependiente de la dosis y el tiempo. El AT-101 (10 µM) induce la apoptosis a través de la activación de caspasa-9, -3 y -7 en células VCaP. El AT-101 (10 µM) disminuye la expresión de Bcl-2 y Mcl-1 en células VCaP. El AT-101 (< 20 μM) es capaz de inhibir el crecimiento de células de mieloma múltiple a pesar de los efectos de crecimiento estimulantes proporcionados por las células estromales en el medio de la médula ósea. El AT-101 (10 μM) induce la apoptosis en células de mieloma múltiple a través de la activación de caspasas 3, caspasas 9 y PARP. El AT-101 (10 μM) promueve la apoptosis en células de mieloma múltiple al alterar la relación Bax/Bcl-2 y el potencial de membrana mitocondrial. | ||||||
| In vivo | El AT-101 sigue siendo detectable en plasma con concentraciones medias de 0,49 μM para el grupo de 35 mg/kg y 0,39 μM para el grupo de 200 mg/kg en ratones SCID beige portadores de xenoinjerto RL-DLBCL. La concentración plasmática máxima de AT-101 se observa después de 30 minutos de administración del fármaco en ambos niveles de dosis, mostrando el grupo de 200 mg/kg una concentración plasmática media casi 4 veces mayor que el grupo de 35 mg/kg (7,88 μM y 27,78 μM, respectivamente) en ratones SCID beige. El AT-101 (25 mg/kg a 100 mg/kg, oralmente) resulta indefinidamente en un inicio más temprano de pérdida de peso equivalente a más del 10% del peso previo al tratamiento y muerte en ratones SCID beige. El AT-101 (35 mg/kg, oralmente por día durante 10 días) más ciclofosfamida (Cy) intraperitoneal y rituximab (R) intraperitoneal muestran un control significativo del volumen tumoral en comparación con cualquier otro grupo de tratamiento. El AT-101 (15 mg/kg, p.o., 5 días/semana) como agente único en ratones intactos reduce significativamente el desarrollo del crecimiento tumoral de VCaP en comparación con los tumores no tratados en las semanas 2 a 6. El AT-101 en combinación con la castración quirúrgica retrasa el inicio del crecimiento tumoral de VCaP independiente de andrógenos en comparación con los grupos de solo castración o solo AT-101 en ratones. |
Protocolo (de referencia)
| Ensayo de quinasa:[1] |
|
|---|---|
| Ensayo celular:[2] |
|
| Estudio en animales:[2] |
|
Referencias
|
Validación de productos por parte del cliente
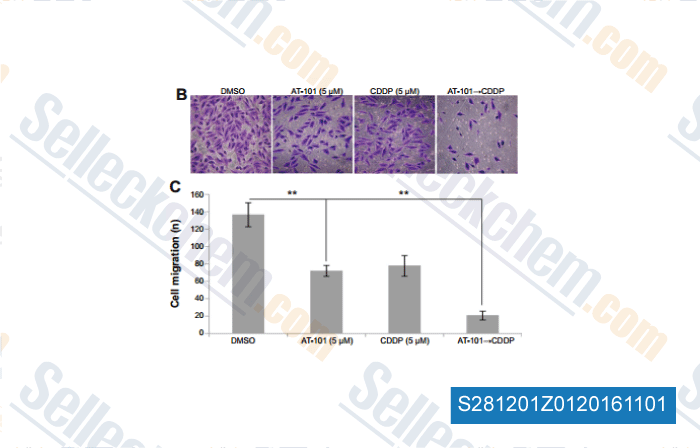
-
, , Drug Des Devel Ther, 2014, 8:2517-29.
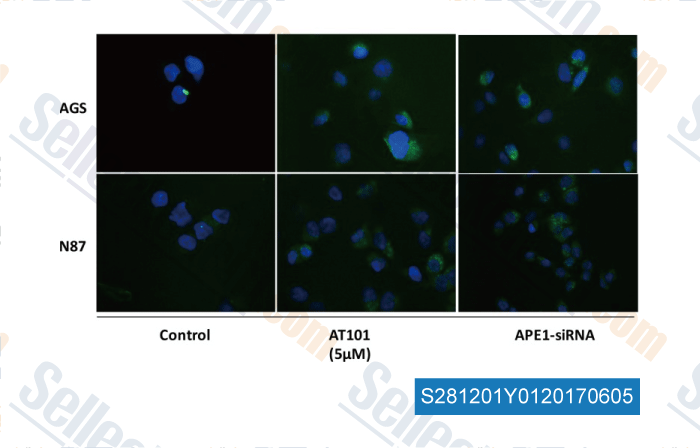
-
Datos de [ , , Oncotarget, 2016, 7(23):34430-41 ]
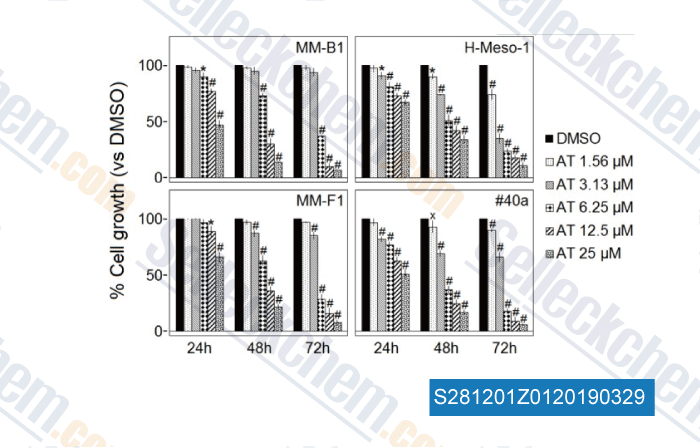
-
Datos de [ , , Front Pharmacol, 2018, 9:1269 ]
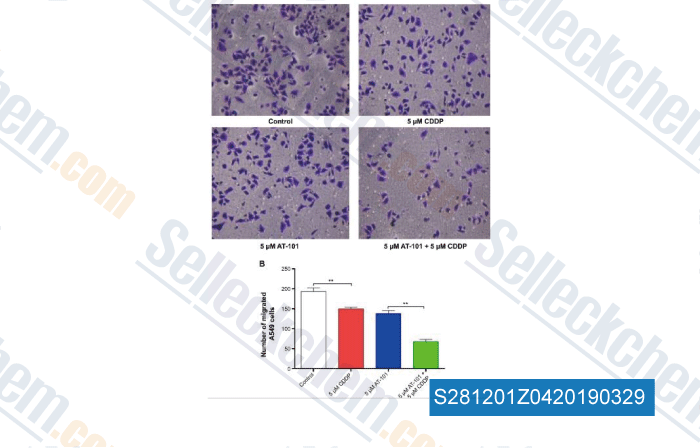
-
Datos de [ , , Drug Des Devel Ther, 2015, 9:2887-910 ]
Sellecks (R)-(-)-Gossypol (AT-101) acetic acid Ha sido citado por 20 Publicaciones
| Follicle stimulating hormone controls granulosa cell glutamine synthesis to regulate ovulation [ Protein Cell, 2024, pwad065] | PubMed: 38167949 |
| Pharmacological Targeting of Bcl-2 Induces Caspase 3-Mediated Cleavage of HDAC6 and Regulates the Autophagy Process in Colorectal Cancer [ Int J Mol Sci, 2023, 24(7)6662] | PubMed: 37047634 |
| Exploiting ulnerabilities induced b recurrent mutations in chondrosarcoma and giant cell tumour of bone: therapeutic targeting of the altered epigenome and be [ Leiden University The Netherlands, 2023, ] | PubMed: None |
| Integrative analysis of drug response and clinical outcome in acute myeloid leukemia [ Cancer Cell, 2022, S1535-6108(22)00312-9] | PubMed: 35868306 |
| Lactate Dehydrogenase B Is Required for Pancreatic Cancer Cell Immortalization Through Activation of Telomerase Activity [ Front Oncol, 2022, 12:821620] | PubMed: 35669414 |
| Gossypol Acetic Acid Attenuates Cardiac Ischemia/Reperfusion Injury in Rats via an Antiferroptotic Mechanism [ Biomolecules, 2021, 11(11)1667] | PubMed: 34827665 |
| AT101 [(-)-Gossypol] Selectively Inhibits MCL1 and Sensitizes Carcinoma to BH3 Mimetics by Inducing and Stabilizing NOXA [ Cancers (Basel), 2020, 12(8):E2298] | PubMed: 32824203 |
| Using CETSA assay and a mathematical model to reveal dual Bcl-2/Mcl-1 inhibition and on-target mechanism for ABT-199 and S1. [ Eur J Pharm Sci, 2020, 142:105105] | PubMed: 31669390 |
| Comparison of putative BH3 mimetics AT-101, HA14-1, sabutoclax and TW-37 with ABT-737 in platelets. [ Platelets, 2020, 10.1080/09537104.2020.1724276] | PubMed: 32079453 |
| Effect of Exosomal APE1 on Sensitivity of NSCLC A549 Cells to Cisplatin [ Cancer Research on Prevention and Treatment, 2020, (7): 492-497] | PubMed: None |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
