Datos técnicos
| Fórmula | C20H18ClF2N5O3 |
||||||
| Peso molecular | 449.84 | Número CAS | 1492952-76-7 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 90 mg/mL (200.07 mM) | ||||
| Ethanol | 30 mg/mL (66.69 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Asciminib (ABL001) es un inhibidor alostérico de ABL1 potente y selectivo con una constante de disociación (Kd) de 0,5-0,8 nM y selectividad por el bolsillo miristoílo de ABL1. | ||
|---|---|---|---|
| Objetivos |
|
||
| In vitro | Asciminib (ABL001) es un inhibidor de Bcr-Abl potente y selectivo que mantiene la actividad en la mayoría de las mutaciones, incluida la T315I, con un mecanismo de acción alostérico distinto. Se une a un sitio regulador típicamente ocupado por un grupo miristoílo en ABL de tipo salvaje e inhibe la actividad de la cinasa ABL a través de un mecanismo distinto de los inhibidores del sitio catalítico. Este compuesto se une a un bolsillo en el dominio de la cinasa BCR-ABL que normalmente está ocupado por el N-terminal miristoilado de ABL1. Tras la fusión con BCR, este N-terminal miristoilado que sirve para autorregular la actividad de ABL1 se pierde. ABL001 imita funcionalmente el papel del N-terminal miristoilado ocupando su sitio de unión vacante y restaura la regulación negativa de la actividad de la cinasa. Inhibe selectivamente el crecimiento de células de leucemia mieloide crónica (LMC) y LLA Ph+ con potencias que oscilan entre 1 y 10 nM, mientras que las líneas celulares BCR-ABL negativas permanecieron inafectadas a concentraciones 1000 veces mayores. Estudios de RMN y biofísicos confirman que se une potentemente (constante de disociación (Kd) = 0,5-0,8 nM) y selectivamente al bolsillo miristoílo de ABL1 e induce la conformación inactiva de la hélice C-terminal. Este compuesto carece de actividad contra más de 60 cinasas, incluida SRC, y es similarmente inactivo contra receptores acoplados a proteínas G, canales iónicos, receptores nucleares y transportadores. Por lo tanto, tiene una alta selectividad. |
||
| In vivo | En el modelo de xenoinjerto de ratón KCL-22, Asciminib (ABL001) muestra una potente actividad antitumoral con regresión tumoral completa observada y una clara correlación dosis-dependiente con la inhibición de pSTAT5. Tiene una absorción oral, un volumen de distribución y una vida media moderados en todas las especies. Este compuesto, como agente único, induce actividad antitumoral clínica y es bien tolerado hasta la fecha en un subgrupo de pacientes con leucemia mieloide crónica que han recibido tratamientos previos intensos. En cuanto a la farmacocinética, la farmacodinámica y la eficacia, las CL (aclaramiento) son de 12, 16 y 6 mL/min/kg en ratones, ratas y perros después de una dosis intravenosa única de 1 mg/kg, 2 mg/kg y 1 mg/kg, respectivamente. En ratones y perros, los T1/2term son de 1,1 y 3,7 h después de una dosis i.v. única de 1 mg/kg. En ratas, el T1/2term es de 2,7 h después de una dosis i.v. única de 2 mg/kg. La biodisponibilidad oral en ratones y ratas es del 35 % y 27 % respectivamente cuando se administra a 30 mg/kg p.o. Mientras que en perros la BA oral es del 111 % (15 mg/kg, p.o). |
Protocolo (de referencia)
| Ensayo celular: |
|
|---|---|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
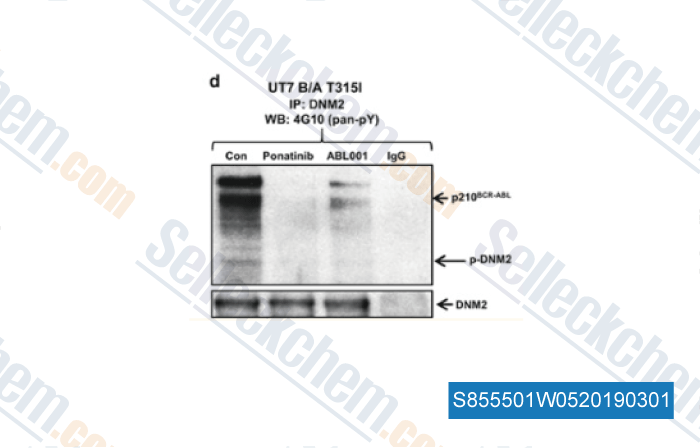
-
Datos de [ , , Leukemia, 2017, 31(11):2376-2387 ]
Sellecks ABL001 (Asciminib) Ha sido citado por 16 Publicaciones
| Asciminib resistance of a new BCR::ABL1 p.I293_K294insSSLRD mutant detected in a Ph + ALL patient [ Ann Hematol, 2025, 10.1007/s00277-024-06142-8] | PubMed: 39774950 |
| ABL1-mediated phosphorylation promotes FOXM1-related tumorigenicity by Increasing FOXM1 stability [ Cell Death Differ, 2024, 10.1038/s41418-024-01339-w] | PubMed: 39060421 |
| The molecular basis of Abelson kinase regulation by its αI-helix [ Elife, 2024, 12RP92324] | PubMed: 38588001 |
| Asciminib Maintains Antibody-Dependent Cellular Cytotoxicity against Leukemic Blasts [ Cancers (Basel), 2024, 16(7)1288] | PubMed: 38610966 |
| Sensitivity to Tyrosine Kinase Inhibitors in a Human Philadelphia Chromosome-Positive (Ph+) Leukemia Model With the T315I-Inclusive Compound Mutation [ Cureus, 2024, 16(12):e76538] | PubMed: 39872583 |
| Effect of asciminib and vitamin K2 on Abelson tyrosine-kinase-inhibitor-resistant chronic myelogenous leukemia cells [ BMC Cancer, 2023, 23(1):827] | PubMed: 37670241 |
| Využití vybraných inhibitorů k překonání anthracyklinové rezistence v terapii nádorových onemocnění (in vitro studie). [ Charles University, 2023, ] | PubMed: None |
| Reengineering Ponatinib to Minimize Cardiovascular Toxicity [ Cancer Res, 2022, 82-15:2777-2791] | PubMed: 35763671 |
| Allosteric Inhibition of c-Abl to Induce Unfolded Protein Response and Cell Death in Multiple Myeloma [ Int J Mol Sci, 2022, 23(24)16162] | PubMed: 36555805 |
| Allosteric Inhibition of c-Abl to Induce Unfolded Protein Response and Cell Death in Multiple Myeloma [ Int. J. Mol. Sci, 2022, 23(24), 16162] | PubMed: None |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
