Datos técnicos
| Fórmula | C23H19N3O2 |
||||||
| Peso molecular | 369.42 | Número CAS | 905854-02-6 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 73 mg/mL (197.6 mM) | ||||
| Ethanol | 12 mg/mL (32.48 mM) | ||||||
| Water | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Tivantinib es el primer inhibidor no competitivo de ATP de c-Met con un Ki de 0,355 μM en un ensayo sin células, poca actividad sobre Ron y ninguna inhibición sobre EGFR, InsR, PDGFRα o FGFR1/4. Este compuesto induce una detención G2/M y apoptosis. | ||
|---|---|---|---|
| Objetivos |
|
||
| In vitro | Se ha demostrado que ARQ-197 previene las respuestas celulares inducidas por HGF/c-met in vitro. Este compuesto posee actividad antitumoral; inhibiendo la proliferación de células A549, DBTRG y NCI-H441 con una IC50 de 0,38, 0,45, 0,29 μM. El tratamiento con este agente resulta en una disminución de la fosforilación de la cascada de señalización MAPK y la prevención de la invasión y migración. Además, la expresión ectópica de c-Met en NCI-H661, una línea celular sin expresión endógena de c-Met, hace que adquiera un fenotipo invasivo que también es suprimido por este químico. Aunque la adición de concentraciones crecientes de este inhibidor no afecta significativamente el Km de ATP, la exposición de c-Met a 0,5 μM de esta sustancia disminuyó la Vmax de c-Met en aproximadamente 3 veces. La capacidad de esta molécula para disminuir la Vmax sin afectar el Km de ATP confirmó que inhibe c-Met a través de un mecanismo no-ATP-competitivo y, por lo tanto, puede explicar su alto grado de selectividad de quinasa. Previene el c-Met recombinante humano con una constante inhibidora calculada Ki de aproximadamente 355 nM. Aunque la concentración más alta de ATP utilizada es de 200 μM, la potencia de este compuesto contra c-Met no se reduce al usar concentraciones de ATP de hasta 1 mM. Bloquea la fosforilación de c-Met y las vías de señalización de c-Met aguas abajo. Este químico suprime la autofosforilación constitutiva y mediada por ligando de c-Met y, por extensión, la actividad de c-Met, lo que a su vez conduce a la inhibición de los efectores de c-Met aguas abajo. Su inducción de apoptosis dependiente de caspasas se incrementa en células cancerosas humanas que expresan c-Met, incluidas las células HT29, MKN-45 y MDA-MB-231. |
||
| In vivo | Los tres modelos de xenoinjertos tratados con Tivantinib muestran reducciones en el crecimiento tumoral: 66% en el modelo HT29, 45% en el modelo MKN-45 y 79% en el modelo MDA-MB-231. En estos estudios de xenoinjertos, no se observaron cambios significativos en el peso corporal después de la administración oral de este compuesto a 200 mg/kg. Farmacodinámicamente, la fosforilación de c-Met en tumores de xenoinjertos de colon humano (HT29) se inhibe fuertemente por este químico, según se evaluó por una reducción dramática de la autofosforilación de c-Met 24 horas después de una dosis oral única de 200 mg/kg de este agente. Esta misma dosis en ratones exhibe que los xenoinjertos tumorales están expuestos a niveles plasmáticos sostenidos del compuesto, consistente con la inhibición farmacodinámica observada de la fosforilación de c-Met y la inhibición de la proliferación de líneas celulares cancerosas que albergan c-Met. Los niveles plasmáticos del agente 10 horas después de la dosificación se determinaron en 1,3 μM, más de 3 veces por encima de la constante inhibidora bioquímica de esta sustancia para c-Met. Por lo tanto, es capaz de suprimir su objetivo in vivo en el tejido tumoral humano xenoinjertado. En conclusión, este inhibidor bloquea el crecimiento de tumores humanos xenoinjertados dependientes de c-Met. |
||
| Características | El primer inhibidor selectivo de c-Met en avanzar a ensayos clínicos en humanos. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
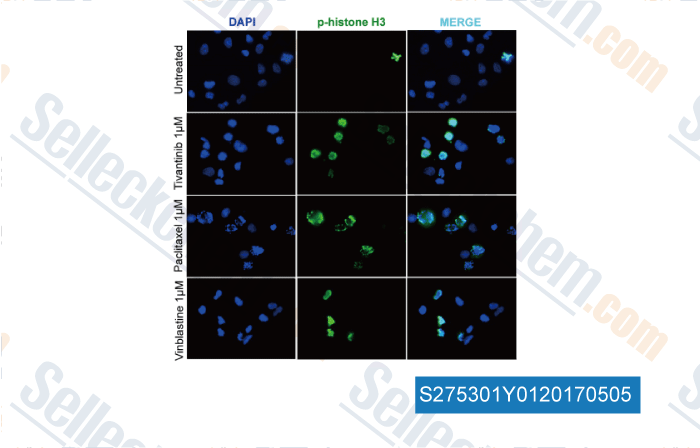
-
, , Clin Cancer Res, 2017, 23(15):4364-4375
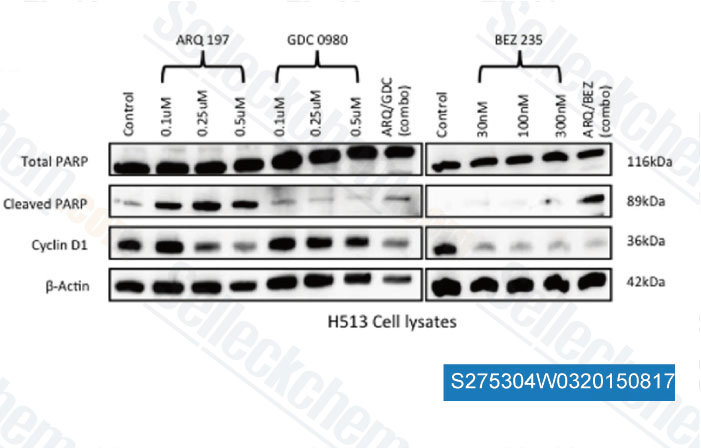
-
Datos de [ , , PLoS One, 2014, 9(9): e105919 ]
Sellecks Tivantinib Ha sido citado por 50 Publicaciones
| MET receptor serves as a promising target in melanoma brain metastases [ Acta Neuropathol, 2024, 147(1):44] | PubMed: 38386085 |
| Insulin receptor substrate 1 is a novel member of EGFR signaling in pancreatic cells [ Eur J Cell Biol, 2024, 103(4):151457] | PubMed: 39326351 |
| EZH2/hSULF1 axis mediates receptor tyrosine kinase signaling to shape cartilage tumor progression [ Elife, 2023, 12e79432] | PubMed: 36622753 |
| A community challenge for a pancancer drug mechanism of action inference from perturbational profile data [ Cell Rep Med, 2022, 3(1):100492] | PubMed: 35106508 |
| High-Resolution Profiling of Lung Adenocarcinoma Identifies Expression Subtypes with Specific Biomarkers and Clinically Relevant Vulnerabilities [ Cancer Res, 2022, 82(21):3917-3931] | PubMed: 36040373 |
| High-resolution profiling of lung adenocarcinoma identifies expression subtypes with specific biomarkers and clinically relevant vulnerabilities [ Cancer Res, 2022, CAN-22-0432] | PubMed: 36040373 |
| Ring Finger Protein 125 Is an Anti-Proliferative Tumor Suppressor in Hepatocellular Carcinoma [ Cancers (Basel), 2022, 14(11)2589] | PubMed: 35681566 |
| Establishment and Characterization of NCC-PMP1-C1: A Novel Patient-Derived Cell Line of Metastatic Pseudomyxoma Peritonei [ J Pers Med, 2022, 12(2)258] | PubMed: 35207746 |
| MTBP enhances the activation of transcription factor ETS-1 and promotes the proliferation of hepatocellular carcinoma cells [ Front Oncol, 2022, 12:985082] | PubMed: 36106099 |
| MET Inhibition Sensitizes Rhabdomyosarcoma Cells to NOTCH Signaling Suppression [ Front Oncol, 2022, 12:835642] | PubMed: 35574376 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
