Datos técnicos
| Fórmula | C19H21F2N7O2 |
||||||
| Peso molecular | 417.41 | Número CAS | 475110-96-4 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 21 mg/mL (50.31 mM) | ||||
| Water | Insoluble | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | ZSTK474 inhibe las isoformas de clase I de PI3K con una IC50 de 37 nM en un ensayo sin células, principalmente PI3Kδ. Fase 1/2. | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
||||||||||
| In vitro | ZSTK474 a 1 μM reduce potentemente la actividad de PI3K al 4,7% del nivel de control, mientras que LY2194002 solo reduce la actividad al 44,6% del control. Este compuesto inhibe las actividades de las p110β, -γ y -δ recombinantes con IC50 de 17 nM, 53 nM y 6 nM, respectivamente. Muestra una potente actividad antiproliferativa contra un panel de 39 líneas celulares de cáncer humano con una GI50 media de 0,32 μM, más eficazmente que la de LY294002 o wortmannin con una GI50 media de 7,4 μM o 10 μM, respectivamente. Este tratamiento químico a 1 μM bloquea el ruffling de la membrana y la generación de PIP3 inducida por el factor de crecimiento derivado de plaquetas en fibroblastos embrionarios murinos (MEF). A 10 μM induce la apoptosis en células OVCAR3, e induce la detención completa de la fase G1 pero no la apoptosis en células A549. Este tratamiento con el compuesto a 0,5 μM disminuye significativamente el nivel de Akt y GSK-3β fosforilados, así como la expresión de la proteína ciclina D1. También inhibe la fosforilación de otros componentes de señalización aguas abajo que están implicados en la regulación de la proliferación celular, incluyendo FKHRL1, FKHR, TSC-2, mTOR y p70S6K de una manera dosis-dependiente. Este químico no inhibe mTOR a 0,1 μM, e incluso a una concentración de 100 μM, inhibe la actividad de mTOR en menos del 40%. Bloquea la migración celular inducida por VEGF y la formación de tubos en células endoteliales de vena umbilical humana (HUVEC), e inhibe la expresión de HIF-1α y la secreción de VEGF en células RXF-631L, exhibiendo una potente actividad antiangiogénica in vitro. Este tratamiento con el compuesto inhibe la producción de IFNγ e IL-17 en células T activadas por concanavalina A, e inhibe la proliferación y la producción de PGE(2) por células sinoviales similares a fibroblastos (FLS). |
||||||||||
| In vivo | La administración oral de ZSTK474 inhibe el crecimiento de tumores de melanoma B16F10 de ratón implantados subcutáneamente de manera dosis-dependiente, produciendo una regresión tumoral del 28,5%, 7,1% o 4,9% el día 14 a 100, 200 o 400 mg/kg, respectivamente, lo que es superior a la de los cuatro principales fármacos anticancerosos a sus respectivas dosis máximas tolerables con una regresión tumoral del 96%, 35,7%, 24% o 68,3%, respectivamente. Este tratamiento con el compuesto a 400 mg/kg inhibe completamente el crecimiento de xenoinjertos de A549, PC-3 y WiDr en ratones, e induce la regresión de los tumores de xenoinjertos de A549. Inhibe significativamente el crecimiento tumoral en el modelo de xenoinjerto RXF-631L, correlacionado con una reducción significativa del número de microvasos en los ratones tratados. La administración oral de este químico mejora la progresión de la artritis inducida por adyuvante (AIA) en ratas. | ||||||||||
| Características | Primer inhibidor de PI3K administrado por vía oral utilizado in vivo. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
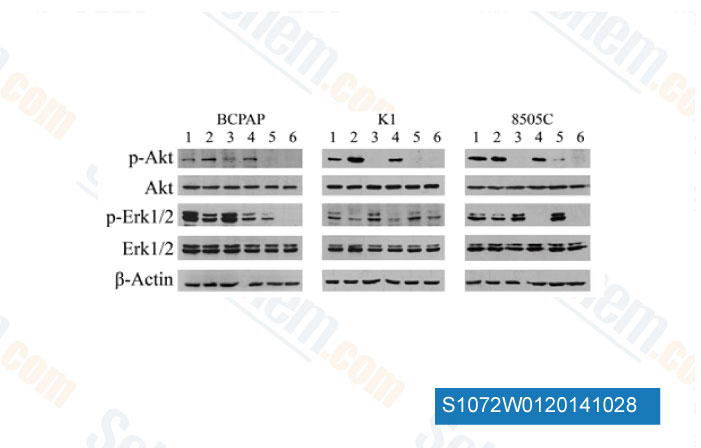
-
Datos de [ Invest New Drugs , 2014 , 32(4), 626-35 ]
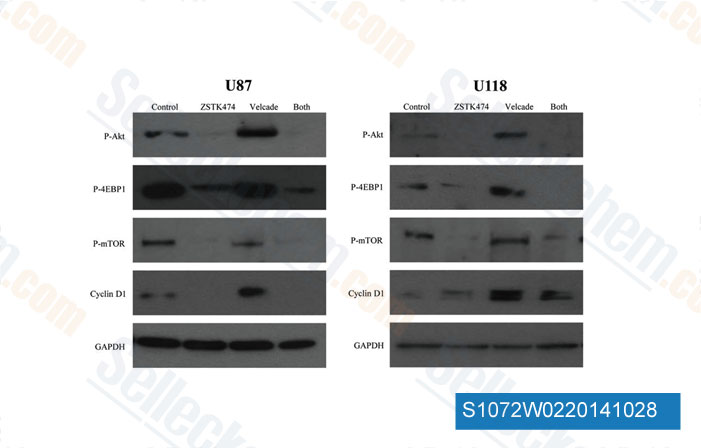
-
Datos de [ Int J Oncol , 2014 , 44(2), 557-62 ]
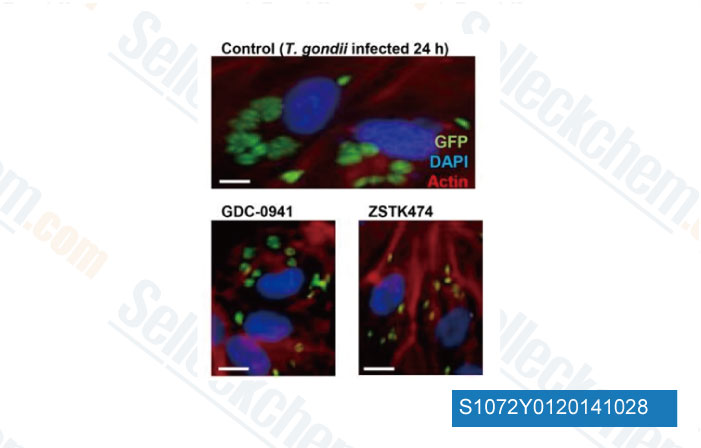
-
Datos de [ PLoS One , 2013 , 8(6), e66306 ]
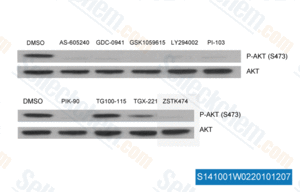
-
, , Saraswati Sukumar of Johns Hopkins University School of Medicine
Sellecks ZSTK474 Ha sido citado por 85 Publicaciones
| PI3K-Akt signalling regulates Scx-lineage tenocytes and Tppp3-lineage paratenon sheath cells in neonatal tendon regeneration [ Nat Commun, 2025, 16(1):3734] | PubMed: 40254618 |
| Perinatal thymic-derived CD8αβ-expressing γδ T cells are innate IFN-γ producers that expand in IL-7R-STAT5B-driven neoplasms [ Nat Immunol, 2024, 10.1038/s41590-024-01855-4] | PubMed: 38802512 |
| Perinatal thymic-derived CD8αβ-expressing γδ T cells are innate IFN-γ producers that expand in IL-7R-STAT5B-driven neoplasms [ Nat Immunol, 2024, 25(7):1207-1217] | PubMed: 38802512 |
| Reporter cell lines to screen for inhibitors or regulators of the KRAS-RAF-MEK1/2-ERK1/2 pathway [ Biochem J, 2024, 481(6):405-422] | PubMed: 38381045 |
| B cell adapter for PI 3-kinase (BCAP) coordinates antigen internalization and trafficking through the B cell receptor [ Sci Adv, 2024, 10(46):eadp1747] | PubMed: 39546610 |
| Multiplex single-cell chemical genomics reveals the kinase dependence of the response to targeted therapy [ Cell Genom, 2024, 4(2):100487] | PubMed: 38278156 |
| Stellettin B Sensitizes Glioblastoma to DNA-Damaging Treatments by Suppressing PI3K-Mediated Homologous Recombination Repair [ Adv Sci (Weinh), 2023, 10(3):e2205529] | PubMed: 36453577 |
| Young and undamaged recombinant albumin alleviates T2DM by improving hepatic glycolysis through EGFR and protecting islet β cells in mice [ J Transl Med, 2023, 21(1):89] | PubMed: 36747238 |
| HDAC Inhibition Restores Response to HER2-Targeted Therapy in Breast Cancer via PHLDA1 Induction [ Int J Mol Sci, 2023, 24(7)6228] | PubMed: 37047202 |
| Multiplex single-cell chemical genomics reveals the kinase dependence of the response to targeted therapy [ bioRxiv, 2023, 10.1101/2023.03.10.531983] | PubMed: None |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
