Datos técnicos
| Fórmula | C21H16ClF3N4O3.C7H8O3S |
||||||
| Peso molecular | 637.03 | Número CAS | 475207-59-1 | ||||
| Solubilidad (25°C)* | In vitro | DMSO | 127 mg/mL (199.36 mM) | ||||
| Water | 0.01 mg/mL (0.01 mM) | ||||||
| Ethanol | Insoluble | ||||||
| In vivo (Agregue los solventes al producto individualmente y en orden.) |
|
||||||
|
* <1 mg/ml significa ligeramente soluble o insoluble. * Tenga en cuenta que Selleck prueba la solubilidad de todos los compuestos internamente, y la solubilidad real puede diferir ligeramente de los valores publicados. Esto es normal y se debe a ligeras variaciones entre lotes. * Envío a temperatura ambiente (Las pruebas de estabilidad demuestran que este producto se puede enviar sin medidas de refrigeración.) |
|||||||
Preparación de soluciones madre
Actividad biológica
| Descripción | Sorafenib Tosylate es un inhibidor multiquinasa de Raf-1 y B-Raf con una IC50 de 6 nM y 22 nM en ensayos libres de células, respectivamente. Sorafenib Tosylate inhibe VEGFR-2, VEGFR-3, PDGFR-β, Flt-3 y c-KIT con una IC50 de 90 nM, 20 nM, 57 nM, 59 nM y 68 nM, respectivamente. Sorafenib Tosylate induce la autophagy y la apoptosis y activa la ferroptosis con actividad antitumoral. | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Objetivos |
|
|||||||||||
| In vitro | Sorafenib tosylate inhibe la actividad de B-Raf tanto de tipo salvaje como mutante V599E con una IC50 de 22 nM y 38 nM, respectivamente. Este compuesto también inhibe potentemente mVEGFR2 (Flk-1), mVEGFR3, mPDGFRβ, Flt3 y c-Kit con una IC50 de 15 nM, 20 nM, 57 nM, 58 nM y 68 nM, respectivamente. Inhibe débilmente FGFR-1 con una IC50 de 580 nM. Este químico no es activo contra ERK-1, MEK-1, EGFR, HER-2, IGFR-1, c-Met, PKB, PKA, cdk1/cyclinB, PKCα, PKCγ y pim-1. Inhibe marcadamente la fosforilación de VEGFR2 en células NIH 3T3 con una IC50 de 30 nM, y la fosforilación de Flt-3 en células HEK-293 con una IC50 de 20 nM. Bloquea potentemente la fosforilación de MEK 1/2 y ERK 1/2 en la mayoría de las líneas celulares, pero no en las células A549 o H460, mientras que no tiene efecto sobre la inhibición de la vía PKB. Inhibe la proliferación de células HAoSMC y MDA-MB-231 con una IC50 de 0,28 μM y 2,6 μM, respectivamente. Además de la inhibición de la vía de señalización RAF/MEK/ERK, inhibe significativamente la fosforilación de eIF4E y disminuye los niveles de Mcl-1 en células de carcinoma hepatocelular (HCC) de manera independiente de MEK/ERK. Inhibe la proliferación de células PLC/PRF/5 y HepG2 con una IC50 de 6,3 μM y 4,5 μM, respectivamente, y conduce a una inducción significativa de apoptosis. |
|||||||||||
| In vivo | La administración oral de Sorafenib tosylate (~60 mg/kg) demuestra una actividad antitumoral de amplio espectro y dependiente de la dosis contra una variedad de modelos de xenoinjertos tumorales humanos, incluyendo MDA-MB-231, Colo-205, HT-29, DLD-1, NCI-H460 y A549, sin evidencia de toxicidad. En asociación con la eficacia antitumoral, el tratamiento con este compuesto inhibe potentemente la fosforilación de MEK 1/2 y los niveles de pERK 1/2 en xenoinjertos HT-29 y MDA-MB-231, pero no en xenoinjertos Colo-205, y suprime significativamente el área de microvasos tumorales (MVA) y la densidad de microvasos (MVD) en xenoinjertos tumorales MDA MB-231, HT-29 y Colo-205. Este tratamiento con este compuesto produce una inhibición del crecimiento dependiente de la dosis de xenoinjertos tumorales PLC/PRF/5 en ratones SCID con TGI del 49% y 78% a 10 mg/kg y 30 mg/kg, respectivamente, lo que es consistente con la inhibición de la fosforilación de ERK y eIF4E, la reducción del área de microvasos y la inducción de la apoptosis de las células tumorales. |
Protocolo (de referencia)
| Ensayo de quinasa: |
|
|---|---|
| Ensayo celular: |
|
| Estudio en animales: |
|
Referencias
|
Validación de productos por parte del cliente
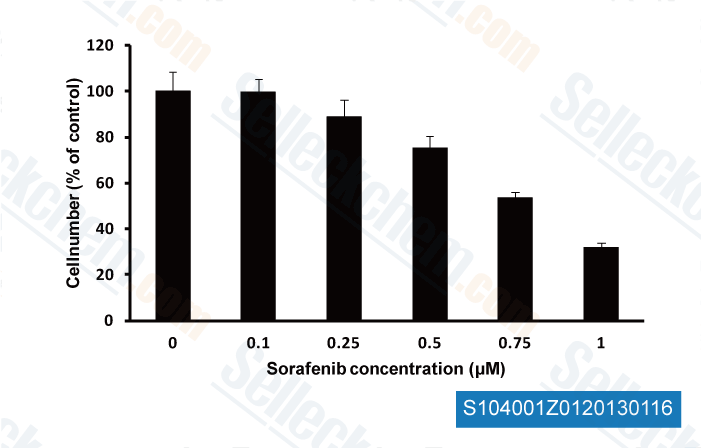
-
, 2013 , Christina W Yde/CDM Danish Cancer Society Research Center Denmark
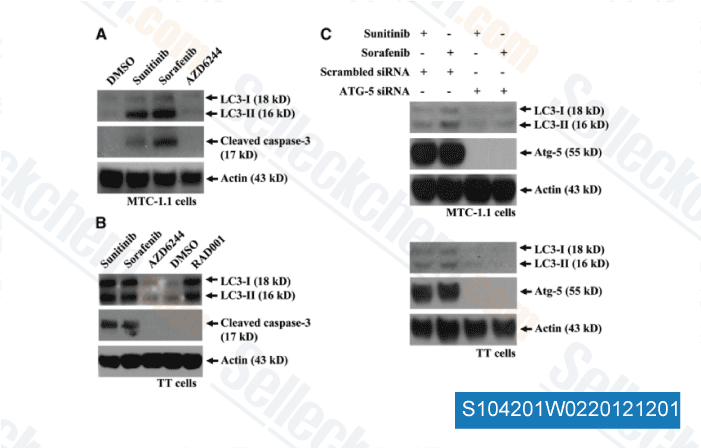
-
Datos de [ Surgery , 2012 , 152(6), 1142-9 ]
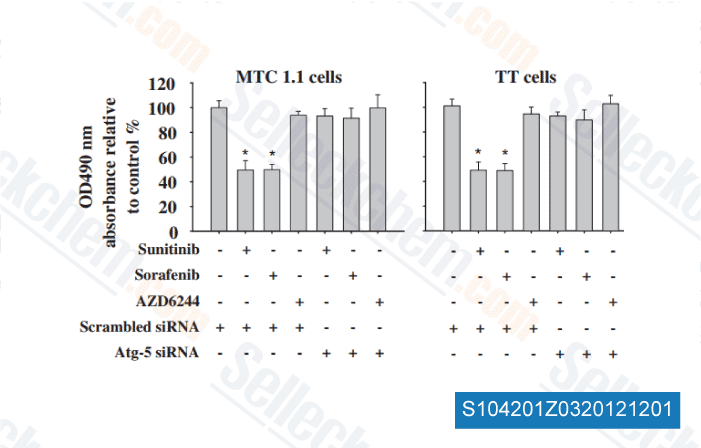
-
Datos de [ Surgery , 2012 , 152(6), 1142-9 ]
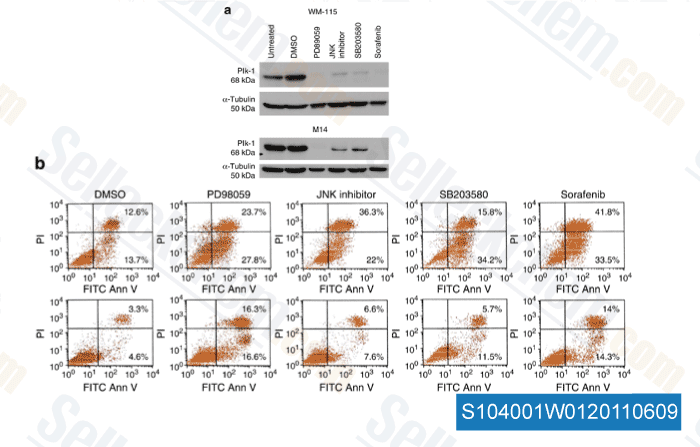
-
Datos de [ J Invest Dermatol , 2011 , 131, 1886–1895 ]
Sellecks Sorafenib Tosylate (BAY 43-9006) Ha sido citado por 274 Publicaciones
| Inhibiting SSBP1 enhances ferroptosis and improves the effectiveness of sorafenib treatment for liver cancer [ Int J Oncol, 2025, 67(3)72] | PubMed: 40747667 |
| Tumour-selective activity of RAS-GTP inhibition in pancreatic cancer [ Nature, 2024, 629(8013):927-936] | PubMed: 38588697 |
| Targeting NG2 relieves the resistance of BRAF-mutant thyroid cancer cells to BRAF inhibitors [ Cell Mol Life Sci, 2024, 81(1):238] | PubMed: 38795180 |
| Mitochondrial GCN5L1 acts as a novel regulator for iron homeostasis to promote sorafenib sensitivity in hepatocellular carcinoma [ J Transl Med, 2024, 22(1):593] | PubMed: 38918793 |
| IL-22 signaling promotes sorafenib resistance in hepatocellular carcinoma via STAT3/CD155 signaling axis [ Front Immunol, 2024, 15:1373321] | PubMed: 38596684 |
| Patient-derived rhabdomyosarcoma cells recapitulate the genetic and transcriptomic landscapes of primary tumors [ iScience, 2024, 27(10):110862] | PubMed: 39319271 |
| EZH2 suppresses ferroptosis in hepatocellular carcinoma and reduces sorafenib sensitivity through epigenetic regulation of TFR2 [ Cancer Sci, 2024, 115(7):2220-2234] | PubMed: 38623968 |
| Upregulation of LHPP by saRNA inhibited hepatocellular cancer cell proliferation and xenograft tumor growth [ PLoS One, 2024, 19(5):e0299522] | PubMed: 38696452 |
| Gravitational and mechanical forces drive mitochondrial translation [ bioRxiv, 2024, 10.1101/2023.01.18.524628] | PubMed: none |
| Arginine reprograms metabolism in liver cancer via RBM39 [ Cell, 2023, 186(23):5068-5083.e23] | PubMed: 37804830 |
POLÍTICA DE DEVOLUCIÓN
La Política de Devolución Incondicional de Selleck Chemical garantiza una experiencia de compra en línea fluida para nuestros clientes. Si no está satisfecho con su compra de alguna manera, puede devolver cualquier artículo(s) dentro de los 7 días posteriores a su recepción. En caso de problemas de calidad del producto, ya sean problemas relacionados con el protocolo o con el producto, puede devolver cualquier artículo(s) dentro de los 365 días a partir de la fecha de compra original. Siga las instrucciones a continuación al devolver productos.
ENVÍO Y ALMACENAMIENTO
Los productos Selleck se transportan a temperatura ambiente. Si recibe el producto a temperatura ambiente, tenga la seguridad de que el Departamento de Inspección de Calidad de Selleck ha realizado experimentos para verificar que la colocación a temperatura normal durante un mes no afectará la actividad biológica de los productos en polvo. Después de la recogida, guarde el producto de acuerdo con los requisitos descritos en la hoja de datos. La mayoría de los productos Selleck son estables en las condiciones recomendadas.
NO PARA USO HUMANO, DIAGNÓSTICO VETERINARIO O TERAPÉUTICO.
